Echinococcus multilocularis (rävens dvärgbandmask) är en bandmask med livscykel hos räv och gnagare.
Människan kan bli accidentell mellanvärd och då utveckla en levertumör (alveolär ekinokockos) med allvarlig prognos utan behandling.
Från att mycket sällan ha diagnostiserats tidigare har under de senaste två åren sex fall av infektion med E multilocularis påvisats i Sverige.
Leverförändringen misstolkas ofta radiologiskt såsom en malign tumör.
Diagnosen ställs med hjälp av radiologi och serologi men kan bekräftas med histopatologi och PCR av vävnad.
Behandlingen är kirurgisk och medikamentell.
Echinococcus multilocularis (rävens dvärgbandmask) är en bandmask som kan ge upphov till en mycket allvarlig leversjukdom (alveolär ekinokockos). I Sverige har tidigare enbart enstaka fall av infektionen upptäckts. De senaste två åren har dock totalt sex patienter som författarna känner till, fyra i Lund/Malmö samt vardera en i Linköping och Stockholm, diagnostiserats med E multilocularis-infektion, varför en ökad uppmärksamhet på sjukdomen är påkallad – särskilt för radiologer, patologer och kirurger. Nedan följer en översikt om sjukdomen samt en beskrivning av de sex svenska fallen.
Livscykel
E multilocularis har räven som huvudvärd och lever i dess tarm. Ägg produceras av den vuxna bandmasken, utsöndras med rävens avföring och förtärs sedan av mellanvärden, oftast en smågnagare. I mellanvärden kläcks ägget i tarmen, och larven penetrerar tarmväggen och förs med portaflödet till levern. I levern utvecklas ett larvstadium i form av en multicystisk tumör, som kallas metacestod. Cirkeln sluts genom att gnagarens lever äts upp av en räv, och från larvstadiet utvecklas en vuxen bandmask i rävens tarm. Den vuxna bandmasken består av ett huvud (scolex) samt 2–6 segment (proglottider) och är inte längre än 7 mm. Äggen är 30–40 µm och kan inte särskiljas morfologiskt från andra bandmaskarters ägg [1]. De är motståndskraftiga mot yttre påverkan och kan vara infektiösa i mer än ett år i lagom fuktig och varm miljö. De dör av torka och hög värme (60–80 °C i 5 minuter) men överlever i månader i en vanlig hushållsfrys (–18 °C). Däremot avdödar frysning ner till –83 °C äggen inom ett par dagar [2].
Experimentella studier har visat att mårdhundar och domesticerade hundar är väl så goda huvudvärdar som rävar, däremot inte katter [3].
Människan kan accidentellt agera mellanvärd, det vill säga i gnagarens ställe, genom att få i sig ägg från en infekterad huvudvärd. Det kan ske genom direktkontakt med en räv eller hund. En annan väg är genom ägg i föda eller vatten. Ägg kan spridas passivt via flugor från plats till plats [1].
E multilocularis ska särskiljas och inte förväxlas med Echinococcus granulosus (cystisk ekinokockos), som också är en bandmask men har en helt annan livscykel, vanligen mellan får och hund, och som ger andra kliniska symtom med stora cystor i företrädesvis levern. Vid infektion med E granulosus ses radiologiskt i levern en välavgränsad rund–oval cystbildning, vars vägg kan ha en dubbelkontur. Innehållet varierar efter cystans ålder. Cystor i tidigt stadium innehåller homogen vätska. Senare bildas så kallade dottercystor i den ursprungliga cystan, vilket ger ett multivesikulärt utseende. Gamla cystor blir heterogent tätare, och kan till slut till större delen förkalkas [4].
Epidemiologi
E multilocularis förekommer främst på det norra halvklotet. Områden med känd förekomst i Europa inkluderar bland annat Frankrike, Tyskland, Schweiz, Tjeckien, Österrike, Polen, Ryssland, Turkiet och Baltikum. I centrala Europa rapporteras ca 100–150 fall av infektion hos människa årligen, och prevalensen hos rävar kan vara upp till 50 procent [5]. Incidensen i europeiska högendemiska områden, såsom södra Tyskland och nordöstra Frankrike, är 5–8 fall per 100 000 invånare/år [6]. Högendemiska områden utanför Europa är centrala Asien, Iran, Kina inkluderande Tibet, Mongoliet, Korea, Japan, Kanada, Alaska och nordcentrala USA [7].
I en fall–kontrollstudie av 40 fall från Tyskland var riskfaktorer för infektion med E multilocularis att vara lantbrukare, äga jakthund, odla grönsaker, äta osköljda jordgubbar samt ha för vana att tugga på grässtrån. Man bör dock nämna att den totala riskökningen var låg för dessa faktorer med tanke på sjukdomens sällsynthet [8].
I Sverige har E multilocularis sedan 2011 påvisats hos både rävar och gnagare i ringa omfattning (< 1 procent) i Småland, västra Götaland, Södermanland och Dalarna [9, 10]. Fall där människa drabbats är mycket få, hittills 9 fall sedan 2012. Men de senaste två åren har fall diagnostiserats där det kan misstänkas att Sverige varit smittolandet [11].
Klinik
Huvudlokalisationen för metacestodstadiet är nästan alltid levern, vanligtvis högra leverloben – troligen på grund av dess större blodtillflöde. Metacestodstadiet ger där upphov till en infiltrativ och destruerande tumör av varierande storlek (upp till 20 cm), ibland med central nekros. Spridning från levern kan ske till i första hand lungorna men även i undantagsfall till andra organ såsom mjälte, hjärna och skelett. Tid från smitta till symtom anges i litteraturen till 5–15 år. Sjukdomen upptäcks i ca två tredjedelar av fallen under utredning av kolestatisk ikterus eller buksmärtor. I en tredjedel av fallen upptäcks den accidentellt vid röntgenundersökning. SR kan vara förhöjd, troligen på grund av hyperimmunglobulinemi. Eosinofili förekommer som regel inte [1].
Primär extrahepatisk infektion med E multilocularis, det vill säga utan någon samtidig levertumör, anses mycket ovanlig.
Obehandlad är åkomman ofrånkomligt dödlig 10–15 år efter diagnos, men med modern behandling är prognosen betydligt bättre. I en schweizisk långtidsstudie från 2008 innebar diagnosen genomsnittligt enbart tre års minskning av förväntad livslängd [12]. Troligen kan spontanläkning ske med degeneration och kalcifiering, men hur ofta detta sker är oklart [1]. Immunförsvaret spelar en stor roll för att hålla parasiten i schack, och vid immunsuppression sker snabbare progress [13].
Diagnostik
Diagnostiken vilar i huvudsak på tre ben: radiologi, serologi och histopatologi (PAD).
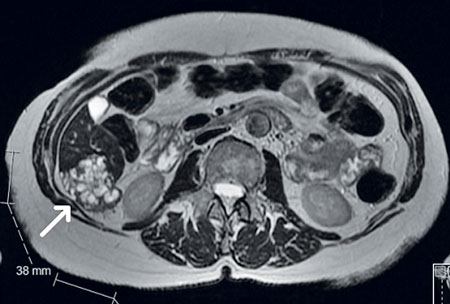
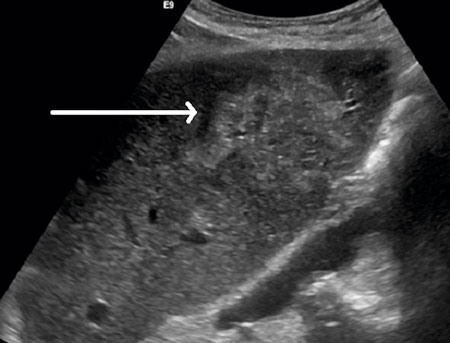
Flera radiologiska modaliteter kan användas för diagnostik av leverförändringen [14]. Skiktröntgen utan kontrast visar en oskarpt begränsad tumörliknande förändring med heterogena inre strukturer med eller utan förkalkningar (Figur 1). Lätt kontrastuppladdning kan ses i periferin. Hypodensa nekrotiska områden kan även ses centralt. MR visualiserar inte de karakteristiska förkalkningarna lika väl, men de små cystorna framträder bättre. De riktigt små cystorna representerar vesiklar av metacestodstadiet, medan större cystbildningar består av likvifierade nekroser (Figur 2). På ultraljud ses leverförändringen med heterogena ekogena partier med eller utan förkalkningar (Figur 3). PET-DT används framför allt som uppföljande undersökning efter behandling. Upptag av fluor-18-fluorodeoxiglukos har föreslagits antyda viabilitet och ses i periferin av lesionen, men beror troligen mer på värdens inflammatoriska reaktion än parasiten i sig [15, 16].
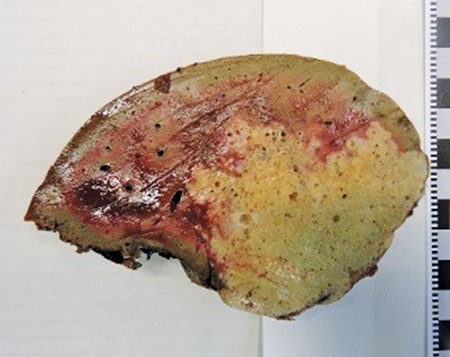
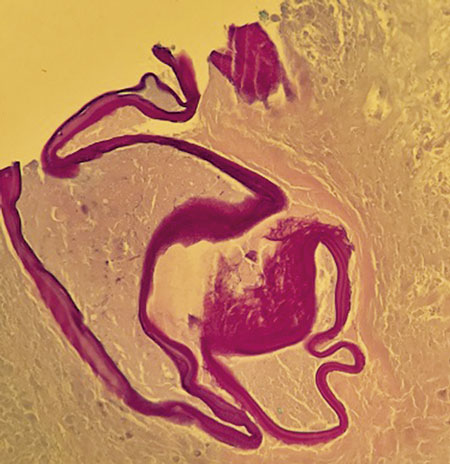
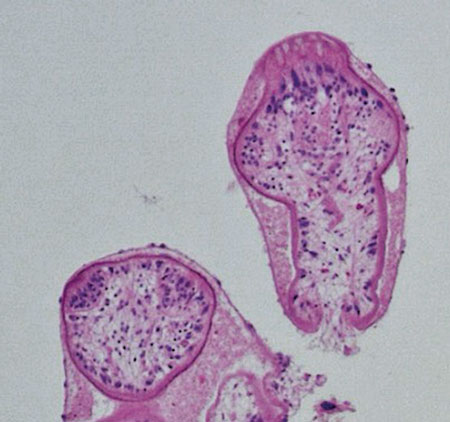
Patoanatomiskt ses makroskopiskt en alveolär struktur med oregelbundna cystor i storleken 1–30 mm (Figur 4). På grund av nekrosbildning kan hålrum ses med flytande till fast nekrotiskt material. Mikroskopiskt innehåller cystorna ett tunt PAS (perjodsyra–Schiff)-positivt lamellärt membran, ibland även ett tunt germinallager (Figur 5). Protoscolices, förstadier till bandmaskhuvuden, (Figur 6) ses mycket sällan, < 1 procent. Cystorna är omgivna av nekroser. Kalcifiering och kronisk inflammation med främmandekroppsreaktion kan också ses [1].
Serologi för att påvisa antikroppar utförs av Folkhälsomyndigheten med både ELISA och western blot-teknik och har hög känslighet (> 95 procent). Båda metoderna är positiva också vid infektion med E granulosus, men bandmönstret vid western blot visar ofta ett artrelaterat mönster. Vid positiv serologi skickas provet vidare till utländskt laboratorium för karakterisering av subklasser av antikroppar. Efter radikal kirurgisk behandling blir några subklasser ofta negativa och kan användas som bedömningshjälp vid uppföljningar [17].
Nålbiopsi avråds av vissa författare då den kan medföra risk för spridning. Detta har visats vara möjligt i djurexperiment, men samtidigt har nålbiopsier på människor utförts i studier utan konstaterad spridning [18, 19].
På senare tid har även PCR-teknik på vävnad utvecklats för diagnostik av ekinokockos, och undersökningen kan utföras vid utländskt laboratorium via Folkhälsomyndighetens försorg. Sekvensering av PCR-produkten ger ofta säker artbestämning [20].
Behandling
Behandlingen är kirurgisk och medikamentell. WHO har publicerat en stadieindelning av alveolär ekinokockos till hjälp för behandlingsbedömning [20]. Om möjligt ska leverförändringen tas bort radikalt med minst 2 cm marginal såsom vid en malign tumör. Om detta inte är möjligt bör man undvika tumörreducerande kirurgi [21].
Efter radikal operation ges antihelmintisk behandling i form av albendazol under 2 år. Albendazol är i Sverige ett licenspreparat. Om tillståndet inte är operabelt ges albendazol livslångt. Albendazolkoncentrationen bör kontrolleras. I sällsynta fall utförs levertransplantation [20].
Sex svenska fall
De senaste två åren har infektion med E multilocularis diagnostiserats hos sex patienter, som artikelförfattarna känner till. Medelåldern vid diagnos var 61 år (spridning 44–87 år) och fem av patienterna var kvinnor. Fem patienter hade svenskt ursprung och en hade ursprung i ett E multilocularis-endemiskt land, men hade bott i Sverige i 30 år utan att ha varit tillbaka i sitt forna hemland. Var och hur de smittats går inte med säkerhet att avgöra. Samtliga hade gjort kortvariga resor till E multilocularis-endemiska områden, såsom Centraleuropa, inom rimlig inkubationstid.
I samtliga fall upptäcktes en levertumör under utredning av buksmärtor. Tre av dem bedömdes såsom misstänkta cystadenokarcinom respektive kolangiokarcinom, och i dessa fall genomgick patienterna direkt leverresektion där diagnosen sedan ställdes via PAD postoperativt. I ett fall genomfördes en diagnostisk laparoskopi och diagnosen ställdes peroperativt med fryssnitt. I två fall gjordes en mellannålsbiopsi och diagnosen ställdes via PAD. I ett av dessa fall krävdes upprepad biopsi för diagnos, då den initiala biopsin bedömdes som enbart nekrotisk. Eftergranskning visade dock att typiska membran fanns redan i den första biopsin. Inte i något av fallen förelåg misstanke om E multilocularis-infektion före operation eller biopsi.
I två fall noterades vid eftergranskning av äldre undersökningar att det funnits en leverförändring på platsen för aktuell E multilocularis-infektion vid tidigare DT-undersökningar, 3 respektive 7 år före diagnos.
Radiologernas utlåtanden om levertumörerna inkluderade ospecificerad malignitet, intrahepatiskt kolangiokarcinom, fibrolamellär hepatocellulär cancer, fibrotiserande jättehemangiom, angiosarkom och cystadenokarcinom. I enbart två fall innehöll utlåtandet att förändringen också skulle kunna vara förenlig med E multilocularis-infektion, vilket dock inte ledde till någon vidare specifik diagnostik som serologisk undersökning före operation eller biopsi.
Samtliga patienter hade positiv serologi för E multilocularis.
I fem fall bekräftades diagnosen genom att E multilocularis-DNA kunde påvisas med PCR-teknik. I fem av fallen utfördes analysen på formalinpreserverad vävnad, i det sjätte på färsk vävnad. I ett av de formalinfixerade proven förelåg inhibition av PCR, det vill säga att det inte var laboratorietekniskt möjligt att få ett resultat.
En patient avled i orelaterad sjukdom innan någon behandling av E multilocularis-infektionen påbörjats. Fyra patienter har genomgått kurativt syftande kirurgiska ingrepp med efterföljande albendazolbehandling. En patient bedömdes inoperabel och behandlas med albendazol. Vid hittills längsta uppföljning på dryga två år har inget recidiv påvisats hos de kirurgiskt behandlade.
Diskussion
Infektion med E multilocularis har varit en ytterst sällsynt diagnos i Sverige, varför kunskapen om sjukdomen kan tänkas vara låg. Detta belyses av ovan rapporterade fall. I de sex svenska fallen har diagnosen ställts först efter kirurgi eller biopsi utan föregående klinisk misstanke. Radiologiskt har E multilocularis endast uppmärksammats differentialdiagnostiskt vid två tillfällen. Upprepade biopsier har krävts vid ett tillfälle. Hos två patienter sågs leverförändring förenlig med E multilocularis-infektion 3–7 år före diagnos utan åtgärd. Det ska betonas att diagnosen är svår även i endemiska länder med upp till en tredjedel av patienterna initialt felbehandlade [22]. Vaksamheten på diagnosen bör dock höjas då vi även fortsättningsvis måste räkna med fall i Sverige, både till följd av smitta under utlandsvistelse och för att inhemsk smitta inte längre säkert kan uteslutas.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
(uppdaterad 2023-02-15)