Susacs syndrom är en ovanlig mikroangiopati som ger symtom från hjärnparenkymet (encefalopati, fokala neurologiska bortfall och huvudvärk), innerörat (hörselnedsättning) och näthinnan (grenartärocklusioner med flimmerepisoder och synbortfall).
Den kliniska triaden (förvirring och syn- och hörselnedsättning) ses hos endast 13 procent av patienterna vid sjukdomsdebuten, vilket gör tidig diagnos till en utmaning.
Korrekt och tidig immunsuppressiv behandling resulterar i signifikant klinisk och radiologisk förbättring och kan förebygga bestående handikapp.
Susacs syndrom kräver ett tvärvetenskapligt samarbete mellan neurologer, neuroradiologer, ögonläkare och otorinolaryngologer.
Susacs syndrom är en sällsynt neurologisk sjukdom som kännetecknas av den kliniska triaden encefalopati, retinal grenartärocklusion och hörselnedsättning. Sjukdomen är förmodligen en autoimmunmedierad mikroangiopati som drabbar hjärnans, näthinnans och innerörats mikrovaskulatur (prekapillära arterioler) [1]. Syndromet beskrevs först av John O Susac 1979 hos två unga kvinnor med den klassiska kliniska triaden [2]. Sjukdomen har också haft andra benämningar, t ex SICRET (small infarcts of cochlear, retinal, and encephalic tissue) [3].
Syndromet är sannolikt underdiagnostiserat på grund av varierande klinisk presentation, och det är en stor diagnostisk utmaning, inte minst eftersom triaden förvirring och syn- och hörselnedsättning ses hos endast 13 procent av patienterna vid sjukdomsdebuten [4]. Fördröjd eller felaktig diagnos är mycket vanlig vid Susacs syndrom och kan leda till att effektiv behandling sätts in för sent [4, 5]. Multipel skleros (MS) är den vanligaste feldiagnosen, och MS-bromsmediciner kan möjligtvis leda till försämring av sjukdomen [4].
Trots att kontrollerade behandlingsstudier saknas anser experter på området att tidig immunsuppressiv behandling kan resultera i signifikant klinisk och radiologisk förbättring och kan vara avgörande för att undvika permanent syn- och hörselnedsättning och kognitiva besvär [6]. Susacs syndrom kräver ett tvärvetenskapligt samarbete mellan neurologer, neuroradiologer, ögonläkare och otorinolaryngologer som känner till sjukdomen.
Här presenterar vi tre fall, som avspeglar sjukdomens mångfasetterade natur och betydelsen av tidigt insatt behandling.
Fallbeskrivningar
Fall 1. En tidigare frisk 33-årig man sökte neurologisk akutmottagning på grund av att han sedan 1 månad hade haft upprepade monookulära flimmerepisoder, 10–30 minuter åt gången på både höger och vänster öga, och även suddig syn perifert efter flimmerepisoderna. Symtomen hade tidigare bedömts som migrän av ögonläkare. Patienten fick därefter tillkomst av yrsel, och några månader senare tappade han också hörseln på höger öra.
Kortison sattes in enligt schema via primärvården på grund av misstanke om plötslig dövhet (sudden deafness). Trots kortisonbehandlingen försämrades hörseln även på vänster öra. Hörselprov visade sensorineural hörselnedsättning i basen på båda sidor ner runt 50–60 dB. Lumbalpunktion visade 6 monocyter/mm3 och albuminstegring 349 mg/l (referensvärde 80–280 mg/l) men inga oligoklonala band. Vid ett tillfälle drabbades patienten av expressiv dysfasi under 30 minuter. MR-undersökning av hjärnan visade »punched-out«-lesioner i corpus callosum och spridda små infarkter bilateralt kortikalt och subkortikalt samt i djupa vitsubstansen (Figur 1).
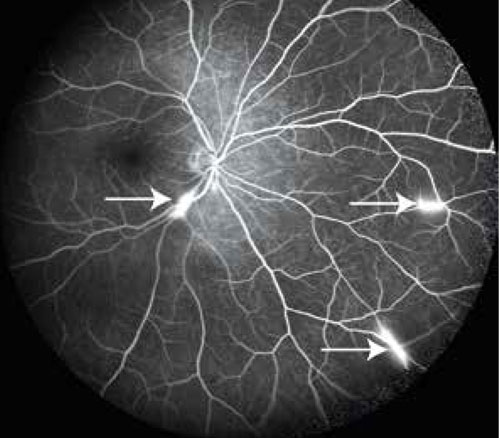
Dessa fynd tillsammans med anamnes ingav misstanke om Susacs syndrom, vilket ledde till akut remiss till ögonkonsult för bedömning. Med fluoresceinangiografi sågs flera fokala förändringar tydande på vaskulopati i båda ögonens näthinnor (Figur 2). Kognitiv bedömning påvisade nedsatt minne, uppmärksamhet och exekutiv funktion.
Patienten genomgick förnyad lumbalpunktion som visade att cellantalet hade gått upp till 50 monocyter/mm3 och albuminvärdet var förhöjt till 770 mg/l. ANA (antinukleära antikroppar), antikardiolipin, kryoglobulin och lupusantikoagulans var alla negativa. Antikroppar mot endotelceller var också negativa.
Patienten behandlades med hög dos kortison, 1 g per dag, i 3 dagar och pulsar med cyklofosfamid (10 mg/kg varannan vecka) i 3 månader och prednisolon 80 mg med nedtrappning.
Några månader senare visade MR att ett 20-tal förändringar hade försvunnit och inte lämnat någon rest. Kort därefter drabbades han ånyo av hörselförsämring, och trots nya hörapparater kunde patienten inte längre prata i telefon. Samtidigt var han ibland förvirrad och hade fått nedsatt arbetsminne.
Nu visade hörselprov uttalad sensorineural hörselnedsättning i bas- och mellanregistren bilateralt. Det var framför allt hörseltröskeln på det vänstra örat som hade sjunkit mellan 30 och 45 dB i diskanten. På grund av detta behandlades han med intravenöst immunglobulin 0,4 g/kg per dag i 5 dagar och fick förlängd behandling med cyklofosfamid (15 mg/kg var fjärde vecka). Efter behandling med cyklofosfamid i totalt 6 månader behandlades han med en kombination av rituximab 500 mg var sjätte vecka och intravenöst immunglobulin 2 g/kg totalt varje månad plus nedtrappning av peroralt kortison.
24 månader senare hade de kognitiva symtomen mestadels försvunnit, och fluoresceinangiografi visade nästan full regress av kärlpatologin. Hörseln hade blivit endast marginellt bättre. Upprepade MR-kontroller visade inte några nya förändringar, förutom en viss atrofi av corpus callosum.
Genom hela sjukdomsförloppet mättes NFL (neurofilament light) i cerebrospinalvätska och gick från ett mycket högt värde på 38 320 ng/l (referensvärde <560 ng/l) till att nästan normaliseras.
Fall 2. En tidigare frisk 25-årig kvinna sökte medicinsk akutmottagning på ett annat länssjukhus efter att under en vecka haft kontinuerlig rotatorisk yrsel och lockkänsla för höger öra. Samtidigt hade hon haft svårigheter att gå och stå, gick bredbent och ostadigt. MR-hjärna på sjukhuset ansågs visa en bild typisk för multipel skleros. Patienten behandlades med höga doser kortison i 3 dagar och blev utskriven till hemmet.
På grund av tilltagande förvirring och apraxi tog hon kort därefter åter kontakt. En likvoranalys visade 9 monocyter/mm3 och mycket förhöjt albuminvärde på 2,07 g/l (referensvärde 80–280 mg/l). Hon genomgick en ny MR-undersökning, som visade radierande vitsubstansförändringar kring corpus callosum, men också spridda vitsubstansförändringar samt leptomeningeal uppladdning, som inte ansågs typisk för multipel skleros. Förändringarna ingav snarare misstanke om vaskulit eller annan neuroinflammatorisk sjukdom.
Patienten flyttades därefter till neurologkliniken vid Karolinska universitetssjukhuset i Stockholm. Vid neurologisk undersökning var hon förvirrad, svag i båda benen, ostadig med bredspårig gång, hade dubbelseende vid blick åt höger, och tonaudiometri visade bashörselnedsättning höger och vänster av sensorineural karaktär. Patienten behandlades återigen med höga doser kortison.
Vaskulitprov och komplementfaktorer utföll med normala värden. En uppföljande MR-undersökning visade minskad leptomeningeal kontrastuppladdning och i övrigt oförändrad utbredning av signalförändringarna i corpus callosum och den vita substansen (Figur 3). Arbetsdiagnosen blev neurosarkoidos. DT-torax visade dock inga parenkymförändringar eller förstorade lymfknutor.
Behandling initierades nu med metotrexat och infliximab. En ny lumbalpunktion visade 6 monocyter/mm3, och prov för ACE, antikroppar mot borrelia, tuberkulos, cytologi, flödescytometri och neuronala antikroppar i serum och cerebrospinalvätska visade normala värden. Patienten hade inga oligoklonala band eller förhöjt IgG-index. DT-angiografi visade inga stenoser eller andra kärlförändringar som skulle indikera vaskulit.
Vid en mer noggrann granskning av MR-bilderna väckte förändringarna i corpus callosum misstanke om Susacs syndrom. Vid oftalmologisk konsultation sågs bilaterala ischemiska retinala förändringar, och med fluoresceinangiografi observerades ställvisa bortfall i den retinala arteriella cirkulationen.
Trots behandling med prednisolon 60 mg, acetylsalicylsyra, 5 plasmafereser och rituximab (1 000 mg)försämrades hon kliniskt, blev mer apraktisk och förvirrad med mer talsvårigheter och sämre minne. MR-hjärna visade progress med nya signalförändringar. Vid Moca-test (Montreal cognitive assessment) fick hon totalt 11 poäng (av 30 möjliga). Ytterligare plasmaferes, 5 omgångar, gav nu effekt. Efter detta behandlades hon med cyklofosfamid 500 mg varannan vecka i 3 månader.
Några månader senare var patienten mycket bättre trots vissa minnesproblem och lätt balanspåverkan. Kortison trappades ut mycket långsamt, fluoresceinangiografi visade inte några nya ocklusioner, MR visade inga tecken till ny aktivitet och de tidigare uppladdningarna hade försvunnit. 5 år senare var patienten återställd.
Fall 3. En tidigare frisk, 29-årig kvinna insjuknade med flimmerepisoder framför båda ögonen, domningar i tunga, läppar och höger arm. Initialt bedömdes det hela som migrän av ögonläkare och neurolog, och patienten fick pröva behandling med triptaner, som inte hjälpte. Hon hade under samma tidsperiod haft episoder av yrsel, illamående, kräkningar och ihållande huvudvärk. Hon kunde inte arbeta på grund av minnesluckor. DT och MR av hjärnan bedömdes först som normala.
Hon blev inlagd på en neurologisk avdelning, och vid eftergranskning av MR-bilderna sågs förändringar i corpus callosum förenliga med Susacs syndrom. En fluoresceinangiografi visade grenartärocklusion i vänster näthinna och lumbalpunktion 9 monocyter/mm3 och lätt förhöjt albuminvärde (289 mg/l). Hörselprov visade nedsättning av basfrekvenser på höger öra.
Patienten behandlades med höga doser kortison och intravenöst immunglobulin. Trots det tillkom nya förändringar på MR i corpus callosum och den vita substansen. Hon erhöll därför 6 infusioner (1 000 mg pulser) av cyklofosfamid, varpå symtomen gick i regress. Under flera år behandlades hon med metotrexat och låga doser prednisolon.
9 år efter insjuknandet var patienten fullt arbetsför, mådde bra och tog endast acetylsalicylsyra. Hon hade kvar ett mindre synfältsbortfall för höger öga. Uppföljande MR-undersökningar har inte visat några nytillkomna förändringar, men en viss atrofi i corpus callosum har noterats.
Epidemiologi
Susacs syndrom är mycket sällsynt. Syndromet anses vara trefaldigt vanligare hos kvinnor än hos män och drabbar främst individer i åldrarna 20–40 år, men patienter mellan 7 och 70 år har rapporterats [7]. Nyligen kom en studie från Österrike, där Susacs syndrom uppskattades ha en prevalens på 0,14 individer per 100 000 invånare [8]. Studien baserades på enkäter till neurologkliniker i Österrike. Sannolikt är prevalensen därför något högre.
Patogenes
Susacs syndrom anses vara en autoimmun mikroangiopati, där mikrovaskulära ocklusioner antas vara medierade av en autoimmun respons (anti-endotelcellsantikropp) mot ett ännu okänt antigen. Detta orsakar mikrovaskulära skador och små infarkter i hjärnan, koklean och näthinnan. Anti-endotelcellsantikroppar kan detekteras hos vissa patienter (25 procent), men är inte specifika för syndromet eftersom de även har identifierats vid andra autoimmuna sjukdomar [1, 4].
På hjärnbiopsier ser man inflammation runt de små kärlen (perivaskulärt) och mikroinfarkter, men nekros finns inte i kärlväggen, vilket talar för att det rör sig om vaskulopati (mikroangiopati) snarare än vaskulit. Nyare patologiska studier har visat endotelförändringar som passar med anti-endotelcellsantikroppar [2, 7]. Till stöd för en antikroppsmedierad etiologi för syndromet färgas >50 procent av kapillärerna i hjärnbiopsiprov starkt för komplementproteinet C4d2 [2, 7]. Biopsier bekräftar också mikrovaskulär endoteliopati i näthinnan och innerörat [3].
Den histopatologiska och elektronmikroskopiska undersökningen visar att immunpatogenesen vid Susacs syndrom till stor del liknar juvenil dermatomyosit, som är en autoimmun endoteliopati som påverkar mikrovaskulaturen i muskel, hud och mag–tarmkanal [5].
Kliniska manifestationer
Encefalopati. Huvudvärk är det vanligaste prodromala symtomet och kan förekomma flera månader före utvecklingen av encefalopati. Den är ofta migränliknande i sin karaktär. Förutom förvirring kännetecknas encefalopatin av psykiska störningar och kognitiva symtom med minnesförlust, som med tiden kan utvecklas till allvarlig kognitiv funktionsnedsättning. Patienten kan samtidigt ha multifokala neurologiska symtom som ostadighet, dysartri, yrsel, kranialnervspåverkan, överaktiv urinblåsa och epileptiska anfall [1].
Retinalt engagemang. Vid Susacs syndrom visar den oftalmologiska undersökningen nästan alltid tecken på arteriell kärlsjukdom och status efter ocklusion av retinala grenartärer [7]. Fynden är ofta bilaterala, multipla och spridda i retina och kan orsaka varierande grad av fläckvisa synbortfall och flimrande retningssymtom för patienten. Den oftalmologiska undersökningen, som i regel inkluderar fluoresceinangiografi, är oerhört viktig för att fastställa diagnosen. Det gäller även patienter som inte rapporterar några synsymtom. I ögonbottnen kan man förutom bomullsexsudat och bleka områden med retinalt ödem upptäcka inskidning av kärlen och gulvita utfällningar, s k Gass-plack [2, 9].
Vid undersökning med fluoresceinangiografi kan man t ex se områden med upphävd retinal blodcirkulation, hyperfluorescens i artärväggarna och läckage av fluorescein (Figur 2). Kärlläckaget är ett känsligt tecken på aktiv sjukdom även när patienten är asymtomatisk. Det kan vara svårt att se kärlläckage vid oftalmoskopi eller på vanliga retinala foton, och då är fluoresceinangiografi till stor hjälp. Kärlläckage på fluoresceinangiografi skulle kunna betraktas som en biomarkör för sjukdomsaktivitet. Även optisk koherenstomografi (OCT) och OCT-angiografiundersökning av näthinnan kan ge värdefull information.
Innerörat. Ocklusioner i arterioler i koklea, speciellt vid apex där sinnesceller för basfrekvenser är lokaliserade, inträffar vid Susacs syndrom. Tonaudiometri avslöjar vanligtvis bilateral sensorineural hörselnedsättning, som är asymmetrisk och anses vara en följd av mikroinfarkter i den apikala koklean. Hörselnedsättningen involverar i huvudsak låga och mittenfrekvenser, och dålig taldiskriminering är vanlig. Vertigo och tinnitus följer ofta hörselnedsättningen. Videonystagmografi kan visa nedsatt kaloriskt svar i det drabbade örat [7].
Radiologi
Susacs syndrom ger oftast utbredda vitsubstansförändringar men kan i stort sett drabba hela hjärnan, såväl vit och grå substans som hjärnhinnorna [1, 4]. Under den encefalopatiska fasen är corpus callosum nästan alltid påverkad, och MR visar ett karakteristiskt mönster av små till stora runda vitsubstansförändringar som ser ut som snöbollar och linjära defekter (»spokes«) som drabbar de centrala fibrerna i corpus callosum.
Sagitella T1-viktade sekvenser visar ofta förändringar som ser ut som »punched-out«-lesioner i corpus callosum, dvs väl begränsad atrofi som påminner om »svarta hål« vid multipel skleros. Axial T1-viktad MR med gadolinium kan visa leptomeningeal uppladdning, speciellt i lillhjärnan, vilket betraktas som ett mycket typiskt fynd [5, 7].
Susacs syndrom kan skiljas från demyeliniserande sjukdom eftersom syndromet involverar mitten av corpus callosum och i motsats till bilden vid multipel skleros försvinner en stor del av förändringarna. En del av de akuta förändringarna kan dock med tiden utvecklas till hål och atrofi av corpus callosum. Cerebral angiografi visar vanligen normala fynd eftersom de drabbade arteriolerna är för små.
Laboratoriemarkörer
Cerebrospinalvätskan visar oftast lymfocytisk pleocytos (mediancelltal 12 celler/mm3) och förhöjda proteinnivåer [4]. Cirka 5–15 procent av patienterna kan ha oligoklonala band eller förhöjt IgG-index, vilket kan leda till misstolkningen om att det rör sig om multipel skleros. Enstaka patienter har förhöjda nivåer av ANA och antifosfolipidantikroppar. Även förhöjda nivåer av faktor VIII- och von Willebrand-faktor kan ses, vilket kan bero på endotelial störning [2].
Särskilda serologiska markörer för syndromet finns inte, men anti-endotelcellsantikroppar förekommer i hög titer hos 25 procent av patienterna med Susacs syndrom, vilket är betydligt oftare än hos friska kontroller [4].
Diagnos
Diagnosen baseras främst på den kliniska presentationen. Tecken till retinal grenartärocklusion och de karakteristiska fynden på MR och audiometri hjälper till att skilja Susacs syndrom från andra inflammatoriska sjukdomar som multipel skleros och ADEM (akut disseminerad encefalomyelit), CNS-vaskulit, neurosarkoidos och Cogans syndrom [10]. Andra differentialdiagnoser som kan beaktas är ischemisk stroke, CADASIL (cerebral autosomalt dominant arteriopati med subkortikal infarkt och leukoencefalopati) och CNS-lymfom. Föreslagna diagnoskriterier för syndromet visas i Fakta 1[11].
Behandling
Inga randomiserade kontrollerade behandlingsstudier finns. Behandlingen baseras därför på klinisk erfarenhet, som stöds av individuella rapporter och fallserier. Nyligen har förslag på behandlingsrekommendationer tagits fram [6].
Samstämmighet föreligger om att höga doser kortikosteroider bör vara förstahandsbehandling och att tidig immunsuppressiv behandling kan förbättra prognosen markant. Det är emellertid fortfarande oklart hur aktiv immunsuppressiv medicinering som krävs, dvs vilka läkemedel och hur länge [5]. Vanligtvis har intravenöst immunglobulin, plasmaferes, azatioprin, metotrexat, cyklofosfamid och rituximab använts i olika kombinationer. Val av preparat och dos bör anpassas efter sjukdomsförlopp och sjukdomens aktivitetsgrad (vi hänvisar till nyligen publicerade förslag på behandlingsrekommendationer [6]).
En retrospektiv studie har visat på förbättring eller stabilisering hos vissa patienter som behandlats med intravenöst immunglobulin eller plasmaferes [12]. Vid nya skov eller försämringar är det nödvändigt att återinsätta eller öka den immunsuppressiva behandlingen för att förebygga funktionshinder [5]. På grund av mikroinfarkter rekommenderas trombocythämmande medicinering. Intratympanisk injektion av dexametason i den akuta fasen av hörselnedsättning och tinnitus kan ge övergående fördel vad gäller risk för dövhet. Hos patienter med svår bestående hörselnedsättning kan kokleaimplantat vara ett alternativ [13].
Sjukdomsförlopp och prognos
Det finns förslag om att dela upp Susacs syndrom i tre huvudsakliga kliniska förlopp [4, 5]:
- monocykliskt
- polycykliskt
- kroniskt.
En aktiv period som varar <2 år skiljer det monocykliska förloppet från de två andra. Cirka 54 procent av patienterna har monocyklisk sjukdom, som ofta omfattar skov och fluktuationer men begränsas till ca 2 år och inte återkommer. Runt 42 procent har polycyklisk sjukdom med återfall som fortsätter efter en 2-årsperiod. Endast 4 procent utvecklar kronisk sjukdom [4].
Under behandlingen måste läkaren ständigt vara beredd på att sjukdomen kan förvärras spontant eller som följd av minskad medicinering. Hos den enskilde patienten kan förloppet och prognosen vara svår att förutsäga. Med tidigt insatt adekvat behandling kan återhämtningen vara nästan fullständig trots signifikant encefalopati och syn- och hörselnedsättning. Försenad diagnos kan däremot leda till permanenta skador. Ungefär 50 procent av patienterna drabbas av permanent kognitiv nedsättning, och kvarstående syn- och hörselproblem är inte ovanliga [4, 5].
Med tidig och kraftfull behandling och kännedom om tillståndet bör man kunna minska och i bästa fall undvika permanenta neurologiska bortfallssymtom.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Diagnostiska kriterier [11]
Definitiv sjukdom – patienter med otvetydigt kliniskt och/eller parakliniskt engagemang från alla de tre huvudorganen
- hjärnparenkym: encefalopati, fokala neurologiska bortfall och huvudvärk
- inneröra: hörselnedsättning, yrsel, tinnitus och balanssvårigheter
- näthinna: grenartärocklusioner med flimmerepisoder och synbortfall.
Sannolik sjukdom – patienter med otvetydigt klinisk och/eller paraklinisk inblandning av två av de tre huvudorganen.




![Figur 1. Fall 1. A) Axial diffusionsviktad MR-bild visar multipla små infarkter (pilar). B) Sagittal MR-bild (T1-viktad volymsekvens med gadolinium) visar en lågsignalerande förändring (»punched-out«-lesion) i corpus callosum (pil). C) MR-bild (axial FLAIR [fluid attenuated inversion recovery]-sekvens) visar »punched-out«-lesioner i mitten av corpus callosum (pilar). D) MR-bild (sagittal FLAIR-sekvens) visar linjära defekter (»spokes«) i de centrala fibrerna i corpus callosum (pilar).](https://lakartidningen.se/wp-content/uploads/EditorialFiles/SS/%5bFSSS%5d/2019-093_1_webb.jpg)
![Figur 3. Fall 2. A) MR-bild (sagittal FLAIR-sekvens) visar karakteristiskt mönster med två stora runda, »snöbollslika« förändringar (pilar) i mitten av corpus callosum. B) MR-bild (axial FLAIR-sekvens) visar en förändring i mitten av corpus callosum (pil) och multipla vitsubstansförändringar, som först väckte misstanke om multipel skleros. C) Axial MR-bild (ADC [apparent diffusion coefficient]-karta) visar minskad diffusion i den stora förändringen längst bak i corpus callosum (pil). D) Axial MR-bild (T1-viktad volymsekvens med gadolinium) visar spridd leptomeningeal kontrastuppladdning (pilar).](https://lakartidningen.se/wp-content/uploads/EditorialFiles/SS/%5bFSSS%5d/2019-093_3_webb.jpg)

















