APTT bör endast användas som screeningtest vid utredning av ökad blödningsbenägenhet.
APTT bör inte används rutinmässigt preoperativt som screeningtest för ökad blödningsrisk.
Normal APTT utesluter inte koagulationsrubbning.
Förlängd APTT är inte alltid relaterad till blödningsrisk.
Perioperativ blödning påverkar såväl patientens sjukhusvistelse/behandling som morbiditet och mortalitet. Blödningen bestäms delvis av patientens koagulationsstatus, och koagulopati är en viktig riskfaktor för blödning. Andra faktorer inkluderar typ av operation, var operationen utförs, grad av vävnadsskada och tidigare operation på samma ställe [1]. Blödningsrisken bedöms preoperativt genom blödningsanamnes, inkluderande familjehistoria och patientens tidigare blödningsmönster i samband med ingrepp, samt fysisk undersökning. Preoperativt används även rutinkoagulationstest vid denna bedömning i varierande grad.
Rutinkoagulationstest har använts preoperativt i många år i tron att de kan identifiera patienter som har medfödd eller förvärvad blödningsrubbning och att testen kan förutsäga perioperativ blödningsrisk så att behandling kan sättas in och blödning förebyggas [2]. Testen ordineras vanligtvis av anestesiologer eller kirurger i samband med en »preoperativ bedömning«. Inte sällan beställs en panel av laboratorieanalyser inklusive APTT (aktiverad partiell tromboplastintid), PK(INR) (protrombinkomplex, internationell normaliserad kvot) och TPK (trombocyter, partikelkoncentration). PK(INR):s förmåga att upptäcka ärftliga koagulationsdefekter är minimal, eftersom PK(INR) endast undersöker det externa systemet [3]. Faktor VII-brist är den enda medfödda blödningsrubbningen som kännetecknas av isolerat förhöjt PK(INR) [1]. APTT, å andra sidan, påverkas av det interna systemet och är därför lämpligare för att upptäcka en ärftlig sjukdom, eftersom de flesta av dessa tillstånd är abnormiteter i det interna systemet. Denna artikel fokuserar på APTT som screeningtest inför operation. Det är troligen en stor andel APTT-test som görs preoperativt. Genomgång av beställarmönster på universitetssjukhusen i Linköping, Göteborg och Stockholm visar att 15–50 procent av alla APTT-test på våra sjukhus beställs från kirurgiska specialiteter. Däremot är dessa tests värde för att förutsäga blödning vid kirurgi inte väldokumenterat, trots omfattande användning.
Vad är APTT och PK(INR)?
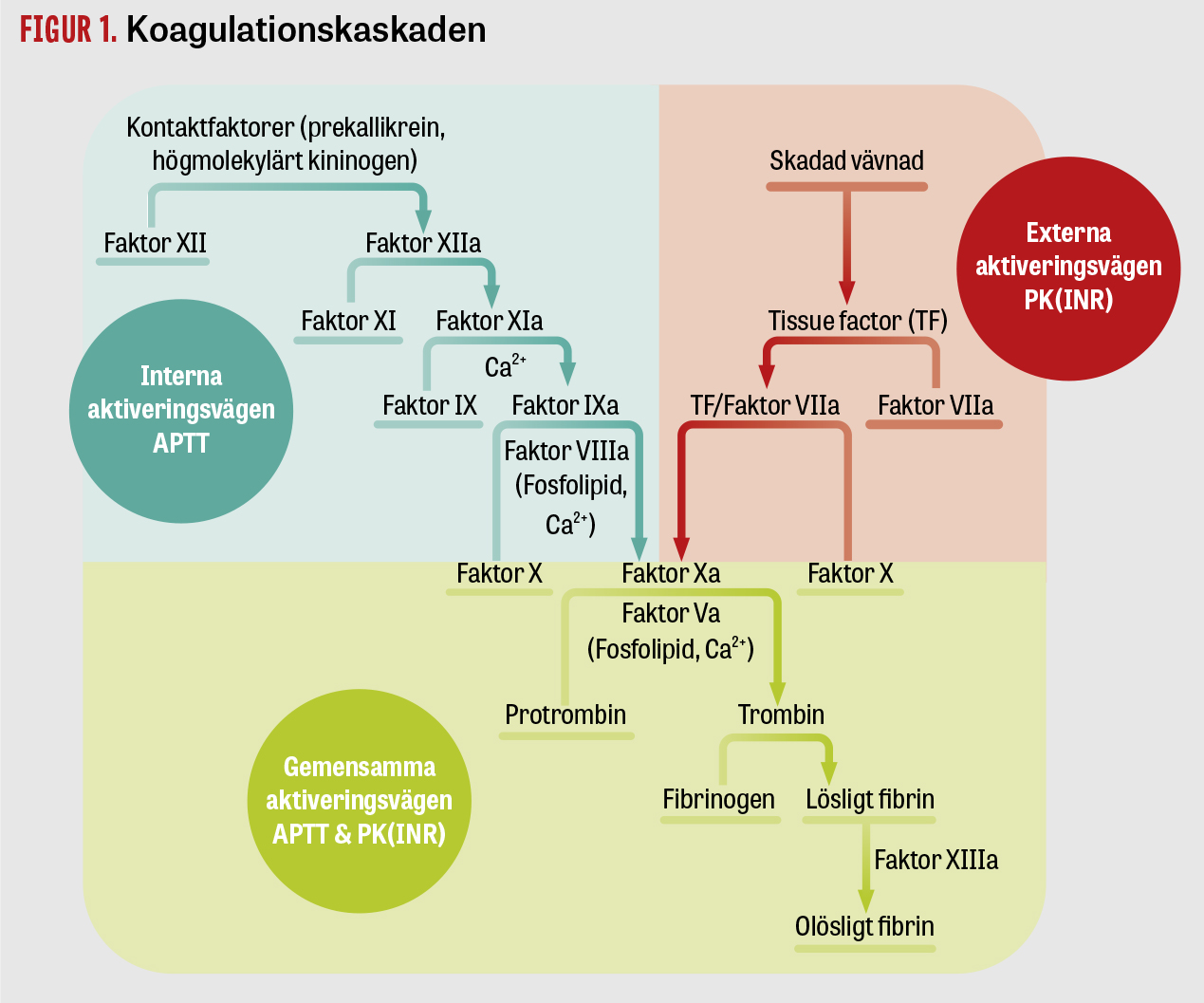
Plasmakoagulation utgörs av en serie proenzymaktiveringar som kulminerar i aktiveringen av protrombin till trombin, som i sin tur klyver och omvandlar fibrinogen till ett fibrinkoagel. Processen delas traditionellt in i det interna och det externa systemet. De två systemen möts i en gemensam väg som involverar aktivering av koagulationsfaktorerna IX, X och protrombin och bildar fibrin (Figur 1). I APTT-analysen används ett reagens som inkluderar kontaktaktivator, fosfolipid och kalcium, och det ger en standardiserad aktivering av det interna systemet och den gemensamma vägen, varefter tiden till koagulation mäts [4]. Beroende på olikheter i typ och koncentrationer av aktivator och fosfolipider är APTT starkt beroende av val av reagens och till viss del också val av instrument. Mot denna bakgrund är det viktigt att informera om referensintervall och beslutsgränser på det lokala sjukhuset. Totalt är det 10 olika koagulationsfaktorer i plasma som påverkar APTT (Figur 1), och en defekt eller avsaknad av någon av dessa faktorer kan leda till förlängd APTT. Förkortad APTT förekommer vid stress och fysisk aktivitet, eller sekundärt till inflammation med förhöjda nivåer av FVIII och fibrinogen. En onormalt kort APTT kan också orsakas av en in vitro-aktivering i provröret i samband med svår eller felaktig provtagning.
Analysen PK(INR), som används på svenska sjukhuslaboratorier, utgörs av den så kallade Owren-metoden och mäter faktor VII, X och protrombin, vilka alla är vitamin K-beroende faktorer som syntetiseras i levern. Metoden är standardiserad enligt nationella riktlinjer och svaret ges med INR (international normalized ratio). Analysen används främst för monitorering av antikoagulerande behandling med vitamin K-antagonister, i Sverige nästan bara warfarin, och också som screeningtest av leverfunktionen och vid utredning av blödningsbenägenhet [4].
Litteraturgranskning
Kliniska studier
Flera studier visar att rutintest med APTT före allmänkirurgiska ingrepp har litet värde. En stor retrospektiv studie av allmänkirurgiska ingrepp inkluderade cirka 1 miljon preoperativa patienter och visade att 23 procent av patienterna hade genomgått analys med APTT-test före operation och att 99,9 procent av denna testning var onödig [5]. En annan observationsstudie visade att APTT har hög specificitet (99 procent) men låg sensitivitet (5,9 procent) för att upptäckta koagulationsabnormiteter, till exempel lindrig faktorbrist, von Willebrands sjukdom eller trombocytfunktionsrubbningar [6]. En nyligen gjord studie av spanska anestesiologer visade att ytterligare undersökningar av avvikande APTT och PK som upptäcktes preoperativt inte var till någon nytta när det gäller blödningskomplikationer och att de var förknippade med en betydande preoperativ försening och ökade vårdkostnader, och därför rekommenderas selektiv preoperativ koagulationstestning baserad på blödningshistoria [7]. Inte heller i en mer selekterad population, med ökad blödningstendens och/eller familjehistoria av blödning, har APTT visat sig ha någon större träffsäkerhet. Hayward et al visade att APTT och PK(INR) hade låg sensitivitet, 2,1 procent respektive 1,0 procent för kliniskt signifikanta blödningsrubbningar [8], bland patienter som hänvisats till hematologer för bedömning av blödningsstatus, det vill säga populationen med hög »pretest probability« (sannolikhet före test).
Även vid operationer med hög blödningsrisk har screening med APTT begränsat värde. Tonsillektomi är en utmärkt modell för kirurgiskt ingrepp förknippat med hög blödningsrisk, där man kan följa upp och monitorera perioperativ blödningsrisk. Ingreppet är associerat med ökad blödningsrisk på grund av hög vävnadsvaskularitet [1]. Sarny et al analyserade 3 041 vuxna patienter och visade att ett positivt rutinkoagulationstest inklusive APTT, PK och TPK inte var signifikant associerat med en ökad blödningsrisk jämfört med ett negativt testresultat [9]. En studie med pediatriska patienter upptäckte att APTT hade en sensitivitet på 16,6 procent och en specificitet på 97,8 procent för detektion av blödningsrisk med ett positivt prediktivt värde på 50 procent och ett negativt prediktivt värde på 93,6 procent [3].
Vid neurokirurgiska ingrepp är perioperativ blödningsrisk kritiskt viktig att bedöma. Även små problem med intraoperativ hemostas eller små postoperativa blödningar kan vara katastrofala och ha skadliga effekter på patienternas återhämtning [10, 11]. Harley et al genomförde en retrospektiv analys på 1 143 patienter som genomgick elektiva neurokirurgiska operationer. Endast 6 patienter hade oväntade störningar i sin koagulationsstatus. Alla de 6 fallen hade isolerat förlängd APTT. Ingen erhöll preoperativ korrigering av koagulopati och ingen hade blödningskomplikationer eller avled [12].
Få kliniska studier hävdar att preoperativ screening med APTT är nödvändig. Av dessa uppvisar 1 studie samband mellan förlängning av APTT och hög blödningsrisk. Om patienterna med hög blödningsrisk exkluderas (till exempel patienter med blödningshistoria i anamnesen), försvinner dock sambandet [13].
Översiktsartiklar
Förutom kliniska studier har flera översiktsartiklar publicerats som beskriver värdet av preoperativ screening med rutinkoagulationstest inklusive APTT under de senaste 15 åren. En övervägande majoritet av översiktsartiklarna rekommenderar inte att APTT används rutinmässigt för att predicera risk för perioperativ blödning hos icke-selekterade patienter före operationer eller andra invasiva ingrepp [1, 2, 10, 11, 14-20].
Diskussion
Endast vid utredning av ökad blödningsbenägenhet
APTT och PK(INR) bör användas som screeningtest endast vid utredning av ökad blödningsbenägenhet.
APTT och PK(INR) utvecklades ursprungligen bland annat för diagnos av blödningsrubbning, till exempel hemofili (blödarsjuka). Detta skiljer sig från användning som screeningtest hos »friska« preoperativa patienter, där förekomsten av blödningsrubbning är extremt låg. Det kan leda till att användning i populationer med låg sannolikhet medför en hög grad av normala resultat. Även om ett resultat är onormalt så kan det bero på defekter som inte är relaterade till blödning, till exempel brist på faktor XII eller lupusantikoagulans [2, 5, 18]. Avvikande APTT kan också erhållas vid felaktig provtagningsteknik eller kontaminering med antikoagulantia (heparin). I en studie som granskade 100 prov med en förlängd APTT berodde 14 procent på venpunktionsartefakt [21]. Det är också viktigt att komma ihåg att APTT är relativt okänslig för lindriga defekter i koagulationssystemet, och ett vedertaget riktmärke är att APTT endast blir förlängd om en enskild koagulationsfaktor understiger 30 procent av referensvärdet [22]. Även ett korrekt utfört APTT-test kan visa på ett normalt resultat vid till exempel lindriga former av von Willebrands sjukdom (VWD) och hemofili, vilka kan vara förenade med allvarliga blödningar i samband med kirurgiska ingrepp. Som nämnts tidigare kan APTT ge varierande resultat med olika reagens [18], vilket kan resultera i skillnader i känslighet för faktorbrister [22, 23]. I Sverige används APTT på drygt 100 laboratorier, och i nuläget finns det 4 olika reagens som vart och ett har sina specifika egenskaper avseende känslighet för antikoagulativa substanser eller defekter som påverkar analysen. Det är alltså viktigt att ha god kännedom om det lokala laboratoriets APTT inklusive lokalt referensintervall. I likhet med APTT kan skillnader i PK(INR)-reagens också resultera i varierande känslighet för faktorbrister. Vissa reagens/instrumentkombinationer resulterar i förhöjt PK(INR) endast när relevant faktornivå sjunker till mindre än 0,3 kIE/l [16]. Förhöjt PK(INR) kan vara en enstaka manifestation av lupusantikoagulans [16]. Det är viktigt att känna till att det finns koagulationsfaktorer som inte påverkar vare sig APTT eller PK(INR). Det gäller till exempel faktor XIII och antiplasmin, som vid bristtillstånd kan orsaka livshotande kirurgiska blödningar; dock är prevalensen av dessa tillstånd mycket låg [16].
Internationella riktlinjer inget stöd för screening
Internationella riktlinjer ger inget stöd för rutinmässig användning av APTT som preoperativt screeningtest.
Flera internationella expertgrupperingar och organisationer har publicerat riktlinjer och rekommendationer om preoperativ laboratoriescreening. De brittiska riktlinjerna, publicerade av British Committee for Standards in Haematology, är baserade på en systematisk genomgång av den vetenskapliga litteraturen inom området. De rekommenderar inte generell användning av rutinkoagulationstest som APTT för att predicera perioperativ blödningsrisk (grad B, nivå III). Kommittén påpekade i stället att en strukturerad metod för att ta en personlig/familje-blödningsanamnes bör användas hos alla patienter (grad C, nivå IV) [16]. Andra internationella organisationer ger också rådet att inte använda koagulationstest som APTT eller PK(INR) som preoperativa screeningtest [24-27]. Nyligen publicerade American Society for Clinical Laboratory Science (ASCLS) rekommendationen att undvika rutinmässig preoperativ screening med APTT och PK(INR) på asymtomatiska patienter, till förmån för en anamnesbaserad blödningsutredning [28]. Trots samstämmiga rekommendationer, som talar emot preoperativ laboratoriescreening, visar undersökningar att APTT och PK(INR) ofta används rutinmässigt inför invasiva ingrepp av anestesiologer internationellt [29]. En exakt lägesbild av hur denna typ av preoperativa screeningtest används i Sverige saknas, men det finns ingen anledning att tro att läget är mycket annorlunda här. I dagsläget saknas också generella nationella riktlinjer avseende frågan om preoperativ screening med APTT i Sverige.
Normal APTT utesluter inte koagulationsrubbning
Normal APTT utesluter inte koagulationsrubbning, och förlängd APTT är inte alltid relaterad till blödningsrisk.
Vad är anledningen till att APTT används så frekvent preoperativt trots avsaknad av riktlinjer? Det kan bero på rädsla för dåligt kliniskt utfall, till exempel perioperativ blödning på grund av en missad koagulopati, samt rädsla för konflikt mellan läkare och patienter på grund av en komplikation till följd av koagulopati. Det kan också bero på att läkare tycker att testets kostnad är relativt låg (trots den kollektiva höga kostnaden) [12]. Ett normalt koagulationstest kan invagga i en falsk trygghet [14]. Bakomliggande orsak kan vara att man inte känner till begränsningarna med laboratorieresultaten. Normal APTT utesluter inte koagulationsrubbning: det finns kliniska tillstånd med blödningsrisk med normal APTT (Fakta 1). Förutom okänslighet för lindrig koagulationsfaktorbrist är APTT också en opålitlig metod för att påvisa pågående antikoagulantiabehandling. Trombocythämmande mediciner, till exempel acetylsalicylsyra, påverkar inte APTT. Graden av påverkan av direktverkande orala antikoagulantia (NOAK) på PK(INR) och APTT varierar mellan läkemedlen och är beroende av dos, men även av vilken kombination av APTT-reagens och instrument som respektive laboratorium använder. Vid normal APTT kan låga koncentrationer av alla NOAK-preparat föreligga. Både vid terapeutiska och höga koncentrationer av apixaban kan såväl PK(INR) som APTT vara normala [30].
Å andra sidan kan förlängd APTT vara falskt positiv och inte alls relaterad till blödningsproblem. Exempel på detta utgörs av brist på faktor XII och förekomst av antikroppar av typen lupusantikoagulans. Fakta 2 visar en lista på vanliga situationer med förlängd APTT men utan blödningsrisk. Dessa »falskt« positiva resultat orsakar potentiellt onödiga ytterligare undersökningar som kan skapa fördröjning av operation, ångest för patienter och familjer, extra kostnad och skada. Dessutom är 30–95 procent av onormala resultat från screeningtest antingen inte dokumenterade eller inte uppföljda, vilket potentiellt ökar risken för rättstvister/felbehandling [18].
Rutinmässig screening med APTT inte kostnadseffektiv
Rutinmässigt bruk av APTT betyder ofta att patienter med onormala resultat från screeningtest måste genomgå upprepade mätningar [11]. Det finns alltså en betydande ekonomisk kostnad för oselekterad koagulationsscreening [12]. Uppfattningen att koagulationsscreeningtest är billiga beror sannolikt på avsaknad av helhetsbild av kostnaden. Enligt en multicenterstudie från USA som gjordes på ett stort antal neurokirurgiska patienter (n = 11 804) kunde man spara ungefär 82 miljoner US-dollar årligen om endast de neurokirurgiska patienterna med positiv historia testades med de basala koagulationstesten (APTT, PK(INR) och trombocyter) [31].
Användning av koagulationstest som inkluderar APTT på selekterade patienter med positiv blödningshistoria (inklusive hereditet), patienter med antikoagulantiabehandling eller patienter med sjukdom som är relaterad till koagulopati, till exempel leversjukdom, kan reducera fördröjning av operationer, ökar negativt och positivt prediktivt värde [10] och är dessutom kostnadseffektiv [12].
Hur identifieras patienter med blödningsrisk?
En omfattande blödningsanamnes är avgörande för att identifiera patienter med ökad blödningsrisk. Sarny et al visar att en positiv blödningsanamnes är signifikant associerad med en högre risk för postoperativ blödning (P < 0,002). Däremot var ett positivt screeningtest (inklusive APTT, PK(INR) och TPK) inte det (P = 0,235) [9]. Hos icke-selekterade preoperativa patienter varierar incidensen av laboratorieavvikelser från 0,5 procent till 16 procent och ökar till 40 procent när patienter väljs ut baserat på positiv blödningsanamnes [25]. Screeningtest med APTT och PK(INR) bör alltså ersättas av riktad anamnes och undersökningar följt av konsultation med hematolog/koagulationsspecialist om anamnesen pekar på ökad blödningsrisk [12]. Blödningsanamnesen bör inkludera frågor om tidigare operation och trauma, menstruationer, graviditet och förlossning, familjehistoria och läkemedel som ökar blödningsbenägenhet, såsom NSAID. Standardiserat Bleeding assessment tool (BAT), som rekommenderas av ISTH/SSC (International Society on Haemostasis and Thrombosis/Scientific and Standardization Committee), kan med fördel användas [10].
Förutom blödningsanamnes bör en noggrann fysisk undersökning utföras och patienten utvärderas för petekier, slemhinneblödningar, ekkymoser eller slemhinneblödningar som antingen kan vara förvärvade (det vill säga läkemedelsrelaterade) eller orsakade av andra trombocytrubbningar [1]. Därefter kan riktade koagulationstest inklusive basala koagulationstest (APTT och PK(INR) med TPK) och eventuella utökade blödningsutredningar utföras under instruktion av hematolog/koagulationsspecialist.
Förutom konventionella koagulationstest finns patientnära instrument som tromboelastometri (ROTEM) och tromboelastografi (TEG). Användning av TEG/ROTEM kan sänka transfusionsbehovet vid hjärt- och leverkirurgi [32, 33]. Metoderna är dock okänsliga för flera faktorer som uppenbart kan påverka en patients risk att blöda; till exempel kan patienter med von Willebrands sjukdom och hemofili ha helt normala TEG/ROTEM-parametrar, och metoderna ger inte heller alltid utslag för behandling med warfarin, NOAK eller lågmolekylärt heparin. Normala fynd vid TEG/ROTEM-analys utesluter alltså inte att patienten är blödningsbenägen. Dessutom saknar TEG/ROTEM rikstäckande standardisering [33].
Sammanfattningsvis, baserat på tillgänglig litteratur, är användning av APTT som koagulationsscreening inte rekommenderad för att förutsäga perioperativ blödningsrisk hos patienter som inte är kritiskt sjuka, inte blöder, inte har fått behandling med antikoagulantia eller har positiv blödningsanamnes och som därmed har låg risk för blödning. Rutinkoagulationstest med APTT bör göras endast om det finns anamnestisk indikation i form av ökad blödningstendens. Man kan då också överväga remiss till koagulationsspecialist för ställningstagande till utvidgad blödningsutredning.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Normal APTT med blödningsrisk [1, 2, 14]
- von Willebrands sjukdom
- Lindrig koagulationsfaktorbrist (FVII, FVIII, FIX, FXI)
- FXIII-brist
- Trombocytfunktionsrubbning
- Hyperfibrinolys (malignitet, till exempel akut promyelocytisk leukemi, prostatacancer)
- Läkemedel (till exempel ADP-receptorantagonister, lågmolekylära hepariner, acetylsalicylsyra, warfarin, NOAK)
Fakta 2. Förlängd APTT utan blödningsrisk [1, 2, 14]
- Faktor XII-brist
- Lupusantikoagulans
- Kontaktfaktorbrist (prekallikrein, högmolekylärt kininogen)
- Preanalytisk variation
– Felaktigt venös provtagning
– Heparinkontamination
– Avvikande hematokrit (EVF)
– Interfererande ämnen (till exempel komplex av CRP och VLDL [very low density lipoprotein], höga lipider)