Andfåddhet är en subjektiv upplevelse och utgör ett ospecifikt, vanligt och potentiellt allvarligt symtom som tidigt bör utredas strukturerat tills orsaken är klarlagd, med fokus på att utesluta allvarliga differentialdiagnoser.
Ökad medvetenhet om allvarlighetsgraden av andfåddhet kan minska fördröjning till diagnos samt förbättra prognosen, inte minst vid sällsynta sjukdomar såsom PAH (pulmonell arteriell hypertension) och CTEPH (kronisk tromboembolisk pulmonell hypertension).
Remiss till/kontakt med specialistcentrum, och specifikt universitetssjukhusens centrum för pulmonell hypertension, vid misstanke om PAH eller CTEPH är av största vikt om diagnos inte kan fastställas efter adekvat initial utredning.
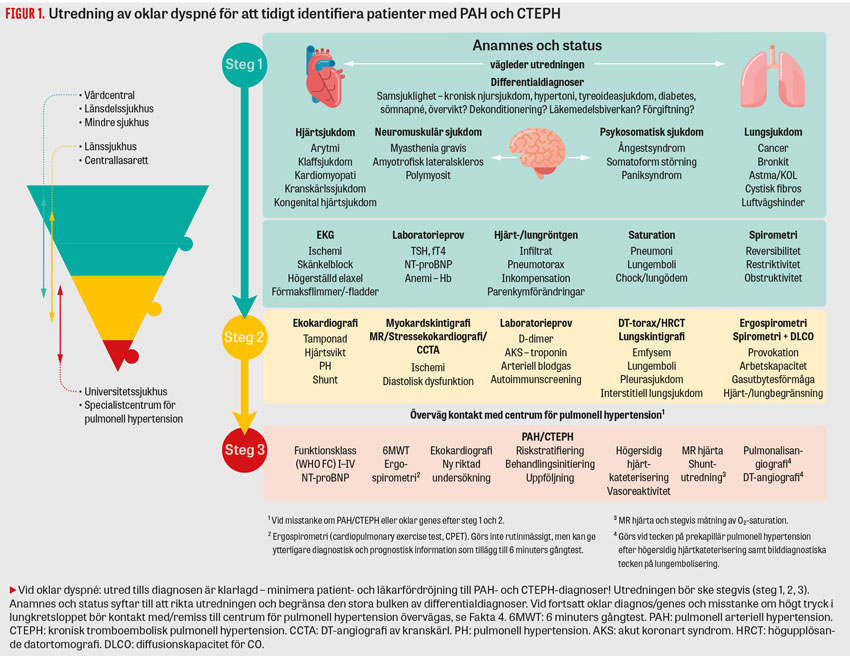
Andfåddhet eller dyspné är ett ospecifikt och vanligt men potentiellt allvarligt symtom, förknippat med ökat antal sjukhusinläggningar samt sämre funktionsnivå, livskvalitet och överlevnad [1, 2]. Åtminstone 20 procent av patienterna har flera bidragande orsaker till andfåddheten, vilket kan medföra diagnostiska utmaningar [3, 4]. Denna översikt ger insikt i patofysiologin bakom dyspné samt förslag till hur en utredning (Figur 1) kan genomföras och när specialistcentrum bör konsulteras, med fokus på PAH (pulmonell arteriell hypertension) och CTEPH (kronisk tromboembolisk pulmonell hypertension). Av största vikt är att begränsa vårdens och patientens fördröjning till diagnos.
Definition
Andfåddhet eller dyspné definieras som en subjektiv upplevelse av obehag vid andning eller medvetenhet om ökat andningsarbete vid ansträngning [5]. Denna upplevelse karakteriseras av ett samspel mellan fysiologiska, psykologiska, sociala samt miljöfaktorer, kan variera i intensitet och vara av distinkt olika kvaliteter. I syfte att reducera andfåddhetskänslan följer ofta en medveten begränsning av fysisk aktivitet, medförande en mer stillasittande livsstil och försämrad kondition [2, 3].
Mått på andfåddhet
Kvantifiering av dyspné är utmanande då upplevelsen kan skilja sig mellan patienter med samma sjukdom och liknande funktionsgrad och lungkapacitet [3]. I syfte att standardisera rapportering av dyspné – för att underlätta uppföljning, bedömning av behandlingsrespons, kommunikation mellan vårdpersonal samt forskning – har såväl enkla som mer komplexa modeller utarbetats och validerats (Fakta 1) [6-8]. Vid kliniska situationer som medför svårigheter att uppskatta graden av andfåddhet kan den åtta-parametriska Respiratory distress observation scale användas (Fakta 1) [9].
Patofysiologi
Patofysiologin vid andfåddhet är multifaktoriell, och det finns inga specifika dyspnéreceptorer eller anatomiska lokalisationer i hjärnan, vilkas stimulering eller förlust medför andningsobehag (Fakta 2) [10]. Den neuropsykiatriska teorin utgår från att dyspné uppstår vid dissociation mellan andningsbehovet och uppnådd ventilation. Uppnådd ventilation fastställs genom afferent sensorisk information från exempelvis kemoreceptorer på karotiderna (stimuleras av hög koldioxid- och låg syrenivå i arteriellt blod) och i hjärnstammen (reagerar på förändringar i pH och koldioxidnivå), mekanoreceptorer i lungparenkym, bronker och muskulatur samt interaktioner mellan psykologiska stimuli från limbiska systemet [2, 5, 11]. Indirekt evidens finns dock för ökad aktivitet i den främre insulära barken samt andra regioner kopplade till hunger, törst och smärta [2].
Differentialdiagnostik
Dyspné uppskattas föreligga hos 9–13 procent av den vuxna befolkningen, 25 procent av patienterna i öppenvården och upp till 37 procent av personer > 70 år [2]. Den inträffar oftast till följd av hjärt- och lungsjukdomar, men kan även uppträda vid neuromuskulära, endokrina, psykiska och fysiologiska tillstånd liksom intoxikationer (Figur 1, Fakta 2) [2, 12].
Hjärt- och lungsjukdomar. Hjärt- och lungsjukdomar utgör de i särklass vanligaste orsakerna till andfåddhet [13]. Hjärtsvikt uppstår när kroppens metabola behov inte kan tillfredsställas på grund av nedsatt pumpförmåga eller förhöjda fyllnadstryck [14]. Hjärtsvikt, i synnerhet med bevarad ejektionsfraktion (HFpEF), är en heterogen, oftast negligerad grupp med kvinnlig överrepresentation, där det uppskattas föreligga en underdiagnostik hos var femte patient i primärvården och en 5-årsmortalitet på 53 procent (Fakta 2) [15-17]. Ischemisk hjärtsjukdom kan uppträda med dyspné som det dominerande symtomet vid icke-ST-höjningsinfarkter hos äldre och utgör tillsammans med diabetes riskfaktorer för hjärtsvikt [18, 19]. Astma och kroniskt obstruktiv lungsjukdom (KOL) är vanliga orsaker till dyspné och utmärks av luftvägsobstruktion, kronisk inflammation och nedsatt ventilationsmekanik [2, 5]. Vid restriktiva lungparenkymatösa sjukdomar tros dyspné uppkomma till följd av ökad styvhet i lungparenkymet (sänkt compliance och ökat elastiskt återfjädringstryck), hypoxemi och försämrat gasutbyte (sänkning av diffusionskapaciteten och ökad »dead space«-ventilation) [2, 5, 56].
Vid pneumonier utgör andfåddhet det vanligaste symtomet (> 80 procent) hos äldre och uppstår, liksom vid lungembolism, till följd av försämrat gasutbyte mellan alveolarluften och lungkapillarblodet. Den övergripande mortaliteten vid pneumonier och lungembolism ligger på 10 respektive 4 procent [2, 4, 20, 21].
Biokemiska rubbningar och anemi. Salicylintoxikation, diabetesketoacidos och njursvikt medför förändringar i vätejonkoncentrationen och kan förklara andfåddheten hos dessa patienter (Fakta 2) [5]. Vid kronisk hyperkapni inträder metabol kompensation, vilket minskar förändringar i vätejonkoncentrationen och ventilationsresponsen samt känslan av dyspné [2, 5]. Nedsatt frisättning av syre till vävnaderna kan orsaka dyspné, såsom vid hemoglobinopatier och kolmonoxidförgiftning [2].
Sköldkörtelsjukdomar. Struma kan leda till direkt mekanisk obstruktion av de övre luftvägarna och orsaka lägesberoende dyspné [22]. Både hyper- och hypotyreoidism kan leda till svaghet i respiratorisk muskulatur (myopati) och dyspné (Fakta 2) [23, 24].
Neuromuskulära sjukdomar. I takt med sjukdomsprogress vid exempelvis myasthenia gravis, muskeldystrofi och amyotrofisk lateralskleros uppträder trötthet, ortopné och hypersomnolens, liksom andra neurologiska manifestationer [4, 25]. Dyspné är oftast inte den primära sökorsaken och uppträder vanligtvis sent i förloppet (Fakta 2) [26, 27].
Fysiologiska tillstånd
Under graviditeten upplever mer än hälften av alla friska kvinnor andfåddhet, som tros bero primärt på hormonella förändringar, medan de mekaniska förändringar som följer av den växande livmodern sannolikt är av mindre betydelse eftersom andfåddheten upplevs redan under första trimestern [2, 12, 28, 29]. Hos friska gravida kvinnor är andfåddheten sällan allvarlig och påverkar oftast inte dagliga aktiviteter eller den maximala aeroba arbetskapaciteten [12]. Dyspné förekommer även vid fetma och åldrande [2, 12]. Svåra bröstkorgsdeformationer såsom kyfoskolios kan också orsaka dyspné till följd av restriktiv lungvolymsfysiologi (Fakta 2) [2, 30].
Psykogena tillstånd. En överrepresentation av psykisk komorbiditet förekommer vid respiratoriska sjukdomar [31-33]. Psykiskt status, liksom förbättring av andfåddheten vid distraktion eller fysisk aktivitet, kan stärka misstanken om psykogen dyspné [4]. Psykiska sjukdomar ska betraktas som uteslutningsdiagnoser och bör sättas först efter en adekvat utförd somatisk utredning [4]. Dyspné kan orsakas och förvärras av psykogena sjukdomar (Fakta 2) [3].
Pulmonell hypertension. Pulmonell hypertension utgör ett allvarligt hälsotillstånd, som drabbar ungefär 1 procent av befolkningen globalt samt 10 procent av individer > 65 år, med påverkan på såväl sjuklighet som dödlighet [34, 35]. Pulmonell hypertension definieras enligt rådande europeiska riktlinjer som förhöjt tryck i lungkretsloppet (invasivt mätt medelpulmonalisartärtryck > 20 mm Hg i vila) och indelas i fem grupper beroende på genes och lokalisation av förändringarna i lungkärlen. Vänstersidig hjärtsjukdom utgör den vanligaste orsaken till pulmonell hypertension (grupp 2) och beror på en bakåttransmission av förhöjda vänstersidiga fyllnadstryck i hjärtat, vilket ytterligare kan kompliceras av en pulmonell vasokonstriktion samt lungkärlsremodellering [35, 48]. Pulmonell hypertension på basen av lungsjukdom och/eller hypoxemi (grupp 3) är den näst vanligaste orsaken. Behandlingen vid pulmonell hypertension i grupp 2 och 3 ska inriktas mot bakomliggande orsak, i avsaknad av direkt behandling mot komponenten för pulmonell hypertension vid dessa tillstånd. Pulmonell hypertension av oklara/multifaktoriella orsaker (grupp 5) är en ovanlig och heterogen grupp, där behandling inriktas mot bakomliggande orsak [34, 48].
Pulmonell arteriell hypertension (PAH; grupp 1) samt kronisk tromboembolisk pulmonell hypertension (CTEPH; grupp 4) är två sällsynta tillstånd, med en incidens i Sverige på ca 8 respektive 2 per miljon invånare och år samt en prevalens på ca 49 respektive 19 per miljon invånare [36]. I dag lever i Sverige drygt 800 personer med PAH eller CTEPH [36]. Dessa tillstånd, som är präglade av andfåddhet, har via moderna behandlingsstrategier i princip omvandlats från akut livshotande till mer kroniska, där tidig diagnos via strukturerad utredning möjliggör förbättrad behandling och prognos (Figur 1) [34, 37].
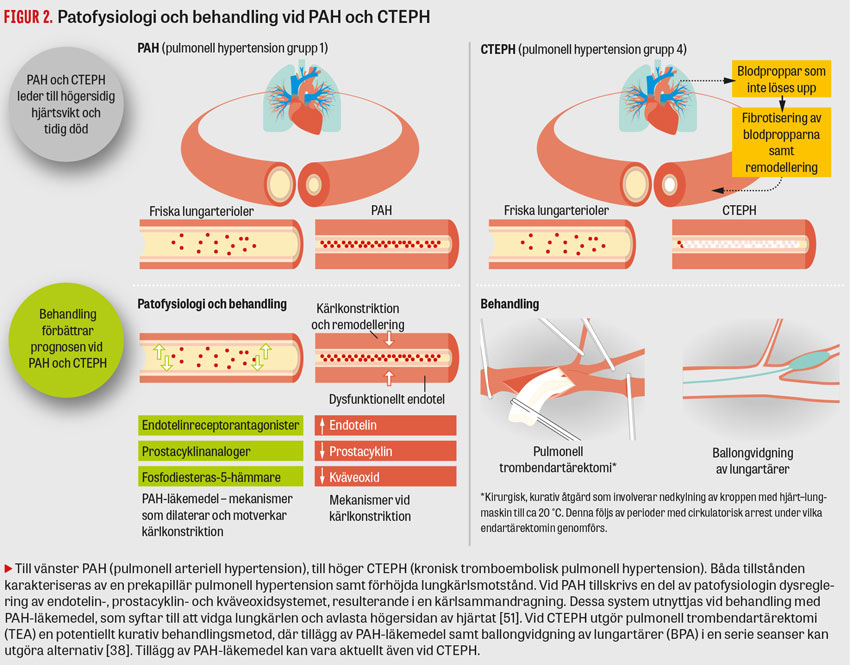
PAH kännetecknas av vasokonstriktion samt progressiv formförändring av lungarteriolerna (Figur 2). Utmärkande för CTEPH, som en konsekvens av oupplösta tromboembolier, är bindvävsbildningar i lungartärerna med fibrotisering och efterföljande distal remodellering av lungarteriolerna, delvis liknande den vid PAH. Både PAH och CTEPH leder till förhöjda lungkärlstryck och -motstånd, vilket orsakar högersidig hjärtsvikt och tidig död [34, 38].
Vid PAH tillskrivs en del av patofysiologin en dysreglering av endotelin-, prostacyklin- och kväveoxidsystemet, resulterande i en kärlsammandragning. Dessa system utnyttjas vid behandling med PAH-läkemedel, som syftar till att vidga lungkärlen och avlasta högersidan av hjärtat (Figur 2) [39]. Vid CTEPH utgör pulmonell trombendartärektomi (TEA) en potentiellt kurativ behandlingsmetod, där tillägg av PAH-läkemedel samt ballongvidgning av lungartärer (BPA) i en serie seanser kan utgöra alternativ [38, 39]. Symtom och kliniska fynd för PAH och CTEPH beskrivs i Fakta 3.
Fördröjning till diagnos
Fördröjningar till diagnos har associerats med sämre mående och prognos, i synnerhet vid allvarliga tillstånd såsom PAH och CTEPH [40, 41]. Både nationella och internationella studier visar på en mediantid från symtomdebut till diagnos på ca 1,2 år hos patienter med PAH och motsvarande för CTEPH [41-45]. En undersökning av patientföreningen PAH Sverige 2020 visade att 40 procent av PAH-patienterna väntade över ett år innan de sökte vård och att 25 procent av patienterna uppskattade att de gjorde fler än 10 vårdbesök innan de remitterades till specialistmottagning [42].
Strukturerad utredning av dyspné
Initial handläggning. Anamnes och karakterisering av andfåddheten är, liksom kliniskt status, avgörande för handläggning [2, 4]. Minnesregeln OPQRST+, som används för smärtanamnes, kan tillämpas för en snabb karakterisering av andfåddheten (Fakta 1). Eftersom andfåddhet kan saknas trots hög andningsfrekvens, eller föreligga vid normal andningsfrekvens, bör den inte förväxlas med kliniska iakttagelser [2, 5, 11]. Således är det av vikt att fråga patienten om dennes symtombild (Fakta 1). Vid akut dyspné är utredningsmålen att utesluta allvarliga orsaker samt fastställa diagnos. Vid kronisk dyspné är det viktigt att klargöra om andfåddheten beror på försämring av underliggande sjukdom eller ett nytt pålagrat tillstånd. Omvärdering av tidigare diagnos kan bli aktuell [2].
Initialt bör bedömning av hjärt- och andningsfrekvens, blodtryck, syremättnad, medvetandegrad och temperatur göras. Förändringar i dessa vitalparametrar har visats vara av prognostisk betydelse, där patologiska värden associerats med ökad sjukhusmortalitet [46].
Steg 1. Anamnes och kliniskt status utgör grunden för diagnostisk vägledning och kan vid kronisk dyspné klargöra rätt diagnos i ca 2/3 av fallen, men behöver kompletteras för att utröna slutgiltig genes bakom andfåddheten [2, 47]. Efter bedömning av patientens vitalparametrar anpassas den första basala utredningen (Figur 1, steg 1) utifrån aktuell vårdinstans samt resurstillgänglighet och bör initieras oberoende av var patienten befinner sig i vårdkedjan. Utredningen bör initialt vara inriktad på att utesluta vanliga orsaker såsom anemi/järnbrist, KOL eller hjärtsvikt, men även tyreoideasjukdom, och kan påbörjas med analys av biokemiska markörer innefattande Hb, TSH, fT4, NT-proBNP och kreatinin [4].
Vidare är ett 12-avlednings-EKG i vila av värde för att påvisa rytmrubbningar och retledningshinder (förmaksflimmer och skänkelblock), förekomst av belastning eller ischemi (P-mitrale, P-pulmonale, hypertrofi respektive övergående höjningar eller sänkningar i ST-sträckan) samt tecken på gamla infarkter (patologiska Q-vågor). Hjärt-/lungröntgen kan förstärka den kliniska misstanken och påvisa lunginfiltrat som vid pneumonier men även pneumotorax eller inkompensation. En enkel spirometri med reversibilitetstest kan avslöja obstruktiv eller restriktiv lungfunktionsnedsättning och föranleda vidare utredning/behandling [15, 48].
Steg 2. I steg 2 görs riktade undersökningar utifrån den övergripande frågeställningen relaterad till fynden i steg 1 (Figur 1). Utökad provtagning, inklusive troponin, D-dimer vid låg klinisk misstanke om lungemboli, arteriell blodgas samt autoimmunscreening, kan bli aktuell. För uteslutande av lungsjukdom ska komplettering med spirometri med diffusionskapacitet och reversibilitetstest samt vid behov metakolintest utföras. Vid kardiopulmonell sjukdom kan ergospirometri ge information om den dominerande genesen bakom andfåddheten och begränsningen i arbetsförmågan. Vidare bör DT av torax med högupplösningsteknik utnyttjas för klargörande av förekomst av parenkymförändringar i lungorna, inklusive lungfibros och emfysem. Lungskintigrafi vid akut och/eller kronisk lungembolism är nödvändig för att klargöra ventilations-/perfusionsdefekter som kan föreligga även vid KOL, fetma, hjärtsvikt, höger–vänstershunt i hjärtat samt vid tumörer. DT-angiografi vid lungembolimisstanke kan övervägas i akut skede eller för senare karakterisering [49].
Vid misstanke om hjärtsjukdom ska ultraljud utföras för att fastställa systolisk/diastolisk dysfunktion, ejektionsfraktion, förekomst av hypertrofi, högerkammarbelastning, perikardvätska, klaffsjukdom samt tecken på pulmonell hypertension. Vid klar misstanke om ischemisk hjärtsjukdom bör man vara mer restriktiv med arbets-EKG, då det har sämre diagnostisk säkerhet jämfört med avbildningstekniker [50]. Vid misstanke om kranskärlssjukdom bör man bedöma »pre-test-probability« samt göra en klinisk sannolikhetsbedömning (clinical likelihood), som ger vägledning om fortsatt utredning [50]. Vid stark klinisk misstanke, icke-känd kranskärlssjukdom och goda förutsättningar för hög bildkvalitet rekommenderas koronar DT-angiografi. Vid låg klinisk sannolikhet rekommenderas i första hand icke-invasiva funktionella avbildningsundersökningar såsom stressekokardiografi, myokardskintigrafi eller MR hjärta [50].
Remittering till specialistvård. Om diagnos inte kan fastställas efter adekvat utredning enligt steg 1 och 2 (Figur 1) ska tidig kontakt tas med specialistenhet. Vid misstanke om PAH eller CTEPH (pulmonell hypertension grupp 1 och 4) ska kontakt tas specifikt med universitetssjukhusens centrum för pulmonell hypertension, för vägledning samt ställningstagande till remittering. Vad remissen bör innehålla presenteras i (Fakta 4).
Steg 3. Inför detta steg (Figur 1, steg 3) remitteras patienten till ett centrum för pulmonell hypertension, där högersidig hjärtkateterisering utgör hörnstenen i differentiering mellan pre- och postkapillär pulmonell hypertension (Fakta 4). Därutöver utförs ett nytt riktat ultraljud av hjärtat samt vid behov MR hjärta för precisering av hjärtshuntar och kärlanomalier samt för prognostisering. Vid misstanke om CTEPH vid lungskintigrafi kompletteras det med pulmonalisangiografi samt eventuellt DT-angiografi för karakterisering samt klargörande av huruvida tillståndet är operabelt med trombendartärektomi eller ballongdilatation (Figur 2) [38, 48].
Vid PAH vägleds sedan behandlingsstrategi och uppföljning via prognostisk riskstratifiering enligt ESC/ERS-riktlinjerna [48]. Utifrån kliniska parametrar, inklusive 6 minuters gångsträcka, funktionsklass enligt WHO, NT-proBNP, ultraljud av hjärta samt hjärtkateterisering, bedöms om patienterna har en låg, intermediär eller hög risk för klinisk försämring och död, motsvarande en ettårsmortalitet på < 5, 5–20 respektive > 20 procent[37, 48]. Behandlingen vid PAH syftar sedermera till att åstadkomma och/eller upprätthålla en lågrisknivå, avseende de kliniska parametrarna, via strukturerade uppföljningar på mottagningar för pulmonell hypertension vid specialistcentrum. Dessa utgår från ett holistiskt samarbete inom multidisciplinära team för att säkerställa ett brett förhållningssätt och upprätthålla hög kvalitet [42]. Vid CTEPH kan liknande riskstratifiering som vid PAH övervägas [48].
Ökad medvetenhet om PAH och CTEPH. Det tar tyvärr ofta lång tid från första symtom till diagnos, då patienter söker sent i förloppet och utredningen även försenas hos vårdgivare i tron att symtomen beror på vanliga, mindre allvarliga tillstånd. Arbetet vid landets specialistcentrum ska, i samråd med Svensk förening för pulmonell hypertension och patientföreningen PAH Sverige, fortsatt verka för att skapa en bredare kännedom om sjukdomarna PAH och CTEPH samt behovet av en tidig och strukturerad utredning tills diagnosen är klar [45].
Konklusion
Andfåddhet är ett vanligt och potentiellt allvarligt symtom som tidigt bör utredas strukturerat med fokus på att utesluta allvarliga differentialdiagnoser. PAH och CTEPH är sällsynta sjukdomar, där tidig diagnos och behandling möjliggör förbättrad prognos. En avvägning bör kontinuerligt göras avseende omvärdering av tidigare diagnos samt när kontakt med specialistcentrum är nödvändig. Det är viktigt att minska både vård- och patientrelaterad fördröjning till diagnos. Att identifiera PAH och CTEPH vid oklar dyspné är som att leta efter en nål i en höstack, där man till en början inte vet att det är nålen man letar efter. Detta kan dock underlättas med stöd av dyspnéutredningsschemat (Figur 1).
Potentiella bindningar eller jävsförhållanden: Salaheldin Ahmed och Abdulla Ahmed har erhållit föreläsararvoden från Janssen. Göran Rådegran är eller har varit engagerad i rådgivande kommittéer för Acceleron, Actelion Pharmaceuticals, Bayer Health Care, Eli Lilly, Glaxo Smith Kline, Janssen, MSD och Sanofi, har erhållit föreläsararvoden från Actelion Pharmaceuticals, Bayer Health Care, Glaxo Smith Kline, Janssen och Nordic Infucare samt är eller har varit klinisk prövare i PAH-studier för Acceleron, Actelion Pharmaceuticals, Bayer Health Care, Glaxo Smith Kline, Janssen, Pfizer och United Therapeutics och i hjärttransplantationsstudier för Novartis.
Fakta 1. Karakterisering av dyspné enligt minnesregeln OPQRST+
Debut/uppkomst (Onset – O)
- Plötslig?
- Smygande?
– Akut dyspné (< 4 veckor)
– Kronisk dyspné (> 4–8 veckor)
Position (Position – P)
- Högt andningshinder/främmande kropp?
- Försämring i liggande?
Kvalitet (Quality – Q)
- Ansträngd andning?
- Trånghet i bröstet?
- Kvävningskänsla?
- Lufthunger?
- Ofullständig inandning?
Förbättrande/försämrande faktorer (Relieving/worsening – R)
- Vila?
- Nattetid?
- Fysisk ansträngning?
- Mediciner/inhalationer?
Intensitet (Severity – S)
- ADL
- Gång
– På plan yta (meter)?
– Trappor (antal steg)?
Kvantifiering av andfåddhet
- Enkla skalor
– Borgskalan (modifierad)
– 6 minuters gångtest
– mMRC (modified Medical Research Council dyspnea score)
– VAS (visuell analogskala) - Multidimensionella skalor
– Dyspnoea-12
– Multidimensional dyspnea profile (MDP) - När patienten inte kan tillfrågas
– Respiratory distress observation scale
Tid/trend (Time/trend – T)
- Konstant?
- Intermittent?
- Varierande över tid?
- Liknande episoder tidigare?
- Utveckling över tid?
Associerade symtom (+)
- Synkope?
- Yrsel?
- Bröstsmärta?
- Hjärtklappning?
- Muskelsvaghet?
- Svullnad/smärta i benen?
- Feber/frossa?
- Hosta?
Minnesregeln OPQRST+ för smärtanamnes kan användas för att på ett snabbt och strukturerat sätt karakterisera patientens andfåddhet.
Kliniska tecken inklusive takypné, hyperpné, användning av accessorisk andningsmuskulatur eller interkostalmuskelindragningar, enstaka eller i kombination, kan – men inte nödvändigtvis – indikera förekomst av dyspné.
Fakta 2. Patofysiologi av dyspné vid olika genes
Hjärtsvikt
- Ökad »andningsdrive« genom ökad afferent signalering via bland annat sträckreceptorer i lungor samt vaskulära receptorer till centrala respiratoriska centrum [2]
- Försämrat gasutbyte och dynamisk hyperinflation av lungorna
- Aktivering av receptorer i muskelceller som respons på förändringar i vävnadernas metabola miljö [2]
- Nedsatt systolisk pumpförmåga och hjärtminutvolym, nedsatt relaxationsförmåga av hjärtat och förhöjda fyllnadstryck, minskning av slagvolym och ventilationsreserver [52]
Ischemisk hjärtsjukdom
- Ischemi i myokardcellerna, ökning av fyllnadstryck och hjärtsvikt
- Försämrad ventrikulär eftergivlighet [53]
KOL
- Nedsatt ventilationsmekanik och hyperinflation av lungorna
- Försämrat gasutbyte
- Kakexi – försvagning av respirationsmuskulaturen
- Förkortning av inspiratoriska muskler och ineffektiv expansion av bröstkorgen [2, 5]
Astma
- Nedsatt ventilationsmekanik och hyperinflation av lungorna
- Luftvägsobstruktion
- Försämrat gasutbyte
PAH och CTEPH
- Pulmonell vaskulär sjukdom – ökad afferent signalering, möjligen via vaskulära och J-receptorer [2]
- Förhöjda fyllnadstryck, högersidig hjärtsvikt samt minskad hjärtminutvolym och kardiell reserv [54]
- Försämrat gasutbyte [54]
Pneumonier
- Försämrat gasutbyte genom ökat diffusionsavstånd mellan alveoler och kapillärer
Blodgasrubbningar/blodsjukdomar
- Vid hypoxi, hyperkapni och acidos ökar den spontana »andningsdriven« och därmed intensiteten av dyspné [2, 5]
- Anemi medför minskad syreupptagningsförmåga. Hemoglobinopatier kan medföra nedsatt frisättning av syre till vävnaderna [2]
Neuromuskulära sjukdomar
- Ineffektiv ventilationsmekanik och därav reducerad afferent feedback för ett efferent respiratoriskt ventilationskommando [2, 5, 26]
Psykogena tillstånd
- Ökad »andningsdrive« och ökad afferent central signalering
- Ökat andningsarbete t ex under hyperventilation [2, 33]
Fysiologiska tillstånd
Graviditet
- Förhöjd central »andningsdrive« genom ökning av bland annat progesteron och östrogen och/eller medvetenhet om hyperventilation som utmärks av ökning i tidalvolymen och oförändrad andningsfrekvens i vila [2, 12, 28, 29]
Fetma
- Minskad eftergivlighet i bröstkorgen [2, 12]
- Ökad luftvägsresistans samt försämrad statisk styrka i inspiratoriska och exspiratoriska muskler [12]
Normalt åldrande
- Minskad eftergivlighet i bröstkorgen [2, 12]
- Förkalkning av intervertebrala utrymmen och ökning av »dead space«
- Försvagning av in- och utandningsmuskler på grund av förlust av muskelmassa, dekonditionering och/eller malnutrition [12]
Tyreoideasjukdomar
Struma och tumörer
- Mekanisk obstruktion av övre luftvägarna. Metastasering till lungorna [22]
Hypertyreoidism
- Adrenergt påslag
- Ökad central »andningsdrive« och ventilation
- Hyperdynamisk cirkulation och hjärtsvikt
- Muskelsvaghet [23]
Svår hypotyreoidism
- Alveolär hypoventilation
- Minskning av »andningsdriven«
- Svaghet i respiratorisk muskulatur [24]
Fakta 3. Symtom och möjliga kliniska fynd vid PAH och CTEPH
Anamnes
- Symtom vid högersidig hjärtsvikt: Oproportionerlig andfåddhet vid ansträngning, trötthet, synkope, bröstsmärta (hos upp till 40 procent), dyspné vid framåtlutning (bendopné) och i liggande (ortopné)
Dessutom vid CTEPH
- Tidigare lungemboli/ventrombos (25 procent utan tidigare anamnes)
- Kvarstående andfåddhet efter lungemboli trots optimal antikoagulationsbehandling under minst 3 månader
Status
- Pansystoliskt blåsljud motsvarande trikuspidalisinsufficiens
- Diastoliskt blåsljud motsvarande pulmonalisinsufficiens
- Ökat bukomfång till följd av ascites
- Bensvullnad
Saturation
- Normal/sänkt
Lungfunktionstest
PAH – varierande beroende på subtyp
- Normal eller sänkt lungvolym och diffusionskapacitet för CO (DLCO)
- 20–50 procent kan uppvisa en restriktiv lungfunktion (total lungkapacitet < 80 procent av predicerad)
- Hos 20–40 procent (idiopatisk PAH) är FEV1 /FVC < 70 procent [55]
CTEPH
- Normal eller sänkt lungvolym och DLCO
- Upp till 30 procent kan ha restriktiv lungfunktionsbild (total lungkapacitet < 80 procent av predicerad)
- Upp till 60 procent kan ha reducerad DLCO [55]
EKG
- Normalt
- Tecken på högerkammarpåverkan
- Förmaksflimmer/-fladder
- Högerställd elaxel
Hjärt-/lungröntgen
- Normal
- Vida centrala lungkärl
- Förstorade höger förmak och kammare
Ekokardiografi
- Förhöjt flöde över trikuspidalisklaffen
- Systoliskt lungartärblodtryck (sPAP) ≥ 35 mm Hg
- Hypertrofi/dilatation av höger förmak och kammare
Autoimmunscreening
- Normal
- Positiv för ANA (antinukleära antikroppar), ENA (antikroppar mot extraherbara nukleära antigener)
Bild- och funktionsundersökningar
Normal eller tecken på lungsjukdom
Lungskintigrafi (V/Q scan)
- PAH: Normal eller perfusionsdefekt i bronkiella delsegment
- CTEPH: Perfusionsdefekt i multipla bronkiella segment
Högersidig hjärtkateterisering
PAH
- Förhöjda medelpulmonalisartärtryck (mPAP > 20 mm Hg i vila), lungkärlsmotstånd (pulmonell vaskulär resistans [PVR] > 2 Wood-enheter) samt normala pulmonella inkilningstryck (PAWP ≤ 15 mm Hg)
CTEPH
- Förhöjda medelpulmonalisartärtryck (mPAP > 20 mm Hg i vila) , PVR > 2 Wood-enheter samt normala pulmonella inkilningstryck (PAWP ≤ 15 mm Hg)
Fakta 4. När kontaktas/remitteras till centrum för pulmonell hypertension och vad ska remissen innehålla?
För patienter med pulmonell hypertension i grupp 1 (PAH) samt grupp 4 (CTEPH) föreligger möjligheter för specifik behandling, varför kontakt med centrum för pulmonell hypertension är nödvändig. En remiss bör innefatta anamnes inklusive förekomst av samsjukligheter och klinisk presentation, liksom utredningsfynd från det som genomförts inom ramen för steg 1–2-utredning.
- Frågeställning och misstanke
- Anamnes inklusive samsjuklighet och hereditet, gärna med dyspnékarakterisering
- Klinisk kemi: Laboratorieprov inklusive NT-proBNP
- Längd och vikt
- Ekokardiografi:
– Vänsterkammarfunktion
– Förmakens storlek
– Klaffarnas status
– Siffra på HK/HF-gradienten (tryckgradienten mellan höger kammare och höger förmak) mer betydelsefull än ett uppskattat medeltryck i lungartären
– Perikardvätska - Lungfunktion:
– Spirometri med eller utan diffusionskapacitet - Avbildningsundersökningar:
– Lungröntgen
– HRCT (högupplösande datortomografi)
– Lungskintigrafi
ENA- och ANA-profil vid misstanke om vaskulit eller autoimmun sjukdom med systemisk skleros som orsak till PAH.
Kontakt med specialistcentrum för pulmonell hypertension kan upprättas tidigare vid stark misstanke om PAH och CTEPH [48].