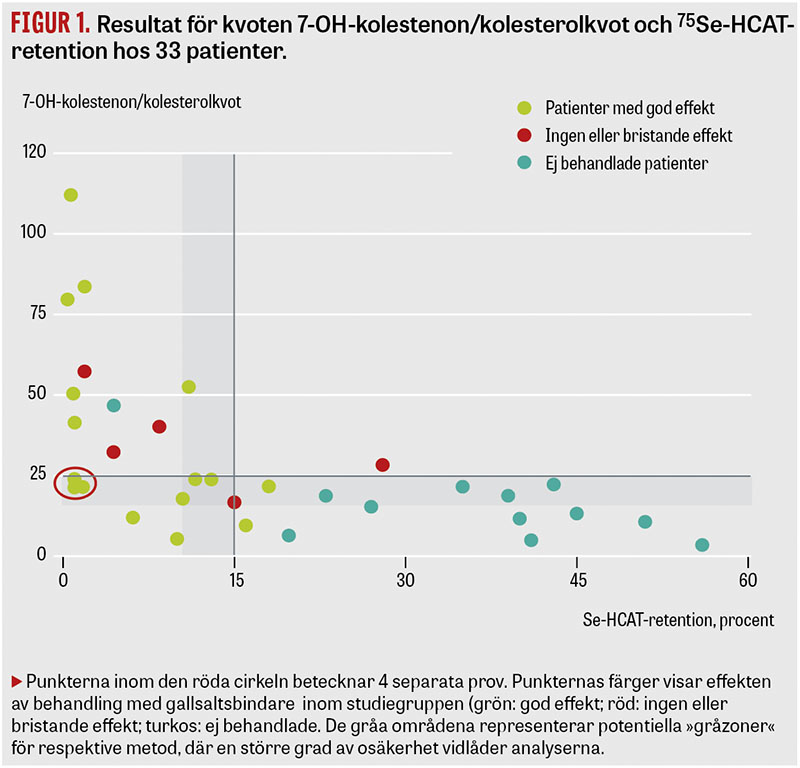
Gallsaltsdiarré förmodas vara ett underdiagnostiserat tillstånd, där effektiv behandling dock finns tillgänglig. Det är därför av vikt att identifiera dessa patienter.
Ett enkelt blodprov kan användas för kostnadseffektiv diagnostik av gallsaltsdiarré.
Ett förhöjt värde säkerställer diagnosen, medan ett lågt värde utesluter diagnosen gallsaltsdiarré. Resultat belägna i en gråzon mellan dessa nivåer innebär att diagnosen inte säkert kan uteslutas, vilket kan kräva kompletterade undersökning, till exempel 75Se-HCAT-test.
Gallsaltsdiarré är ett kliniskt tillstånd som kan vara den oftast förbisedda diagnosen hos patienter med kronisk diarré. 26–32 procent av de patienter som tidigare ansågs ha IBS med diarré eller funktionell diarré har visat sig ha gallsaltsdiarré [1, 2], ett tillstånd som går att behandla. Sjukdomen anses ha en prevalens om ca 1 procent i västerländska populationer [3], men i Sverige har ännu inga genomarbetade studier utförts. Utöver postoperativ gallsaltsdiarré (typ 1) och idiopatisk gallsaltsdiarré (typ 2) kan tillståndet förekomma vid andra sjukdomar i mag–tarmkanalen (typ 3) som mikroskopisk kolit, inflammatorisk tarmsjukdom, celiaki och neuroendokrina tumörer [4].
Symtomen vid gallsaltsdiarré domineras av imperativa, täta trängningar och vattniga diarréer, även nattetid, ibland med fekal inkontinens, vilket kan vara mycket besvärande för patienten och medföra nedsatt livskvalitet. Gallsaltsdiarré kan ha flera olika orsaker. Den vanligaste är en ökad produktion av gallsalter i levern, som inte kan tas upp i distala ileum i tillräcklig utsträckning. Den förhöjda mängden gallsalter mättar transportsystemen och ger en ökad överföring av gallsalter till tjocktarmen, vilket stegrar både tarmens sekretion och dess motoriska aktivitet. Effekterna förmedlas bland annat av särskilda receptorer i tarmväggen, som specifikt aktiveras av gallsalter [5]. Andra orsaker är nedsatt återupptag av gallsalter i ileum på grund av patologiska förändringar, exempelvis inflammation, strålskada eller distal ileumresektion. Oavsett orsak utsöndrar patienterna i regel en förhöjd mängd gallsalter i feces.
Gallsalterna syntetiseras från kolesterol i leverns hepatocyter och utsöndras via gallan till tarmen efter måltid för att underlätta upptaget av fett från födan. Under normala omständigheter återresorberas cirka 95 procent av gallsalterna i distala ileum med hjälp av transportproteinet IBAT (ileal gallsyratransportör), även kallat ASBT (apikal natriumberoende gallsyratransportör), för att sedan återföras till levern via portablodflödet [6]. Resterande 5 procent av gallsalterna når kolon och lämnar kroppen med feces. Syntesen av gallsalter är komplex och noggrant reglerad via olika återkopplingsmekanismer. En viktig komponent är FGF19 (fibroblasttillväxtfaktor 19), ett protein som bildas av enterocyterna i distala ileum och vars produktion stimuleras av gallsyror. FGF19 transporteras i blodbanan till levern och hämmar gallsyrasyntesen genom att nedreglera det hastighetsreglerande enzymet CYP7A1 i syntesprocessen. Även gallsalter i sig reducerar aktiviteten av CYP7A1 och leder till minskad syntes.
Diagnostiska metoder
Diagnostik av gallsaltsdiarré blir aktuell först när vanliga orsaker till vattnig diarré, som infektioner, mikroskopisk kolit och celiaki, har kunnat uteslutas. Gallsaltsdiarré har länge varit problematisk att diagnostisera, men situationen har efter hand förbättras. I dag finns det tre, eller möjligen fyra, diagnostiska verktyg:
75Se-HCAT-undersökning. En gallsyraanalog märkt med 370 kBq selen-75 intas på fastande mage i form av en kapsel, och efter 3 timmar mäts aktiviteten över buken med en okollimerad gammakamera. Spårämnet cirkulerar i det enterohepatiska kretsloppet, och kvarvarande aktivitet mäts sedan på samma sätt efter 7 dygn [7]. Retention av <10 procent efter korrektion för bakgrundsaktivitet och fysikaliskt sönderfall utgör en stark indikation om ökade förluster av gallsyror via feces. Värden över 15 procent gör diagnosen osannolik, medan värden mellan 10 och 15 procent betecknas som en gråzon [6]. Metoden är i dag tillgänglig inom rutindiagnostik i Sverige, men den är dyr och tidskrävande.
Kvantitativ bestämning av serum 7-OH-kolestenon. Detta är en stabil gallsyrametabolit vars koncentration har visat sig motsvara den aktuella gallsyrasyntesens storlek. Metaboliten mäts med vätskekromatografi–masspektrometri, en mycket specifik metod med låg risk för interferenser [8]. Serumnivån av 7-OH-kolestenon är beroende av mängden totalkolesterol, varför man använder kvoten mellan 7-OH-kolestenon (7-alfahydroxi-4-kolesten-3-on) och totalkolesterol [9]. Kvotvärden över 25 nmol/mmol är förenliga med gallsaltsdiarré [10]. Metoden är sedan 2010 etablerad vid kliniskt kemiska laboratoriet vid Karolinska universitetssjukhuset.
Kvantitativ bestämning av gallsyror i feces efter 48 timmars samling. Förhöjda nivåer talar för diagnosen gallsaltsmalabsorption/-diarré [11]. Metoden är i dag inte tillgänglig i klinisk rutin i Sverige.
En fjärde möjlighet är att provbehandla patientens diarré med en gallsaltsbindare. Bundna gallsyror utsöndras med feces och förhindras på så sätt att interagera med cellerna i kolon. Detta är emellertid långt ifrån oproblematiskt. Dels finns en mycket stor variation mellan olika patienter i hur mycket gallsaltsbindare som behövs för att stoppa diarrén, dels verkar det finnas en tröskelnivå som behöver uppnås och från vilken behandlingen sedan ska minskas för att varaktig förbättring ska erhållas. Provbehandling har emellertid visats vara otillräcklig för att diagnostisera gallsaltsdiarré [12]. Då detta vanligen är ett livslångt tillstånd är det enligt vår mening rimligt att beslut om behandling baseras på så objektiva grunder som möjligt.
Behandling av gallsaltsdiarré
Historiskt började man använda gallsaltsbindande resiner i slutet av 1960-talet för att minska gallsalternas effekter på sekretion och motilitet i tjocktarmen [13, 14]. En metaanalys med 15 studier av patienter med idiopatisk gallsaltsdiarré visade att 96 procent av dem svarade på behandling med kolestyramin vid en 75Se-HCAT-retention <5 procent. 80 procent av dem med <10 procent retention och 70 procent av dem med <15 procent retention svarade också på behandlingen [1].
Kolestyramin, ett resin som i dag är förstahandsval vid behandling av gallsaltsdiaré, är ett granulat som många uppfattar som svårt att ta. I slutet av 1990-talet introducerades kolesevelam, liksom kolestyramin primärt för behandling av hyperkolesterolemi. En fördel med kolesevelam är att det är en tablett som ger bättre följsamhet till medicinering. Medlet binder också fler gallsalter och har färre biverkningar och färre interaktioner med andra mediciner [15]. Tre studier har jämfört kolesevelam med placebo vid olika tillstånd med gallsaltsmedierad diarré. Av dessa redovisar två studier en positiv behandlingseffekt av kolesevelam [16, 17], medan en [18] inte kunde visa någon symtomminskande effekt. I Sverige har kolesevelam dock inte gallsyradiarré som godkänd indikation, men kan övervägas i utvalda fall. Kolestipol är inte längre tillgängligt.
En intressant studie från Danmark jämförde resultaten vid behandling med kolesevelam (3 tabletter 625 mg morgon och kväll) respektive GLP-1-receptoragonisten liraglutid hos patienter med 75Se-HCAT-verifierad (<10 procent retention efter 7 dagar) gallsaltsmedierad diarré [19]. Liraglutid titrerades upp från 0,6 mg till 1,8 mg över 3 veckor. Efter 6 veckors behandling uppnådde 20 av 26 patienter behandlade med liraglutid en reduktion av antalet avföringar på ≥25 procent, och 13 av 26 kolesevelambehandlade patienter uppnådde en liknande förbättring. Liraglutid minskade emellertid gallförlusterna mätt med 75Se-HCAT och sänkte nivåerna av 7-OH-kolestenon, medan kolesevelam gav oförändrade gallförluster och stigande nivåer av 7-OH-kolestenon.
Retrospektiv studie
Vi har genomfört en retrospektiv studie för att undersöka samstämmigheten mellan serum-7-OH-kolestenon/kolesterolkvot och 75Se-HCAT-retention. Studien godkändes av Etikprövningsmyndigheten (dnr 2019-05386). Studiematerialet omfattade patienter som inremitterats för utredning av kronisk diarré och som genomgått både 75Se-HCAT-undersökning och analys av 7-HO-kolestenon/kolesterolkvot under tidsperioden 2010 till 2020. Tidsintervallet mellan undersökningarna begränsades till högst 6 månader. 47 patienter identifierades genom att produktionsregistren från nuklearmedicin vid Karolinska universitetssjukhuset Solna och det kliniskt kemiska laboratoriet vid Karolinska universitetssjukhuset Huddinge jämfördes. Från detta material exkluderades 14 patienter som hade andra sjukdomar eller tillstånd med verifierad gallsaltsmalabsorption (resektion av distal tunntarm, Crohns sjukdom, mikroskopisk kolit, strålningsorsakad enterit eller celiaki) eller som behandlades med gallsaltsbindande läkemedel vid något av undersökningstillfällena. Den heterogenitet som vidlådde dessa 14 exkluderade patienter gjorde att några säkra slutsatser knappast kunde erhållas i den lilla gruppen. Av de återstående patienterna var 25 kvinnor i åldern 18–73 år (medianålder 38 år) och 8 män i åldern 18–73 år (medianålder 26 år). På grund av materialets begränsade omfattning har endast deskriptiv statistik tillämpats.
Resultat
Resultaten av vår studie visade att 9 patienter hade både förhöjd 7-OH-kolestenon/kolesterolkvot och sänkta nivåer av 75Se-HCAT (<15 procent) (Figur 1). Ytterligare 9 fall hade patologiska 75Se-HCAT-värden, medan deras 7-HO-kolestenon/kolesterolkvot var ≤25 nmol/mmol. I 14 fall var både 75Se-HCAT och 7-OH-kolestenonkvoten inom referensintervallet. Ett fall med ordinär 75Se-HCAT-retention visade en lätt ökad 7-OH-kolestenon/kolsterolkvot.
Behandling med gallsaltsbindande läkemedel (kolestyramin, kolestipol, kolesevelam) genomfördes på alla patienter utom en med patologisk 75Se-HCAT-retention (<15 procent) (n = 17). Dessutom behandlades en patient med normal 75Se-HCAT-retention och lätt förhöjd 7-OH-kolestenon/kolesterolkvot. Hos 6 av de 9 patienterna med förhöjd 7-OH-kolestenon/kolesterolkvot och sänkt 75Se-HCAT-retention ledde behandlingen till att diarrén försvann. De övriga 3 patienterna fick ingen eller endast obetydlig effekt. Patienten med förhöjd 7-OH-kolestenon/kolesterolkvot och normal 75Se-HCAT visade inte någon förbättring av diarrén efter behandlingen. 8 patienter med lätt eller måttligt sänkt 75Se-HCAT-retention och 7-OH-kolestenon/kolesterolkvot inom intervallet 5,3–23,9 nmol/mmol uppvisade god effekt av behandling, medan en patient inte följde sin behandling och en patient, som fick precis 15 procent 75Se-HCAT-retention, hade otillräcklig behandlingseffekt.
Sammanfattningsvis visar vår studie en god samstämmighet mellan de båda metoderna trots tidsskillnader mellan undersökningstillfällena. Majoriteten av patienterna med patologisk 75Se-HCAT-retension svarade positivt på gallsaltsbindande behandling. Den grupp patienter vars 7-OH-kolestenon/kolsterolkvot låg inom intervallet 15–25 nmol/mmol bestod av ungefär lika många individer med normal som med patologisk 75Se-HCAT-retention. Följaktligen bör resultat i gråzonen avseende 7-OH-kolestenon/kolsterolkvot leda till vidare utredning av 75Se-HCAT-retention.
Analys av produktionsstatistiken vid laboratoriet åren 2021–2023 avseende 7-OH-kolestenon/kolesterolkvot visar att 66 procent av resultaten var lägre än 15 nmol/mmol, 20 procent var högre än 25 nmol/mmol och 14 procent låg inom intervallet 15–25 nmol/mmol.
I enlighet med detta kan en utredningsgång vid misstanke om gallsaltsdiarré skisseras (Figur 2). Det förefaller rimligt att börja utredningen med att bestämma 7-OH-kolestenon/kolesterolkvoten, då detta i majoriteten av fallen (cirka 86 procent) kan leda till diagnos, medan oklara fall behöver utredas ytterligare.
Diskussion
Resultaten från produktionsstatistiken avseende 7-OH-kolestenon/kolsterolkvot tyder på att man i cirka 86 procent av fallen får en tydlig indikation om patientens tillstånd. Eftersom analysen är både kostnadseffektiv och icke-radioaktiv lämpar sig bestämning av kvoten som ett förstahandsalternativ vid klinisk misstanke om gallsaltsdiarré. För de patienter vars svar hamnar inom gråzonen kan dock uppföljande prov med 75Se-HCAT-undersökning vara indicerat, en slutsats vår studie också stödjer. 7-OH-kolestenon är stabilt åtminstone en vecka vid kyl- eller frysförvaring, men i rumstemperatur är hållbarheten ett dygn. Detta innebär att provet måste skickas kylt eller fryst vid längre transporter.
Analys av 7-OH-kolestenon i serum har dels använts i kombination med 75Se-HCAT-analys [17], dels tillsammans med bestämning av gallsyror i feces [11]. Sensitiviteten anges dock vara lägre än för 75Se-HCAT-analys och beror på hur referensintervallet är definierat. I studien av Borup et al [17] anges en gråzon (50–150 nmol) avseende 7-OH-kolestenon, som dessvärre inte kan jämföras med våra kvotvärden, då kolesterolnivå inte redovisas.
Gallsyrasyntesen uppvisar visserligen en dygnsrytm med högst aktivitet på morgonen, men detta ger så obetydliga förändringar i nivån av 7-OH-kolestenon/kolesterolkvoten att provtagningen inte behöver anpassas därefter [9]. Födointag kan också ändra syntesaktiviteten men påverkar inte analysresultatet, varför patienten inte behöver vara fastande. Alkoholintag ett par timmar före provtagning kan emellertid ge påtaglig ökning av serumnivån av 7-OH-kolestenon [20].
Patienter som har genomgått ileocekalresektion eller har en akut enterit har som regel förhöjda värden, varför analysen i dessa fall inte bör användas. Låga värden (<2,5 mmol/l) förekommer ofta utan någon tydligt identifierbar orsak, men i sällsynta fall kan låga nivåer ses vid gravt nedsatt leverfunktion eller kolestas [21].
Vid det ytterst sällsynta tillståndet cerebrotendinös xantomatos, orsakat av genetisk brist på enzymet sterol 27-hydroxylas (CYP27A1) ses hos obehandlade patienter extremt höga nivåer av 7-OH-kolestenon [22].
Behandling med gallsaltsbindare per os (kolestyramin, kolestipol eller kolesevelam) har ofta gett bestående symtomlindring [5, 17]. Terapin måste fortgå över lång tid, och det är i dag oklart om behandlingen i något skede kan avbrytas utan att symtomen återkommer. Upptaget av fettlösliga vitaminer kan påverkas av behandlingen, och gallsaltsbindarna kan även påverka koncentrationer av andra farmaka, varför de bör administreras tidsmässigt separat från övriga läkemedel. Fettreducerad kost kan leda till viss symtomlindring.
En svaghet med vår studie är ett relativt litet patientmaterial samt att det förelåg tidsskillnader mellan provtagningstillfällena för de två metoderna.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.