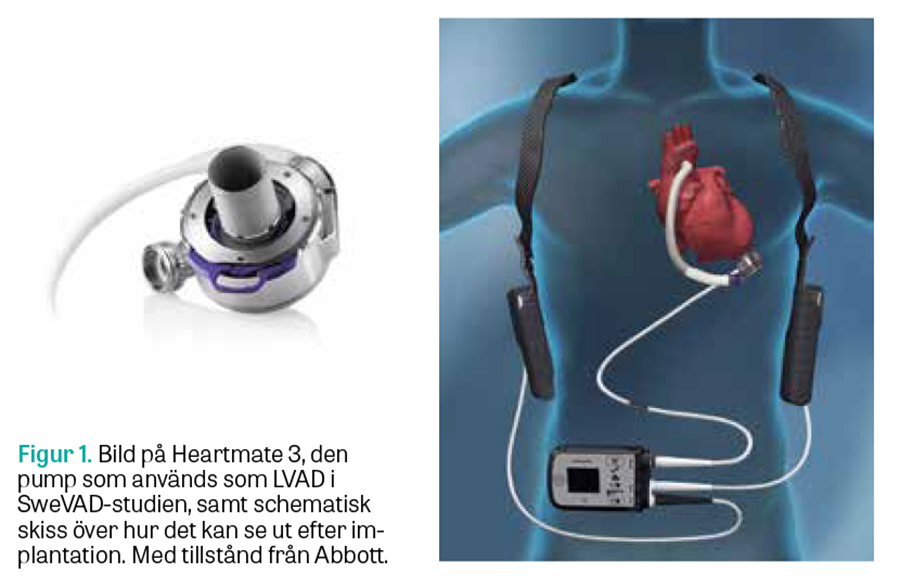
I Sverige har personer med svår hjärtsvikt behandlats med mekaniskt vänsterkammarstöd (left ventricular assist device, LVAD) i över 25 år, dock mest som tillfällig lösning i avvaktan på hjärttransplantation.
Av dem som erhåller vänsterkammarpump överlever 85 procent fram till hjärttransplantation.
Genom teknisk utveckling har pumparna blivit mindre, mer driftsäkra och mer biokompatibla.
I USA och delar av Europa ökar användningen av vänsterkammarpump som permanent behandling utan efterföljande hjärttransplantation.
Enligt Socialstyrelsen bör dock permanent vänsterkammarpump endast tillämpas inom ramen för forskning och utveckling, eftersom det vetenskapliga underlaget anses otillräckligt.
SweVAD är en prövarinitierad landsomfattande multicenterstudie med randomiserad design som utvärderar behandling med permanent vänsterkammarpump hos patienter som inte är lämpliga för hjärttransplantation.
Samtliga sju universitetssjukhus i landet samarbetar kring studien, som finansieras via forskningsanslag, medverkan från regionerna och stöd från industrin.
En fullt implanterbar hjärtpump som brygga (övergångsbehandling) till hjärttransplantation användes för första gången i Sverige 1985 på Karolinska sjukhuset, vilket på sin tid väckte mycket uppmärksamhet [1]. Detta var också det första framgångsrika försöket i Europa där patienten överlevde tack vare en pump fram till hjärttransplantation. I detta fall användes ett så kallat totalt artificiellt hjärta (TAH), som ersätter båda kamrarnas funktion [2]. Den i dag vanligaste formen av en implanterbar hjärtpump stödjer endast vänsterkammaren (left ventricular assist device, LVAD) och har använts som brygga till hjärttransplantation i Sverige sedan 90-talet [3, 4]. I de flesta fall, utom de mest allvarliga och terminala formerna av biventrikulär hjärtsvikt, ger en sådan tilräckligt stöd till det sviktande hjärtat. I länder där det föreligger organbrist går patienterna länge med sin hjärtpump, ibland över 10 år utan att bli transplanterade. I vissa fall har behandlingen blivit permanent, särskilt hos patienter som inte längre är lämpliga för hjärttransplantation på grund av ålder eller samsjuklighet, och benämns då destinationsterapi. I takt med kontinuerlig utveckling av pumpteknik och ständigt förbättrade patientresultat har destinationsterapi med vänsterkammarpump blivit allt vanligare i både USA och Tyskland [5].
Hjärttransplantation
Hjärttransplantation är en etablerad behandling vid avancerad hjärtsvikt. I Sverige utfördes det första hjärtbytet i Göteborg 1984, och i hela landet genomförs numera cirka 60–70 hjärttransplantationer årligen, fördelade på Göteborg och Lund. Den aktuella 10-årsöverlevnaden ligger över 80 procent [6-8]. Huvudindikationen för hjärttransplantation är förekomst av svår symtomatisk hjärtsvikt (NYHA-funktionsklass IIIB–IV) med dålig prognos, där andra behandlingsalternativ är uttömda. Kontraindikationer inkluderar andra tillstånd som kan begränsa överlevnaden efter hjärttransplantation, såsom cancer, infektion, hög biologisk ålder, njursvikt, avancerad aterosklerotisk sjukdom eller multiorgansvikt. På grund av bristen på donatorhjärtan är behandlingen förbehållen ett fåtal och måste prioriteras till patienter där den gör störst nytta. Det existerar ingen övre åldersgräns för hjärttransplantation, men eftersom äldre ofta lider av samsjuklighet och löper större risk för komplikationer listas personer över 65–70 år sällan för hjärtbyte. Det faktum att hjärtsvikt förekommer mycket oftare hos äldre innebär att den stora majoriteten patienter inte erbjuds hjärttransplantation som behandling.
Vänsterkammarpump som brygga till transplantation
Vänsterkammarpumparna blev kommersiellt tillgängliga under 90-talet, varvid användandet som en temporär brygga till hjärttransplantation ökade och mortaliteten på väntelistorna sjönk. I Sverige implanterades en vänsterkammarpump för första gången 1993 i Linköping (Heartmate I, Thoratec Corp, Pleasanton, CA, USA), och patienten genomgick så småningom hjärttransplantation [3]. De tidiga svenska resultaten med denna första generations hjärtpump visade att över 80 procent av patienterna överlevde fram till hjärttransplantationen [3, 9]. När andra generationens pump blev kommersiellt tillgänglig i början av 2000-talet kom behandlingen att spridas till fler sjukhus, och i dag implanteras vänsterkammarpumpar på fem universitetssjukhus i landet (Lund, Linköping, Göteborg, Stockholm och Uppsala). Vänsterkammarpump används i Sverige som brygga till hjärttransplantation. Patienterna är oftast unga till medelålders individer som frånsett sin hjärtsjukdom är relativt friska och som utan pumpbehandling hade försämrats eller avlidit i väntan på hjärttransplantation. I andra fall kan det röra sig om behandling av en kontraindikation för hjärttransplantation, såsom hög lungkärlsresistans, som går tillbaka när vänsterkammaren avlastas med hjärtpumpen. Eftersom en hjärtpump kan förbättra cirkulationen och därmed stabilisera övrig organfunktion har detta lett till högre överlevnad på väntelistan, som i dag ligger kring 85–90 procent [5, 9].
Första generationen av implanterbara vänsterkammarpumpar var tryckluftsdrivna, gav ett pulsatilt flöde och var förhållandevis stora, varför de fick implanteras i buken. Senare generationer har utvecklats till elektromagnetiskt drivna axial- eller centrifugalpumpar som är mindre och kan placeras i bröstkorgen. Tredje generationen är ännu mindre storleksmässigt och får plats inne i hjärtsäcken. Pumptekniken resulterar i ett kontinuerligt flöde, vilket medför att pulsen försvagas eller försvinner. Hjärtpumpen kopplas till en drivlina som går genom huden till en kontrollenhet och strömförsörjande batterier. Med senaste generationens konstruktion har tekniska problem och driftstörningar blivit ovanliga, och ökad biokompatibilitet har avsevärt minskat risken för komplikationer, särskilt tromboembolism från pumphuset, vilket därmed minskat risken för stroke [10]. Ökad biokompatibilitet har också möjliggjort minskning av den rutinmässiga blodförtunningen med både warfarin och acetylsalicylsyra. I en nylig studie med tredje generationens vänsterkammarpump testades enbart warfarin utan trombocythämning, vilket medförde minskad risk för blödningar men ingen ökning av tromboembolism [11], varför trombocythämning inte längre behövs. Omkring 30–40 procent av patienter som listas för hjärttransplantation övergångsbehandlas med en pump [12], och dessa har efter hjärtbyte samma överlevnad som dem som under väntetiden klarar sig utan pump [6].
Vänsterkammarpump som permanent behandling
Den tekniska utvecklingen i form av miniatyrisering, förbättrad driftsäkerhet och ökad biokompatibilitet har tillsammans med goda resultat vid behandling som brygga till hjärttransplantation banat väg för möjligheten att använda hjärtpumpar för permanent behandling (destinationsterapi). Redan under slutet av 1990-talet genomfördes en prospektiv randomiserad studie (Rematch) [13], där svårt sjuka patienter som inte lämpade sig för hjärttransplantation randomiserades till antingen vänsterkammarpump eller optimal medicinsk behandling. Trots att det rörde sig om första generationens konstruktion med begränsad livslängd, så medförde LVAD-behandling bättre 1-årsöverlevnad än medicinsk behandling, dock till priset av betydande pumprelaterad morbiditet, inklusive komplikationer som havererade biologiska klaffar och infektioner. Efter Rematch har alla randomiserade studier kring destinationsterapi enbart jämfört olika generationers vänsterkammarpumpar mot varandra och inte mot optimal medicinsk behandling [14]. Resultat kopplade till permanent LVAD har förbättrats påtagligt över tid [5, 9, 10]. I den senaste stora Momentum-studien jämfördes den senaste generationens pumpar med sina föregångare. Studien inkluderade även ett antal patienter med destinationsterapi, som visade en 5-årsöverlevnad på 60 procent, vilket markerar en tydlig förbättring jämfört med tidigare destinationsterapi [15]. Under samma period har den medicinska behandlingen också utvecklats med nya hjärtsviktsläkemedel, resynkronisering (CRT) och implanterbara defibrillatorer (ICD), som samtliga förbättrar prognosen vid svår hjärtsvikt [16]. Trots optimal behandling med moderna läkemedel och elektroniska hjälpmedel sker ofta en successiv försämring till avancerad hjärtsvikt. I dessa fall kvarstår LVAD som ett potentiellt terapeutiskt alternativ för noggrant utvalda patienter.
Vetenskaplig evidensgrad för permanent behandling
År 2014 publicerade vi en HTA-rapport (health technology assessment) om evidensläget för permanent LVAD [17]. Slutsatsen blev att permanent LVAD-behandling sannolikt ger en överlevnadsvinst, men att det vetenskapliga underlaget var bristfälligt och att det inte fanns några hälsoekonomiska beräkningar, varför stödet för behandlingen blev svagt. Vidare konstaterade vi att det inte förelåg någon randomiserad studie som jämförde senare generationers LVAD med modern medicinsk hjärtsviktsbehandling. I analogi med detta har Socialstyrelsens grupp för prioritering av hjärtsjukdomar bedömt att behandling med permanent LVAD enbart bör begränsas till forskning och utveckling (FoU) [18]. I de europeiska hjärtsviktsriktlinjerna från 2021 erhåller permanent LVAD-behandling rekommendationsgrad IIa, vilket innebär att behandlingen bör övervägas hos noga selekterade patienter med avancerad hjärtsvikt, men att det kvarstår komplikationsrisker och att ytterligare studier behövs om rekommendation av graden I ska uppnås [19]. Det bör uppmärksammas i detta sammanhang att de europeiska riktlinjerna inte tar hänsyn till behandlingens kostnad eller kostnadseffektivitet samt även anger att SweVAD-studien (Swedish evaluation of left ventricular assist device as permanent treatment in end-stage heart failure) pågår och kommer att påverka den framtida strategin rörande permanent LVAD.
SweVAD-studien
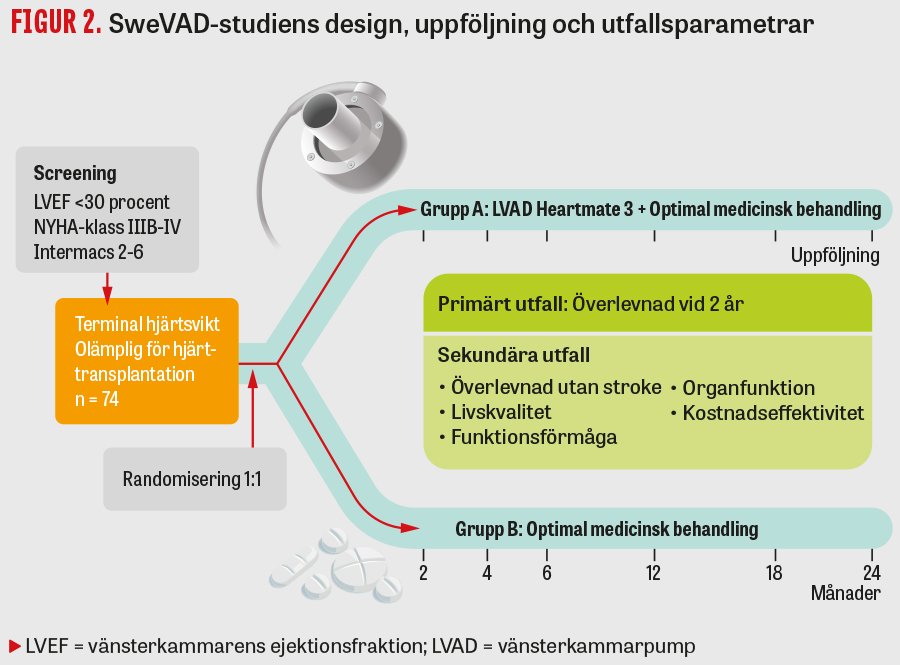
Eftersom vi i Sverige bedömde evidensgraden för permanent LVAD-terapi som otillräcklig har behandlingen inte kunnat införas i klinisk praxis. Vi valde därför att initiera SweVAD-studien för att avgöra om destinationsterapi kunde vara ett alternativ för hjärtsviktspatienter som inte är kandidater för hjärttransplantation. I studien använder vi tredje generationens LVAD (Heartmate 3, Abbott) med goda prestanda och adekvat kringutrustning (Figur 1). Det bör också påpekas att permanent LVAD inte erbjuds utanför studien i Sverige. SweVAD-studien är en prövarinitierad, prospektiv, icke-blindad, nationell randomiserad studie med mångsidig finansiering (Figur 2). Studien följer god klinisk praxis (GCP-ICH) och är registrerad på Clinicaltrials.gov (NCT02592499). Patienterna ska vara i NYHA-funktionsklass IIIB–IV och/eller uppvisa Intermacs-profil (Interagency registry for mechanically assisted circulatory support) 2–6 för att komma i fråga, och patienterna måste ha nekats hjärttransplantation, till exempel på grund av hög ålder och/eller samsjuklighet. Således kan patienter mellan 70 och 80 år som i allmänhet anses olämpliga för hjärttransplantation vara lämpliga för SweVAD. Dessutom kan patienter yngre än 70 år med samsjuklighet som hindrar hjärtbyte eller immunhämmande behandling övervägas för studien. Exempel på tillstånd som utgör en kontraindikation för hjärttransplantation, såsom BMI >35 kg/m2, cancer senaste 5 åren med oklar prognos, måttlig–svår njursvikt, svåra diabeteskomplikationer, resttillstånd efter stroke och signifikant perifer kärlsjukdom, behöver inte vara hinder för deltagande i SweVAD-studien, och varje patient får bedömas individuellt. Även om viss komorbiditet accepteras måste patienternas operationsrisk vara rimlig, och deras förväntade livslängd efter LVAD-implantation bör överstiga 2 år. SweVAD-studien leds av en styrgrupp och har en säkerhetskommitté samt en bedömningskommitté för kliniska händelser. Vi har rekryterat 72 patienter som har randomiserats till antingen vänsterkammarpump eller medicinsk behandling i förhållandet 1:1. Vi planerar att rekrytera sammanlagt 74 patienter och är således nära målet. Patienterna följs upp under 2 år och hela studieprotokollet har publicerats separat [20].
Diskussion
SweVAD-studien undersöker effekten och säkerheten av LVAD som destinationsterapi hos patienter med avancerad hjärtsvikt som inte är kandidater för hjärttransplantation. Målet är att generera kunskap som kan optimera urvalet av patienter, förbättra behandlingsresultaten och minska komplikationerna. Studien inkluderar även en utvärdering av behandlingens kostnadseffektivitet, och dess resultat kan bana väg för framtida förbättringar av LVAD-teknologin. Trots att evidensen för permanent LVAD-behandling ännu inte är fullständig, har ingen motsvarande studie kunnat genomföras någon annanstans i världen. Detta understryker vikten av SweVAD-studien, som fyller en avgörande kunskapslucka inom området och kan leda till värdefulla insikter för framtida vård och behandling av patienter med avancerad hjärtsvikt.
Rematch-studien, som publicerades 2001 [12], är den enda randomiserade jämförelsen mellan permanent mekaniskt vänsterkammarstöd och optimal medicinsk behandling. Även om den första generationens vänsterkammarpump inte var konstruerad för långtidsbruk så resulterade den pumpen i högre korttidsöverlevnad samt bättre funktionsförmåga och livskvalitet än medicinsk behandling. I jämförelse med dagens evidensbaserade riktlinjer var den medicinska hjärtsviktsbehandlingen i kontrollarmen dock mycket omodern. Endast 24 procent av patienterna stod på betablockerare, och varken CRT eller ICD hade kommit till användning. Hur dagens permanenta vänsterkammarstöd står sig mot modern medicinsk hjärtsviktsbehandling i en åldrad hjärtsviktspopulation med samsjuklighet är således fortfarande en öppen fråga. SweVAD-studien erbjuder en direktjämförelse mellan permanent vänsterkammarstöd och medicinsk behandling avseende överlevnad, funktionsförmåga, livskvalitet och komplikationsfrekvens. Samtidigt kommer en noggrann hälsoekonomisk utvärdering av behandlingsmetoden att genomföras. Studien kommer således att ge betydande kunskapsvinster samt ett starkt vetenskapligt underlag för behandlingsbeslut vid svår hjärtsvikt.
I SweVAD-studien, som i många andra prospektivt randomiserade studier, har det visat sig vara en utmaning att identifiera lämpliga patienter, varför rekryteringstakten har blivit lägre än vi hade hoppats på. Inte bara breddinförande av nya hjärtsviktsmediciner (sakubitril/valsartan och SGLT2-hämmare) och covid-19-pandemin (2020–2022) har haft betydelse för studiens långsamma rekrytering, utan även andra faktorer. Efter insatt behandling förblir många hjärtsviktspatienter stabila i NYHA-funktionsklass II–IIIa och uppfyller därmed inte inklusionskriterierna eftersom de är för friska. När en försämring inträffar, till exempel i samband med debut av förmaksflimmer, infektion eller mag–tarmblödning, kan det gå raskt utför och patienten kan inom kort utveckla multiorgansvikt, vilket då också utgör ett hinder för att delta i studien.
I dessa tider kan det vara svårt att hitta vårdplatser för att utreda hjärtsviktsgrad och bedöma prognos. Detta leder till att många patienter inte hinner utvärderas för studien, eftersom tidsfönstret från att patienten bedöms lämplig för deltagande tills hen har blivit för dålig är mycket kort. Flera patienter som vid screening verkat lämpliga för studien har snabbt försämrats och avlidit innan de kunnat inkluderas.
För att kunna identifiera lämpliga studiekandidater är det angeläget att noga följa sjukdomsförloppet och återkommande skatta prognosen. Detta görs enklast med tät klinisk uppföljning, gärna på hjärtsjuksköterskemottagningar, med riktade kontroller av NT-proBNP och analyser av elektrolyter, kreatinin och leverstatus för att kunna värdera graden av sekundär organpåverkan. Det är viktigt att fånga aktuella försämringar hos hjärtsviktspatienterna, eftersom detta indikerar att de kan befinna sig inom det terapeutiska fönstret. Återkommande vätskeretention, tilltagande högerkammarsvikt, intolerans mot hjärtsviktsbehandling, upprepade sjukhusinläggningar och behov av inotrop behandling (inklusive intermittent levosimendaninfusion) är exempel på händelser som predicerar ogynnsam prognos och indikerar lämplighet för deltagande. Nu är vi i slutfasen av SweVAD-studien, men behöver hjälp med att identifiera patienter som är intresserade av att delta. Vi uppmanar därför alla som har hand om patienter med svår hjärtsvikt att ha SweVAD-studien i åtanke och kontakta studieansvarig kardiolog/sjuksköterska på respektive universitetssjukhus om en tänkbar kandidat uppenbarar sig.
Artikelförfattarna, de akademiskt aktiva personerna i studien, är några av alla SweVAD-prövare. Tina Wolmeryd, projektledare i studien, har tillsammans med FoU-sjuksköterskor sett till att studien kan genomföras praktiskt. Många chefer har stöttat projektet moraliskt, praktiskt och finansiellt. Företaget Abbott (före detta St Jude och före detta Thoratec Inc), som producerar pumpen, har stöttat projektet. Studien är finansierad av Vetenskapsrådet, Hjärt–lungfonden, företag och regioner.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.