»Aktiv hälsostyrning« är ett icke-medicinskt och i huvudsak telefonbaserat patientstöd som syftar till att förbättra omhändertagandet och resursutnyttjandet för utsatta patientgrupper.
Genom att tidigt identifiera just de patienter som löper hög risk för undvikbar slutenvård, kan stödet riktas till dem med störst behov och nytta av kompletterande stöd. Särskilt utbildade sjuksköterskor, s k vårdcoacher/vårdlotsar, genomför interventionen.
För att utvärdera modellen för aktiv hälsostyrning har vi genomfört en serie randomiserade kontrollerade studier i fem landsting. Över 12 000 patienter har inkluderats sedan 2010.
Våra resultat visar att aktiv hälsostyrning kan leda till minskad sjukvårdskonsumtion och minskade kostnader för hälso- och sjukvården.
Samhällets kostnader för hälso- och sjukvård ökar trots kontinuerligt effektiviseringsarbete. Av naturliga skäl är en stor del av kostnaderna koncentrerade till en liten del av befolkningen. Till exempel står 10 procent av befolkningen i Stockholms läns landsting för ca 80 procent av de totala hälso- och sjukvårdskostnaderna [1].
Som följd har en rad modeller utvecklats internationellt för att bättre möta de mest utsatta patienternas behov. Två av dessa modeller, vård- och stödsamordning (case management) och sjukdomshantering (disease management), syftar till att framför allt minska patienternas behov av dyr akutsjukvård genom att dels stärka patientens egen förmåga att hantera sin situation, dels förbättra samordningen av vård- och omsorgsinsatser för patienterna [2, 3]. Dessa modeller har visat positiva effekter på såväl kliniska som sociala utfallsmått [4].
Med detta som bakgrund har vi nu utformat en svensk anpassning av dessa modeller för riktad intervention till patienter med förväntat stora behov av undvikbar slutenvård. Vi i författargruppen har valt benämningen »aktiv hälsostyrning«, vilken innefattar telefonbaserat stöd av specialutbildad sjuksköterska.
Syftet med denna studie var att i en serie randomiserade kontrollerade studier i fem landsting utvärdera effekterna av modellen med avseende på sjukvårdskonsumtion. Resultat från pilotfasen av interventionen har publicerats tidigare [5].
Metod
Modellen aktiv hälsostyrning
Aktiv hälsostyrning är en svensk anpassning av de internationellt utvecklade och använda modellerna »case management« och »disease management« och innefattar [5]
- systematisk och tidig identifiering av patienter som löper hög risk för undvikbar slutenvård
- framtagande och genomförande av individuellt anpassade åtgärdsplaner som syftar till att förbättra patienternas hälsa och därigenom förebygga vårdbehov
- proaktiv och nära kontakt mellan patienter och vårdgivare genom telefonsamtal och/eller besök
- kontinuerlig monitorering av patienternas aktuella risk och uppföljning av deras medicinska status, vårdkonsumtionsmönster och livskvalitet [5].
Aktiv hälsostyrning är ett komplement till patientens befintliga vård och omsorg och ges endast under den tid patientens vårdbehov är förebyggbart.
Konceptet aktiv hälsostyrning har utvecklats av företaget Health Navigator AB i samarbete med de landsting där modellen har implementerats. Det övergripande syftet med arbetet har varit att förbättra omhändertagandet och resursutnyttjandet för särskilt utsatta patientgrupper samt att stärka patienternas involvering och ställning i vården och därigenom förbättra deras vård och livskvalitet.
Arbetet med aktiv hälsostyrning bedrivs i två steg:
- Det första steget är regelbunden systematisk identifiering av patienter med hög risk för akuta öppenvårdsbesök och akuta inläggningar. De patienter som bedöms vara i behov av extra stöd och potentiellt hjälpta av den utarbetade interventionen erbjuds denna.
- I det andra steget utför de särskilt utbildade sjuksköterskorna, benämnda »vårdcoacher« eller »vårdlotsar«, en riktad, huvudsakligen telefonbaserad intervention bestående av dels individanpassat, coachliknande stöd, dels koordinering av vård- och omsorgskontakter.
Studiedesign och patientpopulation
Modellen har i dagsläget prövats i fem landsting. I denna rapport inkluderas dock endast data från tre av landstingen – Stockholms läns landsting, Västra Götalandsregionen och Landstinget i Uppsala län. Övriga landsting inkluderas inte på grund av ofullständiga uppföljningsdata (Östergötland) eller för liten studiepopulation (Sörmland).
Samtliga patienter med ≥3 besök på akutmottagning under föregående halvår screenades för inklusion i studien. Exklusionskriterier var demenssjukdom, kraftig hörselnedsättning och/eller psykossjukdom samt palliativt tillstånd. Med hjälp av standardiserade kriterier identifierades därefter patienter med högst risk för framtida potentiellt undvikbar sjukvårdskonsumtion.
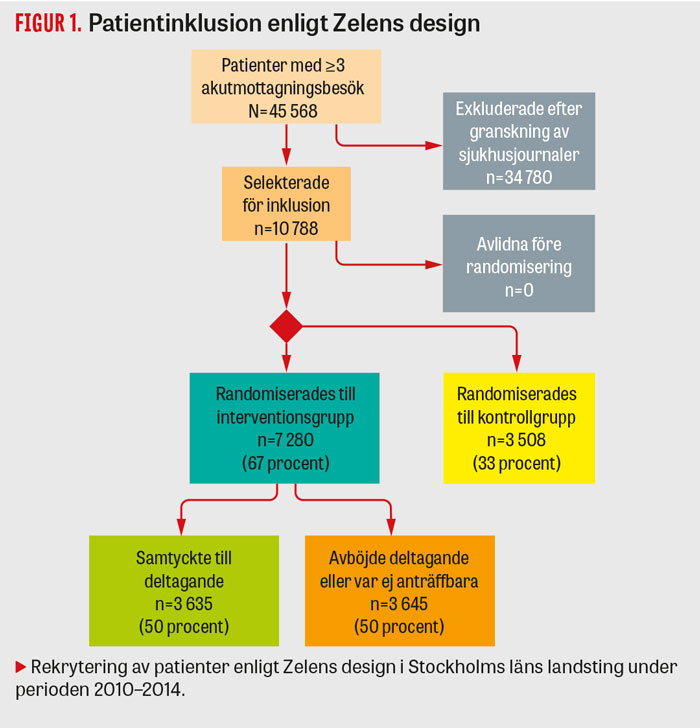
Selekterade patienter inkluderades och randomiserades sedan enligt två olika studieupplägg. I Stockholm inkluderades och randomiserades patienterna enligt Zelens design [6], där randomisering till interventions- eller kontrollgrupp sker innan samtycke inhämtats. De som randomiserats till interventionsgruppen tillfrågades sedan om deltagande, medan kontrollgruppen, liksom i en vanlig registerstudie, följdes passivt utan att samtycke inhämtades. Denna design valdes primärt för att undvika en möjlig Hawthorne-effekt [7].
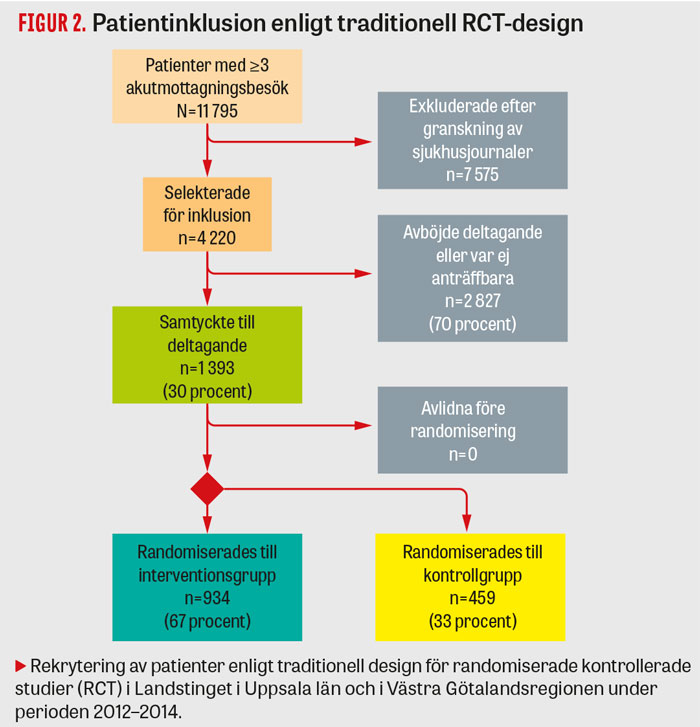
I Västra Götaland och Uppsala följdes ett klassiskt randomiseringsprotokoll (RCT), där patienter som identifierats för möjligt deltagande tillfrågades om deltagande innan randomisering skedde.
Randomiseringen var oblindad, och i båda grupperna randomiserades patienterna med en förutbestämd fördelning av två deltagarpatienter per kontrollpatient. Randomiseringen genomfördes utan block med en central slumptalsgenerator som integrerats i det elektroniska studiestödsverktyget.
Intervention
De patienter som randomiserats till intervention inbjöds först till ett möte med en vårdcoach/-lots, där patientens medicinska och sociala bakgrund kartlades genom en strukturerad intervju. Därefter fastställdes en individuell plan, och patienten fick regelbundet telefonstöd enligt ett koncept beskrivet av Reinius et al [5].
Metoden är en lokal anpassning av tidigare beskrivna modeller för vård- och stödsamordning och sjukdomshantering. I korthet innebär metoden att vårdcoacherna/-lotsarna regelbundet har kontakt med patienterna och, utifrån den personliga planen, identifierar problem i patientens medicinska och sociala situation för att genom vägledning och motiverande samtal försöka hjälpa patienten att komma tillrätta med dessa problem. Inga rent medicinska råd gavs vid telefonkontakterna, men en vanlig del av stödet var att hjälpa patienterna med kontakter med den vanliga vården.
Regelbunden monitorering och uppföljning av interventionens effekt genomfördes under studiens gång med syfte att ge varje vårdcoach/-lots återkoppling för att successivt förbättra genomförandet.
Resultaten från monitoreringen och uppföljningen användes även till att utveckla såväl patientselektionsprocessen som interventionen under studiens gång. Denna adaptiva modell resulterade i en gradvis utveckling av interventionen, från en första enkel modell med icke-centraliserad screening av patienter till en standardiserad, delvis automatiserad screeningmodell med ett standardiserat och elektroniskt system- och beslutsstöd till vårdcoacherna/-lotsarna och med kontinuerlig uppföljning.
Utfallsmått
De primära undersökningsvariablerna var antal sjukhusinläggningar och antal läkarbesök i primärvården. Som sekundära utfallsmått valdes kostnad för hälso- och sjukvård, antal akutmottagningsbesök och mortalitet.
Uppföljning och statistisk analys
Patienterna följdes från randomiseringsdatum fram till sista uppföljningsdatum (31 mars 2014) eller i max 2 år. Uppgifter för slutenvårdstillfällen (inskrivnings- och utskrivningsdatum, vårdtid och vårdkostnad samt utskrivningsdiagnoser) och läkarbesök i primärvården (med datum och kostnad) hämtades ur respektive landstings/regions eller vårdgivares vårddatalager.
För att beräkna skillnader i bakgrundsdata för patienterna användes Wilcoxons test (kontinuerliga variabler) och χ2-test (kategoriska variabler). Relativ risk för vårdkonsumtion, uttryckt som incidenskvoter, där patienterna som randomiserats till deltagargruppen jämfördes med kontrollgruppen, beräknades med negativ binomial regression. Antal dagar med sjukhusinläggning jämfördes med Wilcoxons test; på grund av uttalat skeva fördelningar analyserades skillnader i vårdkostnader med »bootstrap«-test. Analyserna har gjorts enligt »intention to treat«, dvs patienterna studerades så som de randomiserats.
Eftersom såväl patienturvalet som interventionen förändrades kontinuerligt under studieperioden allteftersom erfarenhetsbasen både bland vårdcoacherna/-lotsarna och inom studiegruppen byggdes upp, gjorde vi också post hoc-analyser stratifierade på årtal för randomisering.
Samtliga delstudier som utvärderar aktiv hälsostyrning är godkända av respektive regional etikprövningsnämnd (Stockholm: 2010/976-31/4 och 2011/1391-31/3; Göteborg: 033-12; och Uppsala: 2012/449).
Resultat
Studiepopulation
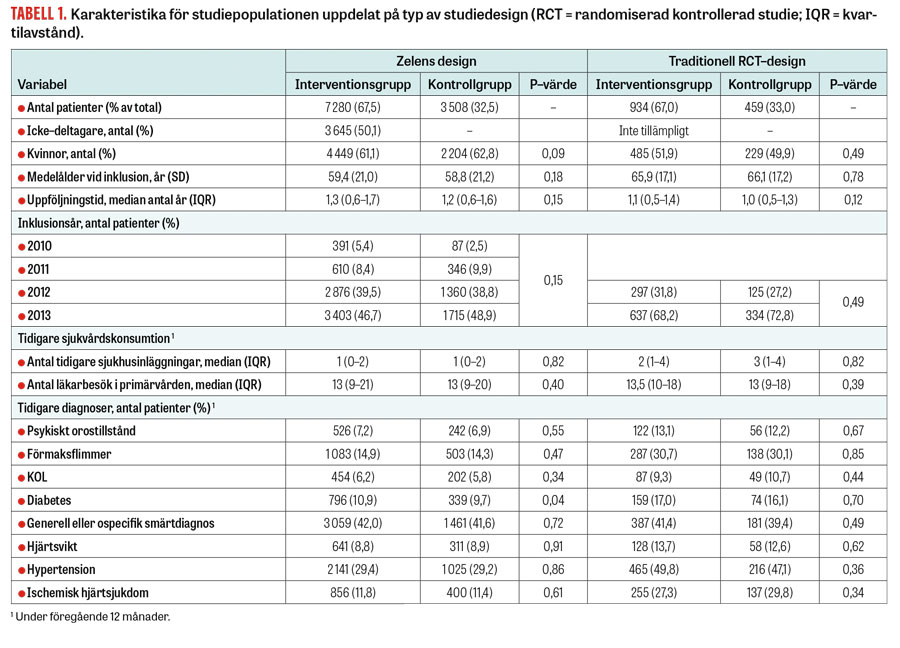
Figur 1 och 2 beskriver inklusions- och randomiseringsprocesserna för respektive studiedesign. I Stockholm, där Zelens design användes, randomiserades totalt 10 788 patienter, varav 7 280 (67 procent) till att erbjudas intervention och 3 508 (33 procent) till kontrollgrupp. Av de patienter som erbjöds intervention tackade 3 635 (50 procent) ja till att delta och inkluderades. I Västra Götaland och Uppsala, där man följde en traditionell randomiserad design, inkluderades och randomiserades totalt 1 393 patienter, varav 934 (67 procent) randomiserades till interventionsgruppen. Tabell 1 presenterar sammanslagna bakgrundsdata för de 12 181 randomiserade patienterna.
Vi såg inga statistiskt signifikanta skillnader mellan interventions- och kontrollgrupperna avseende ålder, kön eller vårdkonsumtion 6 månader före randomiseringen.
Resultat för hela tidsperioden
I studien med Zelens design sågs totalt sett ingen statistiskt signifikant skillnad mellan interventions- och kontrollgrupperna i antal sjukhusinläggningar (incidenskvot: 0,99; 95 procents konfidensintervall [KI]: 0,95–1,02). I studien med RCT-design minskade risken för sjukhusinläggning med 12 procent för interventionsgruppen jämfört med kontrollgruppen (incidenskvot: 0,88; 95 procents KI: 0,81–0,96). Ökat antal läkarbesök i primärvården observerades för interventionsgrupperna för båda studiedesignerna med incidenskvot 1,05 (95 procents KI: 1,04–1,06) för Zelens design respektive 1,05 (95 procents KI 1,01–1,08) för traditionell RCT-design. Vi såg ingen skillnad vad gäller vare sig sjukvårdskostnader eller antal dagar för sjukhusinläggning mellan interventions- och kontrollgrupperna i någon av de två studiemodellerna.
Resultat uppdelade på år för inklusion
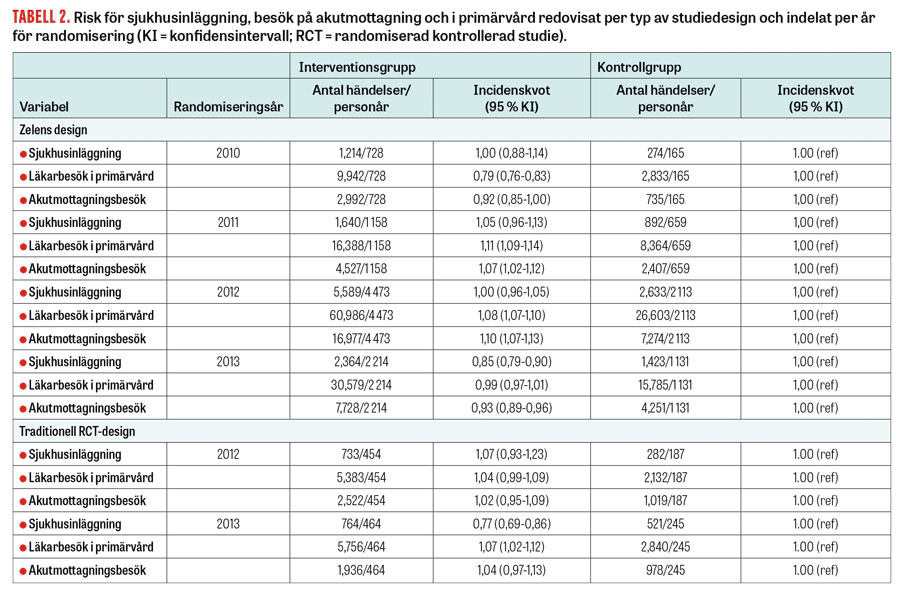
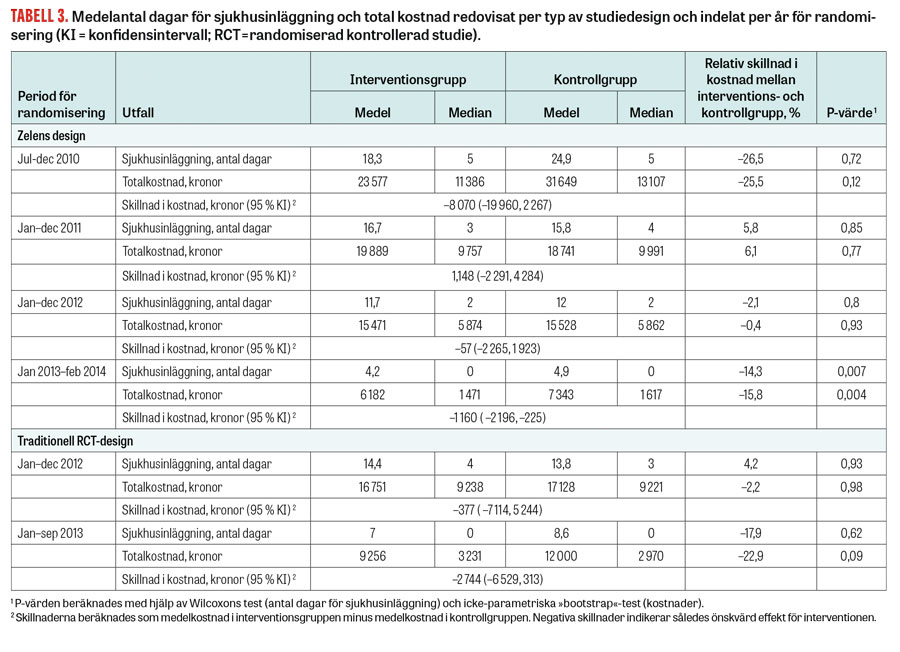
Eftersom ändringar gjordes kontinuerligt i arbetssättet under studiens gång, redovisas även resultaten uppdelade på år för inkludering i studien. Test för heterogenitet visar att effekten av interventionen varierade över tid för de primära utfallsvariablerna (P < 0,001), Tabell 2. I Stockholm, där Zelens design följdes, sågs en minskning av såväl antal läkarbesök i primärvården som antal akutmottagningsbesök för de patienter som inkluderades och randomiserades till interventionsgrupp under det första året (2010), medan en ökning sågs i samma utfallsvariabler för de interventionsgruppspatienter som inkluderades under 2011 och 2012.
För de patienter som inkluderades under 2013 sågs en minskning i antalet sjukhusinläggningar och i antalet akutmottagningsbesök. För variablerna sjukvårdskostnader och antal dagar för sjukhusinläggningar sågs skillnader mellan kontroll- och interventionsgrupperna endast för patienter inkluderade under 2013 (där interventionsgruppen hade lägre kostnader och färre inläggningsdagar) (Tabell 3).
I de studier som följde traditionell studiedesign sågs inga skillnader mellan kontroll- och interventionsgrupperna för de patienter som inkluderades under 2012, medan det för de patienter som inkluderades under 2013 sågs en 23-procentig minskning i antal inläggningar jämfört med kontrollgruppen.
Inga skillnader i mortalitet sågs mellan interventionsgruppen och kontrollgruppen, varken i Stockholm (relativ risk för död: 0,90; 95 procents KI: 0,76–1,06) eller i RCT-studierna (relativ risk för död: 1,02; 95 procents KI: 0,62–1,67).
Diskussion
Vi presenterar här resultat från en sammanlagd analys av en serie randomiserade kontrollerade studier, inkluderande totalt drygt 12 000 patienter, där effekterna av en successivt utvecklad modell för aktiv hälsostyrning har studerats. Det minskade antalet sjukhusinläggningar i delstudien med traditionell RCT-design och det minskade antalet sjukhusinläggningar och akutmottagningsbesök under det sista studieåret i delstudien med Zelens design för interventionsgruppen visar att implementering av den här typen av intervention kan leda till minskad sjukvårdskonsumtion för patienter med risk för hög undvikbar slutenvårdskonsumtion. Samtidigt tydliggör de varierande resultaten, där vi sett både positiva och negativa effekter av interventionen, svårigheterna att uppnå varaktigt positiva effekter.
Både minskad och ökad vårdkonsumtion
Resultaten från tidigare studier av effekter av case management och disease management på sjukvårdskonsumtion är blandade, och vissa studier har till och med uppvisat ökad mortalitet i interventionsgruppen [4, 8-10].
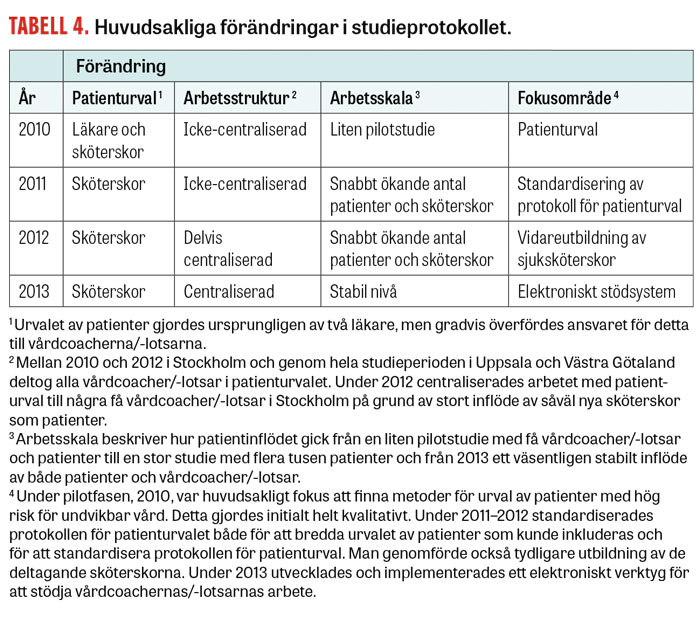
Vi valde att arbeta med ett helt telefonbaserat, icke-medicinskt stöd, vilket skiljer sig från flertalet tidigare studier. Vidare är denna studie unik i det att den är den största i sitt slag, men också i att interventionen – vad gäller patientinklusion och själva interventionen – har utvecklats och förändrats kontinuerligt under studietiden (Tabell 4). Det är därmed viktigt att tolka resultaten mot bakgrund av denna arbetsmodell. Det är också svårt att direkt jämföra våra resultat med tidigare resultat.
I Stockholms läns landsting observerades till en början (2010) en positiv effekt med minskat antal besök i såväl primärvård som vid akutmottagningar i interventionsgruppen. Under 2011–2012, då studien expanderade snabbt med nyanställning av fler vårdcoacher/-lotsar och ett stort inflöde av patienter, noterades i stället ökad vårdkonsumtion. Efter ytterligare anpassning av patienturvalet och arbetssättet sågs slutligen minskad vårdkonsumtion hos dem som ingick i interventionsgruppen.
Begränsningar i studien
Studien har ett antal begränsningar. I en modell med Zelens studiedesign inkluderas samtliga patienter som randomiserats till interventionsgruppen. Följaktligen analyseras även de som erbjudits men avböjt interventionen som interventionsgruppspatienter. I vårt fall valde knappt hälften av patienterna som blivit randomiserade till interventionsgruppen att inte delta eller så gick de inte att nå. En vanlig orsak till att inte vilja delta visade sig vara att man ansåg sig vara för sjuk, vilket talar för en stark koppling mellan icke-deltagande och vårdbehov.
Bortfallet kan kanske ses som en indikation om bristande träffsäkerhet i patientidentifieringen. Bortfallet orsakade troligen en underskattning av interventionens effekt och därmed en kraftig minskning av studiens statistiska styrka. Detta illustrerar en tydlig svaghet med Zelens design, som annars har fördelen att den är en förhållandevis effektiv, pragmatisk studiedesign, som dessutom genererar mer generaliserbara resultat än traditionellt randomiserade studier, där uppmätta behandlingseffekter kan vara svåra att reproducera i verkligheten.
Vidare, eftersom en stor del av patienturvalsprocessen skedde med ett kvalitativt tillvägagångssätt, var det en utmaning att tillförlitligt identifiera patienter med hög och undvikbar hälso- och sjukvårdskonsumtion. Denna process skulle sannolikt underlättas om en större del av selektionen var baserad på kvantitativa mått, framtagna utifrån prediktionsmodeller.
Stor utmaning nå varaktigt positiva effekter
Vår erfarenhet är att det är förknippat med stora utmaningar att uppnå varaktigt positiva effekter med modeller för vård- och stödsamordning och sjukdomshantering. Det är bl a komplext att korrekt och i tid identifiera personer som har hög och förebyggbar risk för akut, oplanerad vård. Därtill bör man beakta en hög patientomsättning i målgruppen, där de som konsumerar mest undvikbar akutvård under 1 år återfinns i begränsad omfattning i samma grupp nästa år.
Baserat på våra kvalitativa erfarenheter från det iterativa utvecklingsarbetet bedömer vi att de viktigaste framgångsfaktorerna under arbetet varit
- en i mesta möjliga mån standardiserad och korrekt riskbedömning så att rätt patienter identifieras i rätt tid
- den standardiserade metodiken och beslutsstöden för utförandet av interventionen
- den kontinuerliga utvärderingen, som hela tiden återrapporteras till vårdcoacherna/-lotsarna, som därmed kan anpassa interventionen.
Alla dessa tre faktorer bör vara samstämmiga för att säkra effekter i storskaligt genomförande.
Sammanfattningsvis visar denna studie att det är möjligt att utforma en telefonbaserad intervention som potentiellt kan leda till minskad sjukvårdskonsumtion för patienter med täta sjukvårdskontakter.
Potentiella bindningar eller jävsförhållanden: Gustaf Edgren har mottagit konsultarvode från Health Navigator AB för rådgivning rörande studiedesign och statistiska analyser. Joachim Werr är vd för Health Navigator, som bistått i utvecklingen.
Studien är finansierad av Stockholms läns landsting, Landstinget i Uppsala län, Västra Götalandsregionen, Landstinget Sörmland och Landstinget i Östergötland.