Denna artikel beskriver det svenska njurbytesprogrammet Step och redogör för de första svenska njurbytena inom ramen för programmet.
Sex operationer i ett trepartsbyte utfördes parallellt på svenska sjukhus och brådskande transporter av njurarna genomfördes mellan enheterna.
Samtliga donationer och transplantationer kunde genomföras som planerat.
Två månader efter transplantationerna har samtliga tre mottagare bra och stabil njurfunktion.
Två månader efter operationerna har samtliga tre donatorer återhämtat sig.
Avslutningsvis beskrivs fyra nyckelproblem som måste lösas för att full potential ska kunna uppnås inom Step. Dessa rör informationskampanjer, skandinavisk utvidgning, ABO-inkompatibla transplantationers roll och mer avancerade matchningstekniker.
Njurtransplantation är vanligen den bästa behandlingen vid terminal njursvikt, och jämfört med dialys leder njurtransplantation ofta till bättre patientöverlevnad och bättre livskvalitet [1]. Njurtransplantation är också billigare än dialys och innebär stora samhällsekonomiska besparingar i form av minskade sjukvårdskostnader [2]. Vid transplantation kan njuren komma från en avliden eller levande donator. Även om det finns en möjlig levande njurdonator – exempelvis i form av en släkting eller nära vän – är det inte säkert att en donation och transplantation kan genomföras på grund av olika medicinska och immunologiska hinder. Den i dag vanligaste immunologiska orsaken till att en närståendes vilja att donera inte kan tillvaratas är förekomst av antikroppar hos mottagaren riktade mot donatorns vävnadstyp (HLA). En följd av detta är att inte alla potentiella levande donatorer kan användas och att fler patienter måste hänvisas till väntelista för njurtransplantation från avlidna donatorer. Då tillgången på njurar från avlidna donatorer inte är tillräcklig medför denna brist ofta långa väntetider. I dag står ca 650 personer på en sådan väntelista i Sverige.
Det finns flera goda anledningar till att njurar från levande donatorer bör användas i så stor utsträckning som möjligt. Det är klart visat att transplantation med njurar från levande njurdonatorer oftast är något bättre (till exempel vad gäller patient- och transplantatöverlevnad) än transplantation med njurar från avlidna donatorer [3]. Vidare innebär levande njurdonatorer att väntelistan indirekt blir kortare och att njurar från avlidna donatorer främst går till patienter som inte har en möjlig levande donator. Det är också betydelsefullt att de individer som vill, och även bedöms vara medicinskt lämpliga, erbjuds möjlighet att hjälpa närstående genom att donera en njure.
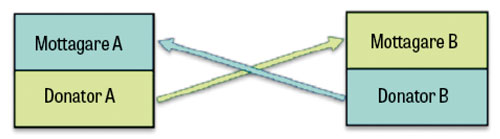
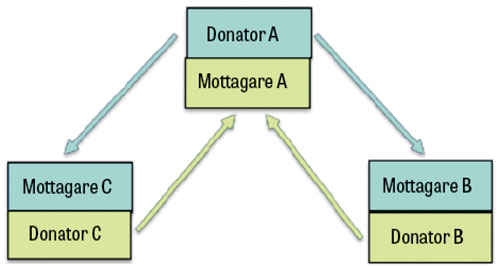
Även om det i dag finns tillgång till metoder för att i vissa fall avlägsna en del av de immunologiska hinder som föreligger vid transplantation återstår det faktum att inte alla njursjuka patienter med en möjlig levande donator kan transplanteras som tänkt. En lösning på detta problem är att skapa ett så kallat njurbytesprogram. Det första programmet där njurbyten identifierades med en algoritm, och där flera centrum deltog, startades i New England år 2004 [4], och idén har sedan dess framgångsrikt använts i bland annat 10 europeiska länder [5]. Grunden i ett njurbytesprogram är att skapa en databas som innehåller par av donator–mottagare där immunologisk inkompatibilitet föreligger. Dessa par kan sedan »byta« donatorer med varandra för att kringgå inkompatibilitetsproblemet. Anta till exempel att mottagaren i par A är immunologiskt inkompatibel med sin egen donator A, men fullt kompatibel med donatorn i paret B. Om mottagaren i par B visar sig vara immunologiskt kompatibel med donatorn i par A kan ett tvåpartsbyte genomföras (Figur 1). På motsvarande sätt kan större bytescykler med fler ingående par genomföras. I Figur 2 illustreras ett trepartsbyte där tre par av donator–mottagare ingår.
En given databas kan innehålla ett flertal möjliga byten, och alla möjliga byten identifieras med hjälp av en matematisk algoritm. Ett problem som kan uppstå är att en del byten är ömsesidigt uteslutande då varje deltagande par maximalt kan ingå i ett byte var. Om exempelvis mottagaren i par A kan ta emot njuren från donatorn i både par B och C samtidigt som patienterna i par B och C endast kan ta emot njuren från donatorn i par A existerar det två möjliga tvåpartsbyten (Figur 3). Par A kan alltså ingå i båda dessa byten, och därför måste det finnas ett regelverk som bestämmer exakt vilket av dessa två byten som ska genomföras. Ett njurbytesprogram består alltså lite förenklat av en databas med par av donator–mottagare, en specialdesignad matematisk algoritm som identifierar alla möjliga byten samt ett regelverk som väljer ut och föreslår njurbyten.
Metod och resultat
Det svenska njurbytesprogrammet Step (Scandiatransplant kidney exchange program) är i dag ett samarbete mellan landets fyra njurtransplantationsenheter (Skånes universitetssjukhus, Sahlgrenska universitetssjukhuset, Karolinska universitetssjukhuset och Akademiska sjukhuset) och nationalekonomiska institutionen vid Lunds universitet. Programmet har som övergripande mål att maximera antalet transplantationer, prioritera kraftigt immuniserade patienter (patienter med höga nivåer av anti-HLA-antikroppar, som alltså har svårt att hitta en lämplig donator) och minimera antal transplantationer över blodgruppsbarriären [6-7]. Algoritmen utesluter dock inte ABO-inkompatibla njurbyten. Utredning av donatorer och mottagare sker på landets njurmedicinska enheter, övrig handläggning och koordinering sker vid landets njurtransplantationsenheter. Deltagande i njurbytesprogrammet är helt frivilligt och sker helt anonymt och under sekretess. Inga uppgifter om andra deltagande par lämnas vidare. Då systemet att transportera organ är säkert och väl etablerat opereras donatorer och mottagare lokalt på ansvarig transplantationsenhet, och njurar skickas sedan mellan enheterna. Studier har visat att detta kan göras utan negativa effekter på resultatet så länge transporttiderna hålls korta [8-9]. Donatorer och mottagare vårdas och följs sedan på den enhet där de opererats.
Nyligen genomfördes framgångsrikt de första transplantationerna i det svenska njurbytesprogrammet, då tre patienter transplanterades samma dag med njurar från tre levande anonyma donatorer. Samtliga sex operationer utfördes parallellt på svenska sjukhus, och brådskande transporter av njurarna mellan enheterna genomfördes (Figur 2). Såväl donationer som transplantationer kunde utföras som planerat och alla transporter fungerade utan problem. Alla donatornefrektomier genomfördes med minimalinvasiv, laparoskopisk teknik [9]. Den kalla ischemitiden (den tid som njuren inte har blodcirkulation utan förvaras kallt i särskild preservationslösning) var 1, 6,5 och 7 timmar. En av njurdonatorerna drabbades av en postoperativ venös blödning i operationsområdet som dock kunde hanteras med interventionell angiografi, och denna komplikation förlängde sannolikt vårdtiden med något dygn och försvårade donatorns återhämtning. Vårdtiden för de tre donatorerna var 4 dygn, 6 dygn och 5 dygn, vilket är jämförbart med vårdtiden för andra levande njurdonatorer. En mottagare med aktiverad protein C-resistens (i homozygot form) och förstärkt koagulationsprofylax reopererades på grund av en diffus blödning i operationsområdet och den blodförtunnande behandlingen minskades. Vårdtiden för mottagarna var mellan 6 och 10 dygn. Två månader efter transplantationerna hade samtliga mottagare bra och stabil njurfunktion (P-kreatinin 91, 121 respektive 120 mikromol/l, eGFR 61, 50 respektive 56 ml/min/1,7 m2). En av mottagarna vårdades efter transplantationen inneliggande på grund av infektioner och behandlades med bland annat bredspektrumantibiotika intravenöst. Samtliga donatorer har sedan återhämtat sig fullt, och den postoperativa uppföljningen har varit utan vidare anmärkning. Det postoperativa förloppet för såväl donatorer som mottagare i det aktuella trepartsbytet har inte varit uppenbart annorlunda än vid sedvanlig njurtransplantation med levande donator.
Diskussion
Att de första tre donationerna och transplantationerna inom ramen för njurbytesprogrammet Step kunde genomföras kan betraktas som en stor framgång. Exempelvis kräver ett njurbytesprogram att olika enheter enas om viktiga medicinska, immunologiska och logistiska principer. Vidare krävs att olika typer av mjukvara utvecklas och implementeras vid de olika enheterna. Även om inget av detta hade varit möjligt att uppnå utan ett stort engagemang från all personal vid de deltagande enheterna återstår mycket arbete innan programmet har uppnått full potential. I en sådan situation är vår förhoppning att 20–30 transplantationer ska kunna utföras årligen i Sverige inom ramen för Step, men exakta beräkningar är svåra att göra. För att nå ett sådant mål måste ett antal åtgärder vidtas. De viktigaste av dessa är:
- Sverige är för litet för att ensamt kunna driva ett effektivt njurbytesprogram. Databasen med ingående par av donator–mottagare är för liten, och större databaser leder alltid till proportionerligt fler njurbyten. Det är därför betydelsefullt att den initiala planen följs och driften av njurbytesprogrammet överförs till den skandinaviska samarbetsorganisationen för organtransplantationer, Scandiatransplant, under 2019. Detta innebär att även inkompatibla par från Norge, Danmark, Finland och Island kan inkluderas, vilket i sin tur innebär att storleken på databasen ökar, fler levande njurdonatorer kan tas till vara och fler njurtransplantationer kan genomföras. Step kommer då att vara ett av de första njurbytesprogrammen där njurbyten sker mellan olika länder.
- Det är viktigt att information om Step sprids så att fler inkompatibla par av donator–mottagare i Sverige får vetskap om denna nya möjlighet och kan inkluderas. I detta informationsarbete har alla som på något sätt arbetar med njurtransplantationsverksamhet i Sverige en viktig roll att spela. Vi hoppas att intresseorganisationer som MOD (Mera organdonation) och Njurförbundet kommer att delta aktivt i informationskampanjer för att öka medvetenheten om Step. Att stödja transplantation med njure från levande donator i allmänhet är också betydelsefullt.
- I dag kan patienter transplanteras med njure från levande donator över blodgruppsbarriären, det vill säga även då ABO-inkompatibilitet föreligger, men detta kräver särskild förbehandling av mottagaren, vilket är kostsamt och resurskrävande för vårdgivaren. Ett alternativ vore att på ett systematiskt sätt inkludera även ABO-inkompatibla par av donator–mottagare i njurbytesprogrammet. Utöver det faktum att dessa ABO-inkompatibla mottagare kan undvika en potentiellt riskabel förbehandling så kan den algoritm som används i Step även programmeras så att dessa patienter kan få en »bättre« njure – exempelvis njure från yngre donator eller med gynnsam HLA-typ – samtidigt som den ökar möjligheten för mottagaren i andra inkompatibla par att transplanteras. En möjlighet kunde därför vara att tillfråga patienter med ABO-inkompatibla donatorer om de kan tänka sig att delta i Step under en begränsad tid (till exempel 3–6 månader) med förhoppning att hitta ett mer fördelaktigt njurbyte. Om ett njurbyte inte kan identifieras inom den överenskomna tidsperioden kan den ABO-inkompatibla njurtransplantationen i stället genomföras enligt nuvarande rutin och efter särskild förbehandling.
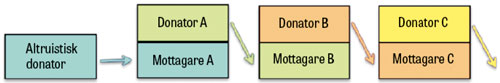
- I det kommande gemensamma skandinaviska programmet kommer algoritmen att leta efter såväl tvåparts- som trepartsbyten samt byteskedjor. En ytterligare framtida utvecklingsmöjlighet är att utnyttja de levande altruistiska donatorer som regelbundet accepteras för att initiera så kallade njurbyteskedjor, där ett större antal par av donator–mottagare kan delta (Figur 4).
Nya metoder måste alltid införas med försiktighet och eftertanke. Ett njurbytesprogram omfattas av samma medicinska och etiska principer som sedvanlig, riktad levande njurdonation och transplantation. Vissa skillnader kan dock tänkas uppkomma, till exempel för donatorn. Njurdonation måste alltid vara helt frivillig, och donatorn får inte på något sätt pressas att donera. Detta framgår mycket tydligt av gällande lagstiftning och etiska regelverk och är något som ligger till grund för dagens kliniska verksamhet inom detta område. Det är samtidigt enkelt att föreställa sig att en levande donator ofta kan uppleva förväntningar från omgivningen och att det kan vara svårt att säga nej till att donera. Ett njurbytesprogram ökar möjligheten för njurdonation och skulle därför kunna upplevas som en ökad press. En ytterligare skillnad i ett etiskt perspektiv är att en donator i ett njurbytesprogram hjälper inte bara sin egen närstående utan även andra mottagare och donatorer i programmet. Även detta skulle kunna medföra en ökad press. Det är därför viktigt att de som utreder, bedömer och handlägger njurdonatorer inom ett njurbytesprogram är medvetna om denna problematik och lyhörda för donatorns behov och önskningar. Det är också väsentligt att poängtera den självklara, grundläggande rättigheten för en donator att avbryta donationsprocessen när som helst utan att behöva förklara detta eller motivera sitt handlande. En donator har alltid en möjlighet att dra sig ur, ända fram till sövningen inför operationen. Här finns det ingen skillnad mellan ett njurbytesprogram och sedvanlig, riktad njurdonation.
I det svenska njurbytesprogrammet Step råder sekretess mellan deltagarna. Detta innebär att ingen av donatorerna eller mottagarna får information om de andra deltagarna, till exempel ålder eller kön, i ett njurbyte. Inte heller ges någon information om hur många andra par som är inblandade i ett njurbyte eller på vilket sjukhus dessa opereras. Sammantaget minskar detta risken för att donatorerna ska uppleva en ökad press att donera.
Det är samtidigt också viktigt att notera att en ökad möjlighet till donation av de allra flesta upplevs som något positivt och en extra chans att hjälpa en närstående med allvarlig njursjukdom. Många levande njurdonatorer motiveras också av en sann önskan att göra gott, varför möjligheten att hjälpa andra i samma situation kan tänkas öka känslan av betydelse och den egna vinsten av donationen.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.