Den utlösande faktorn för förmaksflimmer är oftast extraslag/ektopi från lungvener.
Lungvensisolering med radiofrekvens- eller kryoablation (termisk energi) har använts i många år för att eliminera den utlösande faktorn.
Pulsfältablation (pulsed field ablation, PFA) är en icke-termisk energiform som har visat lovande resultat med stor potential att eliminera risken för allvarliga komplikationer associerade med termisk ablation, såsom lungvensstenos, frenikusnervpares och atrioesofageal fistel. Metoden kan även förenkla och effektivisera ablationsproceduren.
100 patienter genomgick lungvensisolering med PFA. Samtliga lungvener kunde identifieras och isolering kunde uppnås utan svårigheter. Inga allvarliga komplikationer inträffade.
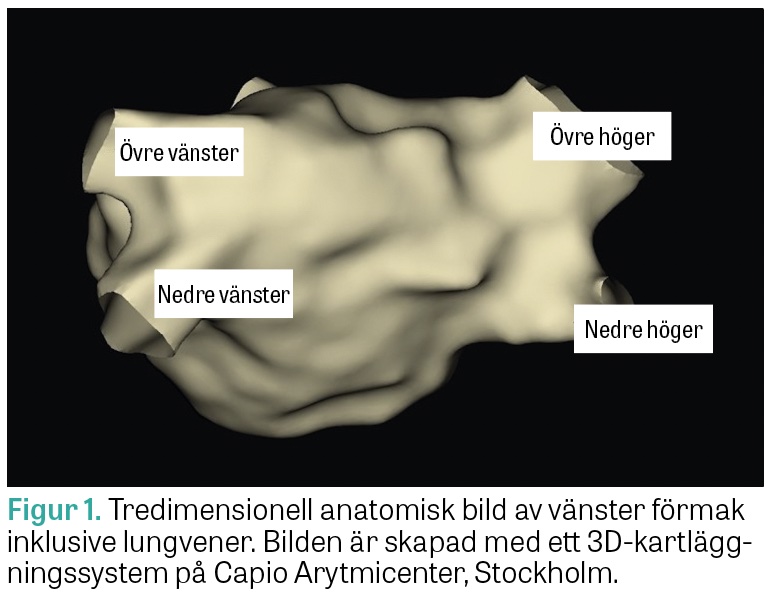
Förmaksflimmer är den vanligaste typen av arytmi och har en prevalens mellan 2 och 4 procent hos vuxna [1]. Denna arytmi är förknippad med sämre livskvalitet [2] och betydligt ökade risker för stroke, hjärtsvikt och för tidig död [3-5]. Antiarytmisk behandling har begränsad profylaktisk effekt och innebär en risk för besvärliga biverkningar. Mekanismen bakom förmaksflimmer var okänd under många år, men i slutet av 1990-talet kunde en forskargrupp från Bordeaux visa att majoriteten av patienter med paroxysmalt förmaksflimmer hade rikligt förekommande supraventrikulära extraslag eller ektopi utgående från områden runt lungvensmynningarna i vänster förmak som utlösande orsak [6]. De flesta människor har 4 separata lungvener som mynnar ut i vänster förmak: 2 till vänster och 2 till höger (Figur 1). Gemensam mynning förekommer hos en minoritet av patienterna. På basen av denna upptäckt introducerades kateterburen ablation vid förmaksflimmer. Syftet med behandlingen var att uppnå elektrisk lungvensisolering genom värme (radiofrekvensablation) eller frysning (kryoablation) [7, 8]. Metoderna har utvecklats genom åren, med en allt bättre långtidseffekt och färre allvarliga komplikationer. Randomiserade studier har visat att ablation är en effektiv metod för att återställa sinusrytmen hos en patientgrupp där antiarytmika inte varit verksamma [9]. Ett problem med dessa energiformer är risken för allvarliga komplikationer i form av lungvensstenos (≤1 procent), frenikusnervpares (upp till 4 procent) och atrioesofageal fistel (<0,1–0,25 procent) [10-12]. Risken för dessa komplikationer är låg, men konsekvenserna kan vara förödande. Forskning om andra typer av energikällor, såsom högintensivt ultraljud eller laser, har pågått i många år. Dessa energiformer har dock sämre effekt och/eller större komplikationer än radiofrekvens- och kryoablation och har därför inte fått något kliniskt genomslag.
Pulsfältablation (pulsed field ablation, PFA) är en icke-termisk teknik som använder ett pulsat elektriskt fält med hög amplitud. Elektriska pulsar med hög amplitud och mycket kort duration destabiliserar cellmembranet i vävnaden genom att orsaka irreversibla och mycket små porer (elektroporation) som leder till läckage av cellinnehåll och så småningom apoptos [13, 14]. Energitröskeln för att framkalla celldöd skiljer sig mellan vävnader och är lägre för förmaksmyokardiet än andra vävnader och organ, såsom nervfibrer, esofagus och blodkärl [15, 16]. Skillnaden i känslighet mellan vävnader kan utnyttjas genom att åstadkomma transmurala lesioner i förmaksmyokardiet samtidigt som närliggande vävnader och strukturer sparas. Under de senaste två åren har PFA börjat användas kliniskt för lungvensisolering med lovande resultat [17-19].
Vi rapporterar vår erfarenhet av denna teknik hos de första 100 patienterna med förmaksflimmer i Sverige.
Metod
PFA-utrustningen består av 3 komponenter (samtliga från Boston Scientific): en generator som levererar högspänningspuls, en 12-F PFA-kateter (Farapulse) som förs in över en ledare med så kallad »over the
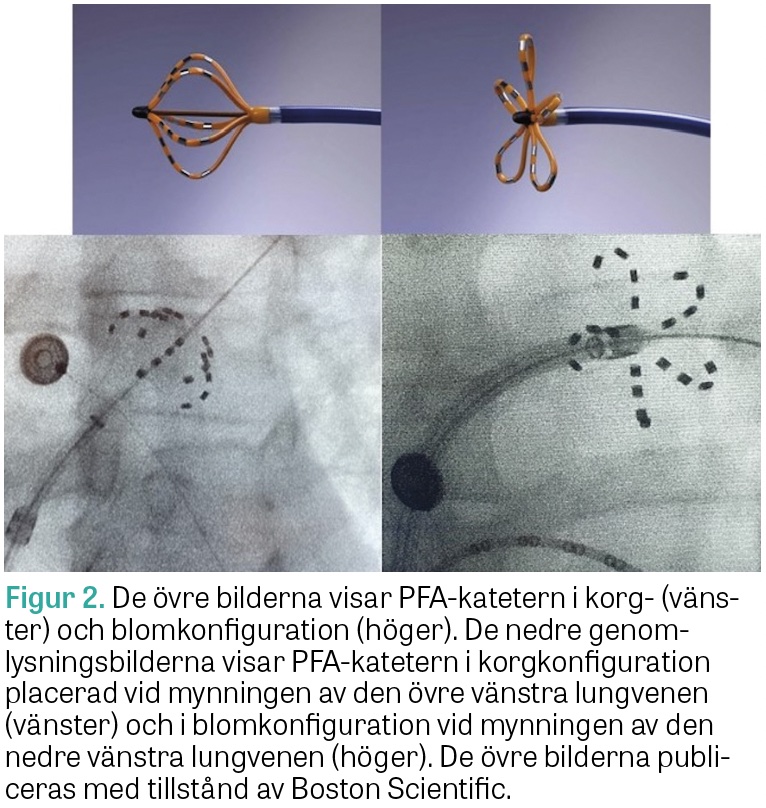
wire«-teknik och en 16-F styrbar införingshylsa (Farawave). PFA-katetern har 5 armar (splines) med 4 elektroder på varje arm. En av elektroderna på varje arm kan registrera elektrogram. Operatören kan med kateterhandtaget forma katetern till en korg- eller blomkonfiguration (Figur 2). Katetern finns i två storlekar beroende på lungvensdiameter. Efter att ledaren förankrats i en lungven förs katetern fram över ledaren och placeras vid mynningen av lungvenen så att samtliga delar i både korg- och blomkonfiguration får kontakt med vävnad runt lungvensmynningen. Ablationsenergin levereras från alla elektroder med 2,5 sekunders duration. Efter två behandlingar roteras katetern så att elektroderna täcker områden mitt emellan elektroderna i den föregående positionen. Sammanlagt 8 behandlingar ges i både korg- och blomkonfiguration under 20 sekunder i varje lungven (Figur 2). Ytterligare behandlingar kan ges enligt operatörens bedömning. Målet är att elektriskt isolera varje lungven. Isoleringen konstateras genom avsaknad av lungvenspotentialer och genom elektrisk stimulering innanför lungvensmynningen som inte överleds ut i vänster förmak. Ytterligare en 10-polig kateter placeras i en kammargren av sinus coronarius, alternativt i högerkammare, och vid eventuell bradykardi/asystoli under pågående behandling kan stimulering utföras med denna.
100 patienter genomgick PFA på Capio Arytmicenter i Stockholm mellan augusti 2022 och februari 2023. Proceduren genomfördes under oavbruten peroral antikoagulantiabehandling. Antiarytmika sattes ut 5 halveringstider före ingreppet. Patienter med ≥1 poäng på CHA2DS2-VASc-skalan och alla med pågående förmaksflimmer oberoende av poäng bedömdes avseende tromb med transesofageal ekokardiografi strax före proceduren. Punktion med transseptal nål (Boston Scientific) och konventionell införingshylsa avsedd för att ge tillgång till vänster förmak (Abbot, SL1) genomfördes i vena femoralis med röntgengenomlysning efter lokal bedövning av höger ljumske. Strax efter punktionen gavs heparin intravenöst (100 E/kg kroppsvikt) och atropin 0,5 mg intravenöst för att förebygga bradykardi/asystoli. Kartläggning av lungvensanatomin erhölls med antingen DT lungvener (utförd före ablationen) och tredimensionell konstruktion av DT-bilderna eller identifiering av lungvener genom placering av sinus coronarius-kateter i varje respektive ven (»roadmapping«) med röntgengenomlysning under proceduren. Vid »roadmapping« sparades genomlysningsbilderna för jämförelse med PFA-kateterns position i varje lungven. Därefter byttes SL-1 till Farawave-införingshylsa. Strax efter tillgång till vänster förmak startades infusion av propofol (3‒6 mg/kg kroppsvikt/timme) för att uppnå djup sedering med spontan andning. Patienterna övervakades med kontinuerligt EKG samt regelbunden blodtrycks- och kontinuerlig saturationsmätning tills de vaknade. 9 patienter hade gemensam lungvensmynning på vänster sida, medan övriga hade 4 separata lungvener. Endast den mindre Farapulse-katetern användes. Vid kvarstående signal i lungvenen gavs ytterligare behandling, varefter isoleringen av lungvener kontrollerades.
Efter avslutad procedur genomgick samtliga patienter översiktlig ekokardiografi för bedömning av eventuellt förekomst av perikardutgjutning. Katetrar och införingshylsor avlägsnades och en sutur i ljumsken lades. Därefter placerades tryckförband (Safeguard). Patienterna fick inta sängläge i cirka 3 timmar under övervakning av hjärtrytm och blodtryck, och därefter påbörjades mobilisering. Beroende på patientens ålder och medicinska tillstånd i övrigt och klockslaget för ablationen skedde utskrivningen samma dag efter cirka 4‒5 timmars observation eller morgonen därpå.
Resultat
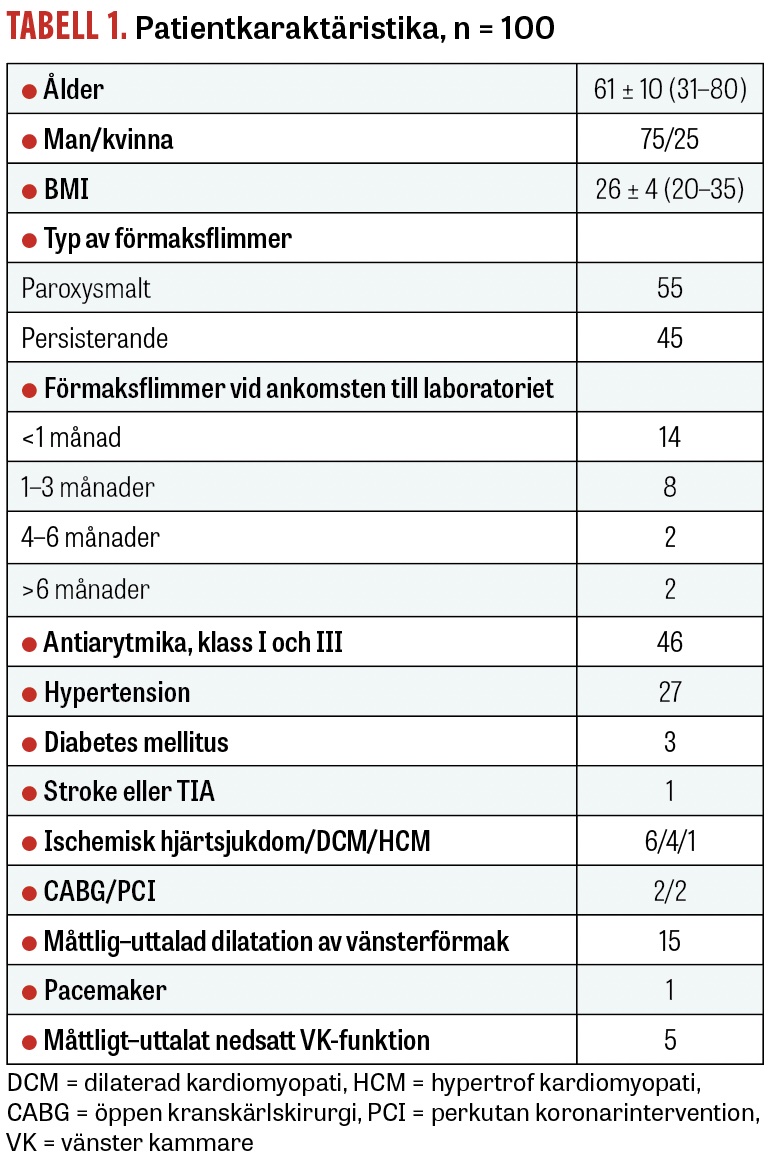
Den kliniska bakgrunden framgår av Tabell 1. Värden anges i medelvärde ± standarddeviation. Ålder var 61 ± 10 år, och 75 procent var män. Paroxysmalt förmaksflimmer förekom hos 55 patienter (55 procent). 26 patienter hade pågående förmaksflimmer vid ankomsten till laboratoriet. Antiarytmika (klass I eller III) hade prövats hos 46 patienter med otillräcklig effekt eller icke-tolerabla biverkningar. BMI var 26 ± 4.
Ablationen genomfördes utan någon komplikation under proceduren. Samtliga lungvener kunde identifieras framgångsrikt hos samtliga patienter, och isoleringen kunde uppnås utan svårigheter. Minst 2 extra behandligar gavs hos 36 patienter. Information om procedurtid och genomlysningsstråldos/-tid framgår av Tabell 2. Redan under de första 20 procedurerna kunde både ingreppstid och genomlysningstid reduceras avsevärt (Figur 3). 97 patienter kunde skrivas ut enligt den ursprungliga planeringen. 60 patienter skrevs ut samma dag som ingreppet.
Komplikationer
En patient (man, 76 år) fick feber och frossa direkt efter avslutat ingrepp. Man misstänkte bakteriemi och behandlade med antibiotika intravenöst i 2 dagar. En patient (man, 50 år) fick andningskorrelerade bröstsmärtor cirka 1 timme efter proceduren. Ekokardiografisk undersökning visade cirka 8 mm perikardutgjutning som inte behövde åtgärdas. Patienten observerades under natten och kunde skrivas ut dagen efter. 2 patienter fick hematom i höger ljumske; en av dessa (kvinna, 80 år) stannade ytterligare en natt för observation. DT-angiografi visade ingen extravasering eller fistelutveckling.
Diskussion
Ablation av förmaksflimmer eller lungvensisolering är en väletablerad och vedertagen invasiv behandlingsmetod. PFA är en teknik som nyligen har introducerats för kateterburen ablation av förmaksflimmer. Som första centrum i Sverige har vi utfört PFA mot förmaksflimmer på 100 patienter med goda akuta resultat utan någon allvarlig komplikation. Detta talar för att metoden är säker. Dessutom är långtidseffekten av PFA jämförbar med de etablerade teknikerna för lungvensisolering [17-20]. Det finns flera fördelar med PFA. Publicerade djurförsöksstudier [15, 16] har påvisat att PFA är vävnadsspecifik, vilket innebär att endast förmaksvävnaden får den önskade ablationseffekten, utan varaktig påverkan på närliggande vitala organ. Detta skulle kunna medföra stora fördelar för patienter genom att eliminera risken för flera allvarliga komplikationer. Denna fördel har också påvisats i kliniska studier inklusive långtidsuppföljningar av patienterna [17-20]. I en nyligen publicerad multinationell registerstudie rapporterades inga fall av lungvensstenos, permanent frenikusnervpares eller atrioesofageal fistel [20]. Det är dock värt att notera att en övergående påverkan på frenikusnerven observerades hos 0,46 procent av patienterna i denna studie.
Inlärningskurvan är brant, och redan efter fåtal procedurer kan ingreppet utföras självständigt av operatören. Procedurtiden är kort, och på vårt centrum har vi lyckats förkorta den till cirka 50‒60 minuter. Detta kan jämföras med den genomsnittliga procedurtiden för flimmerablation i Sverige på 159 minuter enligt den senaste publicerade årsrapporten från Nationellt kvalitetsregister för kateterablation 2021 (www.ablationsregistret.se). Det är välkänt att långa ingrepp i vänstra hjärthalvan signifikant ökar risken för potentiellt allvarliga komplikationer, såsom tromboembolisk händelse och luftemboli. En procedur som tar avsevärt kortare tid är således gynnsam även för patienten. En ytterligare fördel med kort procedur är möjligheten att flera patienter kan genomgå flimmerablation polikliniskt, vilket avlastar vårdavdelningar som redan är under stor press på grund av platsbrist. Följaktligen har detta också positiv inverkan på de helt oacceptabelt långa väntetider som den nationella ablationsverksamheten lider av i nuläget. De publicerade studierna och vår erfarenhet av PFA talar för att tekniken kommer att spela en viktig roll vid ablation av förmaksflimmer och att tekniken bör erbjudas till denna patientgrupp.
Metoden har vissa begränsningar som bör belysas. Randomiserade studier saknas, något som krävs för att kunna jämföra PFA:s långtidsresultat med konventionell radiofrekvens- eller kryoablation. Sådana studier pågår nu, och inom en snar framtid kommer resultaten att redovisas. Med dagens PFA-kateter kan man bara utföra lungvensisoleringar. Vid eventuell förekomst av andra arytmier utöver förmaksflimmer, såsom förmaksfladder, så kallat Wolff–Parkinson–White-syndrom eller AV-nodal återkopplingstakykardi, måste tekniken skiftas till radiofrekvens-eller kryoablation i samma seans. För närvarande sker visualisering av ablationskatetern i hjärtat med hjälp av genomlysning, vilket innebär ökad exponering för strålning. Visualisering av PFA-kateter och tredimensionell konstruktion av vänster förmak samt 3D-kartläggning av lungvener med PFA-kateter vore mycket attraktivt. Denna metod är i utvecklingsstadiet och i åtminstone ett av de tillgängliga 3D-kartläggningssystem är den genomförbar. PFA-katetern är betydligt dyrare än radiofrekvens- och kryoablationskatetrar. Denna kostnadsökning i nuläget kan försvaras av en sannolikt mindre risk för komplikationer. En ytterligare begränsning är behov av djup sedering, vilket innebär närvaro av narkospersonal under proceduren och behovet av övervakning under ett par timmar efter avslutat ingrepp. Följaktligen kommer behovet av narkospersonal på ablationscentrum att öka för att kunna använda metoden.
Läs även författarintervju:
5 frågor till Fariborz Tabrizi
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
(uppdaterad 2024-10-17)