Att avbryta livsuppehållande behandling är en vanlig uppgift för intensivvårdsläkare.
Det finns en del beslutsstöd när det gäller huruvida livsuppehållande behandling ska avbrytas, men inte för hur det ska göras.
Hur livsuppehållande behandling avbryts varierar från läkare till läkare, även i identiska fall, och den variationen kan skapa stress hos den övriga personalen.
Läkares beslut påverkas av senioritet och Iva-erfarenhet.
Studien kan användas som diskussionsunderlag för att hjälpa läkare att förstå varför och för vem de gör som de gör.
Under 2019 vårdades 43 660 vuxna patienter på Sveriges intensivvårdsavdelningar (Iva). Under året dog ungefär 3 500 patienter, vilket ger en mortalitet på 8 procent. Beslut om att begränsa livsuppehållande behandling hade fattats hos 18 procent av Iva-patienterna någon gång under vårdtiden (7 900 patienter) [1]. Att ta hand om döende patienter och att fatta beslut om livsuppehållande behandling är vanliga arbetsuppgifter för läkare på Iva.
En opublicerad pilotstudie som undersökte hur läkare valde att avsluta livsuppehållande behandling hos Iva-patienter genomfördes på två sjukhus i Stockholm under 2018 (Södersjukhuset, 12 Iva-läkare; Karolinska universitetssjukhuset, 14 Iva-läkare). Läkarna fick två fiktiva patientfall med tillhörande frågor och några olika svarsalternativ rörande hur de skulle avsluta den livsuppehållande behandlingen. Det fanns inga etiska aspekter kvar att diskutera angående beslutet att avsluta; frågorna gällde endast hur vården skulle avslutas. Trots detta förelåg en stor variation gällande hur och när inotropt stöd, ventilatorvård och läkemedel såsom antibiotika skulle avslutas. Erfarenheter från Iva på Södersjukhuset talar för att en sådan variation kan orsaka osäkerhet och stress hos både Iva-personalen och närstående.
Svensk förening för anestesi och intensivvård (SFAI) har publicerat en riktlinje för avbrytande av livsuppehållande behandling [2]. Den innehåller generell information om hur ett avbrytande bör gå till, men är så allmänt skriven att alla föreslagna svarsalternativ i pilotstudien, trots stor variation dem emellan, följer riktlinjen.
Donation efter cirkulationsstillestånd (DCD) har nyligen introducerats i Sverige (Fakta 1). DCD-protokollet ger mer specifik vägledning när det gäller avbrytande av livsuppehållande behandling än SFAI:s riktlinje [3]. Pilotstudien visar att många läkare avbryter livsuppehållande behandling i enlighet med SFAI:s riktlinje, men att avbrytandet inte skulle vara kompatibelt med en DCD-process.
Det finns många faktorer som påverkar beslut kring hur ett avbrytande ska gå till. Riktlinjer föreslår att själva avbrytandet ska anpassas till både patientens och närståendes behov, men baserat på klinisk erfarenhet och lokala diskussioner tror vi att olika Iva-läkare kan ha väldigt olika tillvägagångssätt, även i identiska fall. Pilotstudien visade att denna variation skulle kunna bero på olika läkares erfarenhet, etiska uppfattningar eller tidigare upplevelser. Att vårda patienter efter att beslut om att begränsa livsuppehållande behandling har fattats är en riskfaktor för stress och utmattning, och gott samarbete och kommunikation inom vårdteamet är viktigt för att minska stressen [4, 5]. Den variation som pilotstudien visade skulle därför kunna vara negativ för vårdteamet [6].
Syftet med vår studie var att undersöka variation i läkares beslut kring hur livsuppehållande behandling avslutas och huruvida genus, erfarenhet eller sjukhusstorlek påverkar.
Metod
Det svenska donationsnätverket (regionalt donationsansvariga läkare, RDAL, och donationsansvariga läkare, DAL) användes för att nå så många läkare i Sverige som tjänstgör på Iva som möjligt. Läkare fick en inbjudan per mejl att delta i studien via en digital enkät. Enkätsvaren anonymiserades före analys.
Enkäten innehöll frågor om genus, erfarenhet, huvudplacering och antal Iva-platser. Det fanns två fiktiva patientfall där beslutet att avbryta livsuppehållande behandling redan hade fattats. De deltagande läkarna blev ombedda att svara på frågor om hur de skulle avbryta livsuppehållande behandling.
Resultaten analyserades med deskriptiv statistik. Skillnader mellan grupper beräknades med Fishers exakta test. P < 0,05 accepterades som statistiskt signifikant. Beräkningar gjordes med SPSS Statistics version 28.
Enkäten undersökte läkares uppfattningar och innebar ingen behandling av känsliga personuppgifter, varför studien inte föll under lagen om etikprövning.
De två fiktiva patientfallen beskrivs i Fakta 2.
Resultat
En kontaktperson som var villig att delta i studien identifierades på 37 av 87 möjliga sjukhus. Efter uppföljning och instruktioner om hur enkäten skulle distribueras deltog 14 sjukhus. 486 läkare fick digitala enkäter och 247 returnerades (51 procent svarsfrekvens).
Deltagande läkare var ST-läkare (19 procent), specialister (33 procent) och överläkare (48 procent). 43 procent var män och 55 procent kvinnor, och 2 procent föredrog att inte ange kön. Läkare uppgav att de hade arbetat inom specialiteten mindre än 5 år (17 procent), 5–10 år (27 procent) eller mer än 10 år (56 procent). Sjukhusen som representerades hade färre än 5 Iva-platser (7 procent), 5–10 Iva-platser (71 procent) eller fler än 10 Iva-platser (22 procent). 45 procent uppgav att deras huvudplacering var Iva, 32 procent hade huvudplacering på operationsavdelning och 23 procent arbetade lika mycket på Iva och operationsavdelning.
Fall 1
97 procent av läkarna uppgav att de skulle avsluta antibiotikaterapi och enteral nutrition. 83 procent skulle avsluta vätsketerapi. 90 procent skulle stänga av noradrenalininfusionen, medan 9 procent skulle trappa ut den över timmar och 1 procent skulle fortsätta den.
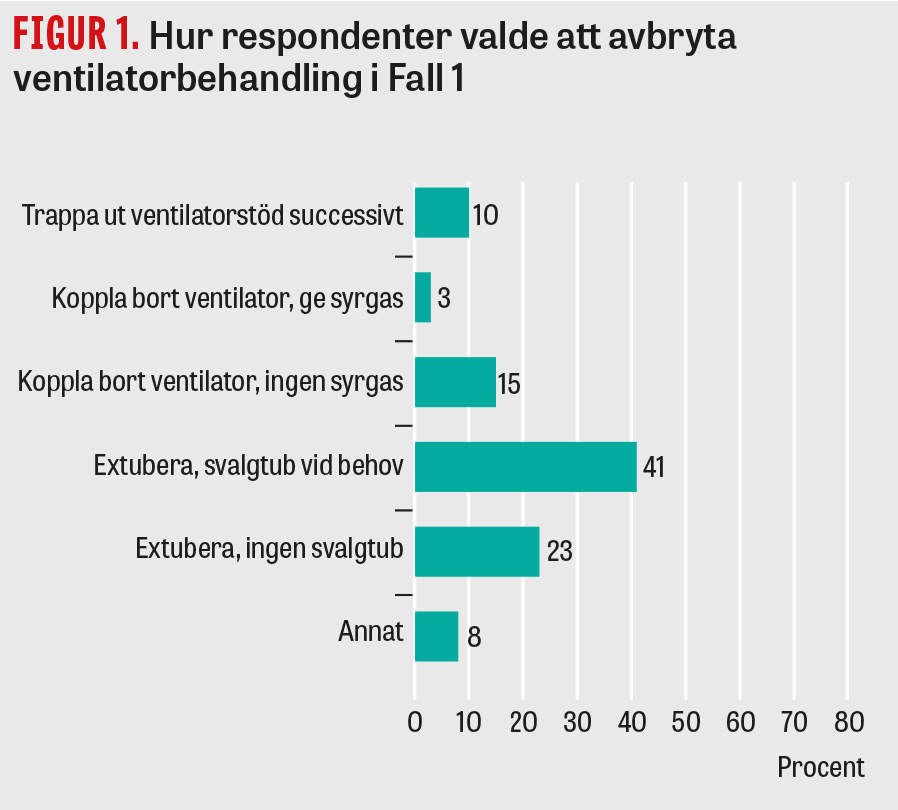
28 procent av läkarna skulle inte extubera patienten, inklusive de 10 procent som skulle trappa ut ventilatorbehandlingen över tid. 64 procent skulle extubera patienten, och 8 procent uppgav att de skulle göra en kombination beroende på hur patienten reagerade (Figur 1).
Fall 2
90 procent av läkarna uppgav att de skulle avsluta antibiotikaterapi, och 91 procent skulle avsluta enteral nutrition. 88 procent skulle avsluta trombosprofylax och 81 procent stressulkusprofylax. 80 procent skulle stänga av noradrenalininfusionen, men 18 procent skulle trappa ut den över timmar.
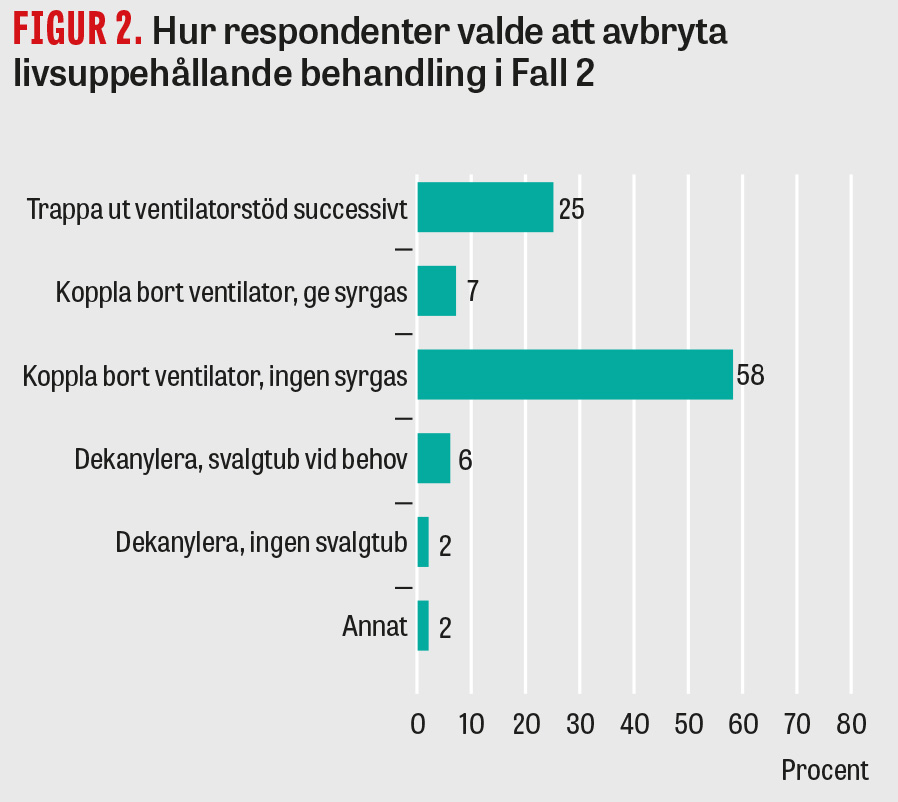
25 procent av läkarna skulle trappa ut ventilatorbehandlingen över tid, 58 procent skulle koppla bort ventilator och låta patienten andas rumsluft. 8 procent skulle dekanylera patienten. 3 procent valde en kombination av nedtrappning av ventilatorstöd och sedan bortkoppling av ventilatorn när patienten hade blivit medvetslös (Figur 2).
Skillnader beroende på placering och kompetens
I Fall 1 var det vanligare att beslutet att extubera fattades av en läkare som hade Iva som huvudplacering jämfört med läkare som arbetade huvudsakligen på operationsavdelning (P < 0,001) eller som arbetade lika mycket på Iva och operationsavdelning (P < 0,001). I Fall 2 var det vanligare att specialister avslutade ventilatorbehandling jämfört med ST-läkare (P = 0,007). Varken sjukhusstorlek eller genus var associerade med skillnader i beslut.
Diskussion
Beslut kring avbrytande av livsuppehållande behandling är viktiga och en vanlig del av arbetet på en intensivvårdsavdelning. Det finns en del stöd när det gäller hur beslut ska fattas, men lite stöd när det gäller hur behandlingen ska avbrytas. Den skillnaden kan kanske vara en del av förklaringen till den variation i praxis som vi har visat i vår studie. När ett beslut att avbryta livsuppehållande behandling har fattats ska all icke-palliativ behandling avbrytas [2], men 20 procent av respondenterna uppgav att de skulle fortsätta med ulkusprofylax och vätsketerapi. Det kan vara så att enstaka läkare ser de behandlingarna som palliativa. Närstående kan ha velat ha kvar vätsketerapi i tron att patienten annars skulle lida av törst.
Att behandla lågt blodtryck med noradrenalin är inte en palliativ behandling, men 9 procent i Fall 1 och 18 procent i Fall 2 skulle trappa ut behandlingen över några timmar och därmed förlänga döendet. En förklaring kan vara att läkare inte vill att en patient ska dö »för snabbt« eller i för nära anslutning till avbrytandet, med risk för etisk stress hos närstående eller vårdteamet.
Störst variation fanns kring beslut om hur man skulle avbryta ventilatorbehandling. 10 procent i Fall 1 och 24 procent i Fall 2 skulle trappa ut ventilatorbehandling och därmed förlänga döendet, kanske för att undvika känslan att det var själva extubationen som orsakade patientens död. Av de som skulle extubera var det 44 procent som skulle använda en svalgtub om patienten inte kunde hålla fri luftväg – en behandling som förlänger döendet, men som vissa läkare kanske ser som palliativt.
En stor multicenterstudie som undersökte hur extubation eller nedtrappning av ventilatorbehandling påverkade närstående och Iva-personalen visade ingen skillnad när det gäller närståendes posttraumatiska stressymtom, ångest eller depression [7]. Läkare beslutade att extubera oftare om patienten var medvetslös, och valde att trappa ut ventilatorstöd om patienten hade respiratorisk svikt, vilket är i linje med våra resultat. Iva-personalen mådde bättre psykologiskt vid extubation än vid nedtrappning. För att en DCD-process ska fungera måste patienten extuberas. Intervjuer av personal och närstående som genomfördes som en del av DCD-introduktionen i Sverige visade att extubation accepterades i alla DCD-fall och att närstående hade hoppats att döendet skulle gå fort [8].
Det finns stor variation kring när och hur beslut att begränsa livsuppehållande behandling fattas mellan världsdelar, mellan länder, mellan olika sjukhus inom samma land och även inom samma intensivvårdsavdelning [9]. Det är kanske inte förvånande att vår studie visar att det även finns en stor variation när det gäller hur livsuppehållande behandling avbryts.
Det är viktigt att patienter behandlas som individer och att behandling och avbrytande av behandling anpassas till patientens behov och önskemål. Ett team i Frankrike har utvecklat ett instrument för att utvärdera närståendes upplevelse av vården under processen att dö [10]. Av de 15 punkter som ingår i frågeformuläret finns det inga som handlar om hur eventuell livsuppehållande behandling blev avbruten. De flesta frågorna handlar i stället om kommunikation mellan vårdteam, patient och närstående. Närstående mådde bättre vid uppföljning efter 6 månader om kommunikationen upplevdes som bra.
Att vårda en döende patient efter att livsuppehållande behandling har avbrutits kan vara associerat med ökad stress för personalen. Faktorer som har visat sig vara viktiga för att hjälpa personalen att hantera eller minimera stressen inkluderar god kommunikation och samarbete inom vårdteamet samt effektivt ledarskap och tydligt beslutsfattande [5].
Vi har visat en stor variation i praxis trots att fallen var identiska. Variationen beror därför inte på patientens eller närståendes preferenser, utan på hur läkarna resonerar. Variation mellan läkare som arbetar på samma avdelning riskerar att öka stressen hos vårdteamet om inte kommunikationen är adekvat.
En av studiens styrkor är att de fiktiva fallen inte innehöll några etiska frågor om beslutet att avsluta den livsuppehållande behandlingen; frågorna rörde endast tillvägagångssättet. En svaghet är den låga svarsfrekvensen. Även urvalsprocessen, där donationsnätverket användes för att identifiera kontaktpersoner på sjukhusen, kan ha påverkat vilka läkare som valde att svara på enkäten. Det kan vara så att frågor som är personliga och som rör etiskt komplexa situationer är svåra att svara på. Det var dock en styrka att enkäten besvarades av läkare som representerade olika åldrar, erfarenheter och arbetsplatser.
Slutsats
Vår studie visar att läkare gör olika även i identiska fall och att yrkeserfarenhet och vana vid intensivvård påverkar besluten. Det kan vara så att läkare och närstående har olika syn på vad som är viktigt när livsuppehållande behandling avbryts.
Det behövs kvalitativa studier som undersöker både personalens och närståendes förväntningar och upplevelser när det gäller avbrytande av livsuppehållande behandling. Det är viktigt att avbrytandet av livsuppehållande behandling sker baserat på vad som är bäst för patienter och deras närstående och inte på vad som känns bäst för läkaren. Det är kanske inte möjligt att skriva ett strikt protokoll för avbrytande av livsuppehållande behandling, men det kan finnas en vinst med en viss standardisering av processen för att underlätta teamarbetet. Livsuppehållande behandling behöver inte alltid avbrytas på ett sätt som är kompatibelt med DCD, men om den avbryts på ett annat sätt är det bra att fundera på varför man väljer att förlänga dödsprocessen.
Oavsett hur livsuppehållande behandling avbryts är kommunikation mellan vårdteam, närstående och om möjligt patienten väldigt viktig.
Resultaten skulle kunna ligga till grund för diskussion på olika intensivvårdsavdelningar, när en läkare vill fundera på sin egen praxis, när riktlinjer kring avbrytande behöver skrivas eller uppdateras och när DCD-processen introduceras.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Donation efter cirkulationsstillestånd (DCD)
Vid en DCD-process fastställs döden med indirekta kriterier (kännetecken som visar på varaktigt hjärt- och andningsstillestånd). Fastställandet sker efter att livsuppehållande behandling avbrutits, det vill säga att patienten har kopplats bort från respiratorn, och en 5 minuter lång väntetid, en så kallad »no-touch«-period, då ingen cirkulation eller andningsrörelser registrerats. Vid en DCD-process behöver donationsoperationen påbörjas skyndsamt efter att döden fastställts, eftersom organen inte är syresatta.
Fakta 2. Fiktiva fall 1 och 2 i enkätundersökningen
Fall 1
Kvinna, 55 år, behandlad för hypertoni (amlodipin), hittas av sin make medvetslös i badrummet. Patienten kommer till akuten med ambulans och med ofri luftväg, tecken på aspiration, blodtryck 180/90 mm Hg, GCS (Glasgow coma scale) 4 och spontanandning. Patienten intuberas på akuten, DT visar massiv subaraknoidalblödning. Konservativ behandling på grund av dyster prognos enligt neurokirurgjour. Patienten tas till Iva.
Efter 2 dygn visar patienten inga tecken på inklämning. Patienten spontanandas med FiO2 0,4, positivt slutexspiratoriskt tryck (PEEP) 10; blodtrycket är 120/60 mm Hg med noradrenalin 100 ng/kg/min. Patienten behandlas med cefotaxim för aspiration, enteral nutrition 20 ml/h, glukosdropp med elektrolyter.
I samtal säger maken att hans fru har tagit klar ställning mot donation och sagt att hon inte vill bli vårdad på Iva som en »grönsak« om hon skulle drabbas av något allvarligt. Personalen och familjen är överens om att avbryta livsuppehållande behandling och låta patienten dö. Inga fler närstående är på väg, och familjen som har samlats känner att de har fått den tid de behöver.
Fall 2
Man, 68 år, har varit rökare hela sitt vuxenliv och varit inlagd flera gånger under de senaste 2 åren med KOL-exacerbationer. Han har nu varit inneliggande på Iva i 3 veckor på grund av en KOL-exacerbation och lunginflammation. Han är trakeotomerad sedan 14 dagar tillbaka, och urträning har inte fungerat på grund av koldioxidretention och stress när ventilatorinställningar har minskats. Hans döttrar berättar att han var mycket medveten om hur sjuk han var före detta vårdtillfälle och hade berättat för dem att han inte ville vårdas i ventilator länge om det inte gick framåt. Han var glad över sitt liv och inte rädd för att dö. Efter samtal med Iva-personal är alla överens om att avbryta livsuppehållande behandling.
Patienten är ventilerad i tryckunderstöd (TU)/kontinuerligt positivt luftvägstryck (CPAP) med PEEP 8 cm H2O, TU 6 cm H2O och FiO2 0,3. pO2 är 8 kPa, pCO2 9 kPa och andningsfrekvens 16/min. Han hade varit stressad och takypnoisk och är därför sederad med dexmedetomidin och fentanyl. Han är lugn i vila, grimaserar vid undersökning. Blodtrycket är 110/60 mm Hg, hjärtfrekvens med sinusrytm 100 och noradrenalin 80 ng/kg/min. Han behandlas med cefotaxim och har full enteral nutrition via en nutritionssond.