Tillförlitliga data för barnreferensintervall har länge varit en bristvara.
I en prospektiv studie från Falun samlades blod från 701 friska barn. Referensintervall för ett 50-tal allmänkemiska och hematologiska analyser beräknades.
Tillförlitliga data för barnreferensintervall har länge varit en bristvara, men under 2012 och 2013 har tre stora projekt publicerats i vilka blodprov från friska barn har samlats prospektivt i förskolor och skolor. I en studie från Falun mättes allmänkemiska och hematologiska analyser på 700 friska barn. I studier från Kanada och Danmark har också blod samlats för allmänkemiska analyter.
Tidigare data
Referensintervall bör skapas efter mätningar på blodprov från referenspersoner som är friska och definierade med avseende på ålder, kön och etnisk grupp. I det nordiska samarbetsprojektet NORIP (Nordiska referensintervallprojektet) [1] mättes allmänkemiska analyter på 3 600 friska individer från 18 års ålder [2]. De referensintervall som togs fram i detta projekt implementerades vid de flesta klinisk-kemiska laboratorier i de nordiska länderna för cirka tio år sedan. Motsvarande studier på barn har varit svåra att genomföra. Etikkommittéerna har varit restriktiva vad gäller att låta forskare samla in prov från friska barn, och logistiken kan vara besvärlig, varför vi länge har varit hänvisade till att använda barnreferensintervall av varierande kvalitet.
Vad har funnits tidigare av barnreferensintervall? Diagnostikaindustrins förslag är oftast bara för vuxna. Den stora bibeln på området har länge varit Soldins »Pediatric reference ranges« [3], men många av källorna boken utgörs av retrospektiva utsökningar ur laboratoriernas databaser. Nackdelarna med detta är många. I vissa fall har man använt olika statistiska procedurer för att minska inflytandet av de mest avvikande resultaten, som skulle kunna tänkas komma från patienter med en sjukdom eller behandling som påverkar det man vill mäta. I andra fall har man eliminerat data från särskilda enheter, t ex hematologiska och onkologiska avdelningar, där man kan förvänta sig svårt sjuka barn med klart avvikande laboratorievärden. Andra studier har använt överblivet provmaterial från barn som bedömts vara relativt friska, t ex från öppenvårdsmottagningar eller viss elektiv kirurgi. Men även sådana infallsvinklar har uppenbara svagheter – på barn tas blodprov bara när det är mycket välmotiverat!
En annan kompromissmetod som tillämpats är att samla blod i samband med anestesi vid planerad kirurgi på barn som är metabolt friska. Denna utgångspunkt har använts i Uppsala och vid ARUP labs ChildX-projekt i USA [4, 5]. Detta sätt att arbeta kräver stora resurser. Patientunderlaget blir också lätt skevt med avseende på kön och ålder – små pojkar med urologiska missbildningar och tonårsflickor med skolios kan t ex vara vanliga på operationsschemat.
Prospektiva studier på friska barn
Prospektiva studier av referensintervall för friska barn beträffande de analyser som ingår i våra dygnet runt-sortiment är förvånansvärt få. Många studier är av äldre datum, och analyserna har utförts med metoder och instrument där överensstämmelsen med dagens laboratorieresultat är varierande och där beskrivningen av metoder, reagens och kalibratorer är bristfällig [6].
Det kanadensiska projektet CALIPER har under de senaste åren publicerat flera studier på data från mätningar på överblivet provmaterial, uppdelat på olika instrumenttillverkare [7-9]. Under 2012 kom dock ett stort prospektivt arbete från CALIPER [10], där man hade rekryterat 2 188 friska barn i åldern 0–18 år från skolor och kyrkor i Toronto-området. För barn under 1 års ålder tvingades man dock att använda överblivet provmaterial från sjukvården. Arbetet redovisade även en del data efter uppdelning i de största etniska grupperna. Studien omfattade ca 40 allmän- och proteinkemiska analyser utförda med instrument från tillverkaren Abbott. Nyligen publicerades också en studie från Köpenhamn [11]. Den inkluderade 1 429 individer i åldern 6–20 år, där prov samlats in i skolor. I studien analyserades ett 20-tal allmänkemiska analyter med instrument från tillverkaren Roche.
Faluprojektet
Faluprojektet är ett samarbete inom regionen Uppsala–Örebro. Studien inkluderade 701 barn i åldern 6 månader till 19 år efter godkännande av regionala etikprövningsnämnden i Uppsala. Barnen rekryterades på barnavårdscentraler, förskolor och skolor i Faluområdet. Sjuksköterskor och lärare på barnavårdscentraler respektive skolor ställde upp med lokaler och schemaavbrott. De mindre barnens blodprov togs under lugna förhållanden på en barnmottagning, medan provtagningen på skolbarnen ägde rum i skolorna. Alla uppmanades att sitta och vila 15 minuter före provtagningen.
Barn med kronisk sjukdom eller infektion de senaste tio dagarna ombads att inte delta. Barnen och deras föräldrar fick fylla i en enkät som innehöll bl a frågor om hälsa, sjukdomar, allergier och läkemedel, både receptfria och receptbelagda. Fyra barn exkluderades: två med typ 1-diabetes, ett med neurofibromatos och ett med tyreotoxikos. Däremot inkluderades den stora grupp som angav någon form av allergi eller astma. Vid provtagningen togs serum- och EDTA-rör venöst. De allmänkemiska analyserna gjordes på serum, men de beräknade referensintervallen bör till stora delar även kunna tillämpas på plasma. För ett par av de nu aktuella analyserna (kalium och fosfat) noterades smärre skillnader mellan serum och plasma i NORIP [1]. Analys av ett 50-tal komponenter utfördes med Abbott Architect (allmän kemi), Siemens Bayer
Advia (hematologi) samt Mono S och Tosoh system (HbA1c). Barnen var inte fastande. NORIP:s serum X användes för spårbarhet till erkända referensmaterial och i vissa fall för korrigering av rådata. Resultaten finns pub-licerade i fyra del-arbeten [12-15]. Överblivet provmaterial från projektet finns också tillgängligt för framtida egna eller externa studier.
Liknande upplägg i studierna från Falun och Köpenhamn
Faluprojektet och Köpenhamnsstudien har haft liknande upplägg med avseende på den statistiska bearbetningen med utgångspunkt i NORIP. Detta inkluderar uträkning av icke-
parametriska 2,5- och 97,5-percentiler, Dixons test för detektion av extremvärden samt uppdelning i ålder och kön enligt Lahti-modellen [16].
Uppdelning med avseende på ålder utgör en särskild fråga vad gäller barnreferensintervall. Flera studier har använt fasta intervall för alla analyter, t ex CALIPER:s förstudier på överblivet material. Både Faluprojektet, CALIPER och Köpenhamnsstudien har använt »kvalificerade gissningar« för att utifrån tidigare publicerade data och egna siffror börja bearbeta rådata vad gäller uppdelningar.
Puberteten är ett särskilt problem vad gäller barnreferens-intervall. Pubertetsutvecklingen har bara bedömts enligt Tanner-skalan i ett fåtal barnreferensintervallstudier. Samtidigt är det inte rimligt att laboratorierna avkräver beställaren sådan information vid analys av rutinprov. Dessutom är det svårt för laboratorierna när man skickar provsvar att med dagens IT-system koppla ihop resultaten med referensintervall som tagit hänsyn till pubertetsutvecklingen. I Köpenhamnsstudien, som utgick från blodinsamling i samband med ett projekt om pubertet, noteras att vissa analyter förändras under puberteten, t ex kreatinin, som ökar kontinuerligt med åldern.
Jämförelse av data från Falun, Köpenhamn och Kanada
Hur står sig data från Falun, Köpenhamn och Kanada vid en jämförelse? För vissa analyser ses tydliga skillnader; för and-ra är samstämmigheten god. Eftersom köns- och åldersuppdelningar varierar är det svårt att göra direkta jämförelser. Detta kan illustreras med fosfat, där alla källor uppvisar samma tendens till att mittpunkten på referensintervallen sjunker med åldern. Hos de yngsta barnen ses inga skillnader mellan könen, men åldern för när könsdifferenser först observeras varierar sedan mellan 8 och 14 år. Uppdelningen i olika åldersgrupper varierar mellan två till fem i de olika studierna. För de äldre tonåringarna stämmer de flesta referensintervall väl med referensintervallen för 18-åringar i NORIP-projektet [12-15].
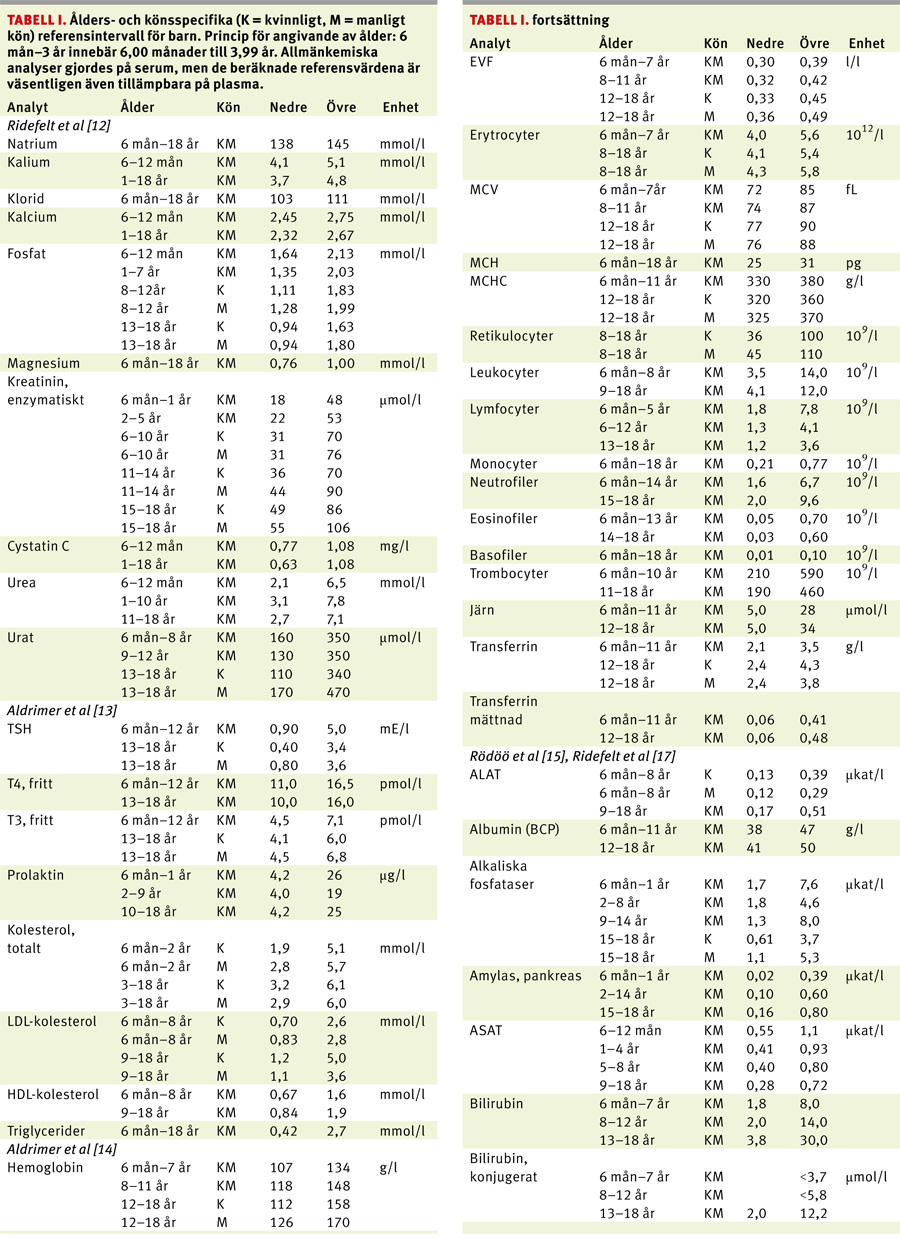
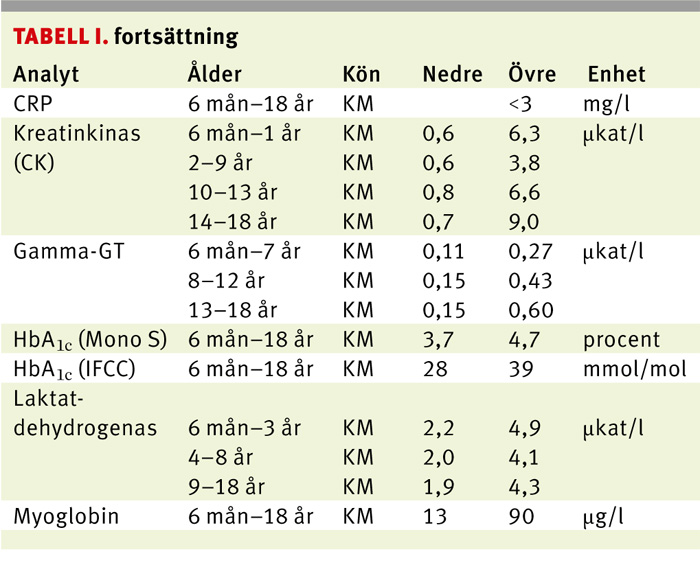
Tabell I sammanfattar de referensintervall som tagits fram genom Faluprojektet. Många av de allmänkemiska analysernas referensintervall bör kunna användas vid laboratorier med andra instrument, medan en del av de immunkemiska analysernas referensintervall, t ex för tyreoideahormoner, i första hand är tillämpbara på samma analysplattform.
Referensintervall för de allra yngsta barnen saknas
Falustudien innehåller endast data på barn från 6 månaders ålder. De flesta analyser uppvisar stora förändringar hos friska barn under de första veckorna efter födelsen. För en del analyser, t ex inom hematologi, tar det flera månader innan de analyserade parametrarna har stabiliserats. CALIPER-studien innehåller data på barn ända ner till 0 dagars ålder. Dessa data kan i viss mån användas för att extrapolera Falustudiens referensintervall då projektet saknar mätningar på barn i åldern 0–6 månader. Detta är dock en procedur med stor osäkerhet.
Ett alternativ är att laboratorier vid utskick av svar på prov från barn 0–6 månader lämnar en textkommentar om de värden som gäller för barn från 6 månaders ålder och uppåt i stället för ett riktigt referensintervall. Nackdelen med detta är att ett sådant förfarande i dagens laboratoriedatasystem och elektroniska patientjournaler inte kommer att generera några markeringar för avvikande värden, t ex stjärnor eller avvikande färg på siffersvaret.
Kommentarer till specifika analyser
För blodfetter (kolesterol, HDL, LDL, triglycerider) anges i tabellen 2,5–97,5-percentiler. I bland används även 5–95-procentspercentiler i referensintervall för blodfetter. Dessa siffror finns angivna i Aldimer et al [13]. För cystatin C pågår ett standardiseringsarbete (inkluderande omräkningsformler till glomerulär filtrationshastighet, GFR), varför endast absolutvärden i mg/l angivits för den metod och kalibrering som använts i Falun och Uppsala under de senaste åren.
Dessutom är de formler som används för att beräkna GFR från cystatin C som regel enbart validerade på vuxna. Den använda metoden är inte optimerad för att mäta riktigt låga halter av CRP, varför den uppskattade gräns som anges mer är att betrakta som en medicinsk beslutsgräns än som ett sant referens-intervall. Flera barn under 2 år hade klart förhöjda halter av alkaliskt fosfatas. Detta har beskrivits förr och tros bero på uteslutningsdiagnosen benign transient hyperfosfa-tasemi. Vid beräkning av referensintervallen har dessa barn exkluderats [17]. Kalcium redovisas i Tabell I endast som P-kalcium. I Ridefelt et al [12] visas data för albuminmodiferat kalcium enligt den formel som används i Falun.