En intraosseös infart kan ha stor klinisk betydelse i den akuta situationen då det är svårt att få kärlaccess.
Provtagning via intraosseösa nålar har ifrågasatts med tanke på risken att aspirera benmärgspartiklar.
Vi rekommenderar, så långt det är möjligt, patientnära metoder för intraosseösa prov. Detta gäller särskilt då helblod (exempelvis blodgaser) ska analyseras.
Vid centrifugering av intraosseöst aspirat kommer eventuella benmärgspartiklar att hamna i pelleten. Supernatanten motsvarar närmast plasma. Vi har på så sätt analyserat kreatinin, morfin och troponin i intraosseösa prov.
Leukocyter och trombocyter, vilka bildas i benmärgen, kan ge falskt förhöjda värden vid analys av intraosseösa prov. Risken för hemolys bör övervägas.
För kritiskt sjuka patienter är det viktigt att behandlingen kan påbörjas snabbt. Detta förutsätter att man får tillgång till blodbanan, vilket kan vara svårt hos patienter med sviktande cirkulation.
Intraosseös tillgång till blodbanan kan i dessa situationer vara av livsavgörande betydelse. Flera svenska landsting rekommenderar att det i varje akutambulans/prehospitalt akutteam finns utrustning och kompetens för att etablera en intraosseös infart för livsviktig tillförsel av läkemedel och/eller vätska då perifer venväg är svår att etablera. Vid cirkulationssvikt går det snabbare att etablera intraosseös än intravenös infart [1-3]. Utrustningen har också införts i akutväskor på flera sjukhus.
Intraosseös access introducerades för nära 100 år sedan [4], och efter att under en period ha minskat i omfattning har intraosseösa nålar fått något av en renässans [1-3]. Åsikterna om hur väl analysresultat från intraosseös provtagning överensstämmer med dem från venös provtagning verkar variera. Det finns dock en del äldre studier på barn och djur som tyder på att akutanalyser av till exempel hemoglobin, natrium, kalium, klorider och glukos ger resultat som överensstämmer relativt bra med dem från venösa eller arteriella prov, medan det är betydande skillnader vad gäller leukocyter och trombocyter [5, 6]. Resultat från senare studier, utförda på hemodynamiskt stabila försökspersoner, överensstämmer väsentligen med dessa fynd [7, 8].
Indikationer och metod
Intraosseösa injektioner/infusioner används främst då det finns ett akut behov av att tillföra läkemedel och vätska, när man misslyckats med att skapa en fri venväg [9-11].
Även om olika tillverkare har valt olika tekniska lösningar är de grundläggande principerna för inläggning av intraosseösa nålar gemensamma. När man bestämt infartsställe (vanligen caput humeri eller proximala tibia) och nålstorlek, desinficeras huden och den intraosseösa nålen läggs in med vald teknik till ett läge med spetsen intramedullärt, varefter den fixeras. När den intraosseösa nålen är på plats kan blodprov aspireras, vilket bör ske innan vätskebehandling påbörjas [12, 13]. Man bör kassera åtminstone 2 ml av det första aspiratet [12, 13]. Observera att såväl injektion som provtagning via den intraosseösa nålen kan utlösa kraftig smärta hos en patient vid medvetande.
Blandat provmaterial
Intraosseösa prov kommer att bestå av en blandning av venöst blod och benmärg. Det innebär sannolikt att ämnen som produceras lokalt i märgen kan ge upphov till en felaktig bild av koncentrationen av dessa ämnen i blodbanan, medan påverkan bör vara mindre för ämnen som produceras till exempel i levern. Intraosseös provtagning skulle också kunna bidra till en ökad hemolysgrad jämfört med venös provtagning.
Vilka analyser kan rekommenderas?
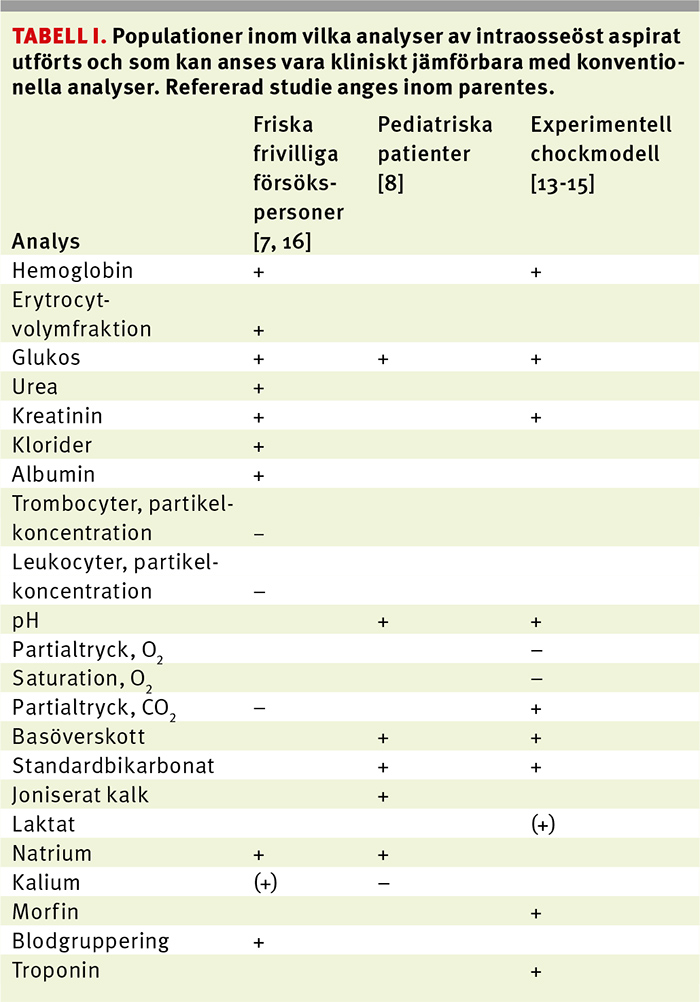
Intraosseös provtagning används enbart i akutsituationen. Det är ett begränsat antal analyser som kan anses viktiga i den akuta handläggningen av patienten under tiden fram tills man får en fungerande ven- och/eller artärnål. Tabell I visar ett försök till sammanställning av vilka av dessa analyser som går respektive inte går att göra. I detta sammanhang måste betonas att humanstudierna [5, 7, 8] utförts under cirkulatoriskt stabila förhållanden, medan djurförsök utförts i en chockmodell. Rekommendationen avseende tolkning av blodgaser under experimentell chock [13] hänför sig till den tidigaste fasen av detta experiment. Skillnaderna mellan intraosseöst aspirat och konventionellt tagna prov tenderar att öka med tiden. Dessa begränsningar kan ha betydelse för tolkningen av våra rekommendationer. Det är således väsentligt att betona att analyser av intraosseöst aspirat är utpräglade akutprov, som måste tolkas med stor försiktighet och inte kan ersätta konventionellt tagna blodprov. De svar man erhåller vid analys av intraosseöst aspirat får ses som en första indikation inför den akuta handläggningen av en svårt sjuk patient. Exempelvis är partialtrycket av syrgas (pO2) i intraosseöst aspirat väsentligt lägre än i artärblod, medan partialtrycket av koldioxid (pCO2) kan ge vägledning om förhållandena i artärblod. Intraosseösa prov bör därför givetvis, i görligaste mån, kompletteras med andra tänkbara metoder för monitorering, exempelvis saturationsmätare.
Vår bestämda rekommendation är att man så långt det är möjligt använder patientnära analysmetoder (point-of-care technology, POCT) med engångskyvetter. Det är en typ av instrument som ofta används på husläkarmottagningar för att mäta hemoglobin (Hemocue eller i-STAT) eller CRP, vid graviditetstest, Strep-A- eller Monospot-test.
Då provet i dessa fall analyseras i en kyvett finns ingen risk för att eventuella benmärgspartiklar i det intraosseösa aspiratet kommer i kontakt med analysinstrumentet och stör analyserna av kommande prov. Vi har med hjälp av POCT analyserat blodgaser experimentellt såväl i cirkulatoriskt jämviktsläge som i en chockmodell [12, 13]. POCT kan användas för ett flertal av de analyser som kan behövas i det akuta skedet.
I de fall det av någon anledning inte är möjligt att använda POCT bör provet centrifugeras så att eventuella benmärgspartiklar ansamlas i pelleten, medan supernatanten närmast motsvarar plasma. Vi analyserade utan problem kreatinin respektive morfin i intraosseöst aspirat och analysen gjordes på supernatant [14, 15]. Morfin analyserades som typsubstans för opiater, mot bakgrund av att dylika farmaka ses vid intoxikationer. Troponin I analyserades på samma sätt utan problem med en högkänslighetsmetod, Architect ci16200 analyzer (Abbott Laboratories) [16].
Cellräknare är känsliga för koagel (och därmed även benbitar), och det är risk för allvarliga driftsproblem vid analys av den typen av prov. Hur stort detta problem egentligen är vet vi inte säkert i dag. Intraosseösa prov kommer att innehålla omogna celler från benmärgen. När proven kommer till laboratoriet uppfattar man dem som vanliga venösa prov om de inte specifikt anges vara benmärgsaspirat. När man sedan finner omogna celler med hjälp av cellräknaren så är den normala laboratorierutinen att man undersöker proven manuellt med mikroskop. Detta kommer i sin tur att leda till en betydande försening av analyssvaren. Troligtvis får man svaret på analys av leukocyter och trombocyter snabbare om man avvaktar till dess att man förbättrat cirkulationen och fått tillgång till ett alternativt kärl.
Man bör därför undvika att analysera leukocyter och trombocyter i intraosseösa prov. Leukocyter och trombocyter behövs i regel inte heller i den riktigt akuta situationen. Blodgruppering kan utföras på intraosseösa prov [17]. En viss försiktighet vid tolkning rekommenderas för intraosseöst tagna prov för kalium och laktatdehydrogenas då det sannolikt är vanligare med hemolys i intraosseösa prov, vilket kan leda till ökade nivåer av dessa ämnen. Även om det går att mäta kalium och laktatdehydrogenas medför risken för hemolys att vi generellt vill tillråda försiktighet vid tolkningen av dessa analyter i intraosseösa prov. Det gäller framför allt laktatdehydrogenas, som är en så pass ospecifik markör att det är tveksamt om det finns något behov av en sådan analys inom de första 1–2 timmarna för en patient med akut cirkulationssvikt.
Slutsats
Även om intraosseösa nålar var vanliga på 1920–40-talet så skilde sig den tidens laboratoriemetoder från dagens, vilket gör det svårt att dra slutsatser om användbarheten från den tiden. Det finns relativt få aktuella humanstudier och totalantalet individer är lågt [7, 8]. Resultaten är dock i linje med resultaten från grismodellerna [12-15].
Blodprov tagna intraosseöst kan skada laboratorieutrustning. Användning av patientnära analysmetoder med engångskyvetter kringgår detta problem. Alternativt kan speciellt omhändertagande av provet på sjukhuslaboratoriet göra att detta kan analyseras med vanliga instrument. Om inte anatomiska/fysiologiska förhållanden antyder annat kommer de flesta intraosseösa provsvar att ligga nära motsvarande venösa prov.
Sammanfattningsvis kan rätt hanterade blodprov tagna ur intraosseös nål bidra med värdefull information vid handläggning av svårt sjuka patienter.
Potentiella bindningar eller jävsförhållanden: Mats Eriksson har erhållit resebidrag från Vidacare Corporation, TX. Vidacare Corporation har finansiellt stött forskning avseende intraosseös administration av antibiotika vid experimentell septisk chock.