Nationellt kvalitetsregister för cervixcancerprevention har analyserat möjliga orsaker till den ökning av livmoderhalscancer som setts i Sverige under senare år.
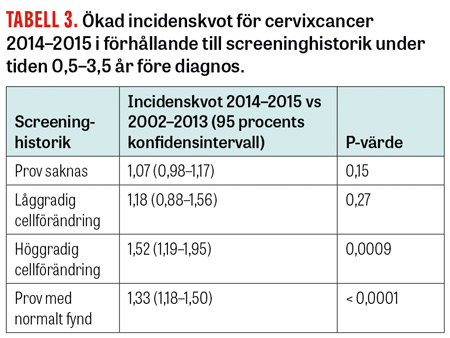
Den mest signifikanta ökningen (30 procent) ses hos kvinnor som haft ett normalt cellprov i föregående screening (P < 0,0001).
Även cancerrisken för kvinnor som tidigare haft höggradig cellförändring har ökat (P = 0,0009).
Flera laboratorier har en fortsatt mycket låg cancerrisk efter normalt cellprov, vilket tyder på att ökningen beror på faktorer som kan åtgärdas.
Alla data om omgranskning av prov tagna före diagnos av cancer och höggradig cervikal intraepitelial neoplasi kommer att begäras in och analyseras för att närmare belysa den exakta orsaken.
Cervixcancer har under senare år ökat i Sverige [1]. För 2014–2015 jämfört med 2002–2013 har det skett en ökning med 17 procent, från ca 450 till ca 550 årliga fall. Ökningen är kraftigare för adenokarcinom (31 procent) än för skivepitelcancer (12 procent). Screening skyddar sämre mot adenokarcinom då denna cancertyps förstadier är erkänt svåra att upptäcka och inte alltid är påvisbara. Till skillnad från vad som rapporterats från andra länder har Sverige haft en god effekt av screening mot adenokarcinom [2]. Det är möjligt att eventuella kvalitetsproblem skulle drabba den svåraste diagnostiken först.
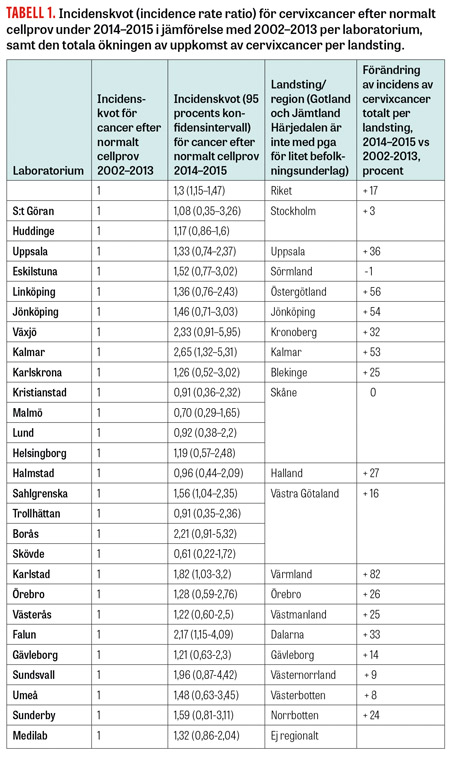
Ökningen visar anmärkningsvärda skillnader mellan landsting, från en ökning på > 80 procent till oförändrat nyinsjuknande i cervixcancer hos flera landsting (Tabell 1). Detta tyder på att ökningen kan vara relaterad till de regionalt organiserade screeningprogrammen. För ett mellanstort landsting motsvarar ökningen ca 3 fall per år. Ökningen ses i flertalet av de åldrar som erbjuds screening (Tabell 2) men är begränsad till tidiga stadier av cancer (IA och IB) (Tabell 2), och någon ökning av dödlighet har inte setts [3].
För att undersöka möjliga orsaker har vi jämfört 2014–2015 med den tidigare perioden med avseende på om kvinnor med cervixcancer har haft tidigare normala prov, haft avvikande prov eller saknat prov. Undersökningen har gjorts utifrån data från Nationellt kvalitetsregister för cervixcancerprevention (NKCx). Förekomst och utfall av cellprov taget i det tidigare screeningintervallet analyserades (0,5–3,5 år respektive 0,5–5,5 år före cancerdiagnos beroende på ålder. Prov tagna ≤ 0,5 år före cancerdiagnos inkluderades inte). Det ses ingen säkerställd skillnad mellan perioderna beträffande om prov finns eller inte (Tabell 3), vilket tyder på att skillnader i deltagande inte bidrar nämnvärt till ökningen. Detta är i linje med att deltagandet i screening har ökat under en lång följd av år [1]. Cervixcancer bland invandrade kvinnor förklarar inte ökningen.
HPV-vaccinationer har inte haft nämnvärd effekt. En länkning mellan HPV-vaccinationsregistret och NKCx för de mest aktuella åldersgrupperna (födda 1965–1984) mellan 2007 och 2016 fann 2 fall av cervixcancer hos HPV-vaccinerade (4 938 kvinnor) och 3 273 cervixcancerfall bland de 1 071 870 kvinnor som inte fått HPV-vaccin.
Risken för cervixcancer efter ett normalt prov har ökat kraftigt, med ca 30 procent (Tabell 1). Riskökningen efter normalt prov visar påtagliga skillnader mellan olika laboratorier, från mer än fördubblad risk till riskminskningar (Tabell 1). I synnerhet för laboratorier med små provvolymer kan slumpvariationen vara betydande från år till år, och resultaten för enskilda laboratorier bör tolkas försiktigt.
Även risken för cancer efter ett avvikande prov har ökat, en riskökning som är statistiskt signifikant efter en höggradig cellförändring (high-grade intraepithelial lesion, HSIL) (Tabell 3). Det har också skett en kraftig ökning av normala provsvar i screeningintervallet innan kvinnor fått den histopatologiska diagnosen höggradig cervikal intraepitelial neoplasi (CIN 2 +). Denna ökning varierar också kraftigt mellan olika laboratorier (opubl data; 2018) och kan möjligen vara relaterad till den ökade risken för cancer efter höggradig cellförändring. Det har tidigare tagits upp i en debatt i Läkartidningen [4] att det skett en uppdatering av analysmetoden till så kallad vätskebaserad cellprovtagning (liquid based cytology, LBC). Ett flertal laboratorier som använder vätskebaserad cytologi har fortsatt låga risker efter negativt provsvar. Vidare har det enda laboratoriet som inte infört vätskebaserad cytologi under perioden (Uppsala) också en numerär ökning av cancerinsjuknande efter normalt prov (Tabell 1).
Utredning för att hitta och åtgärda orsakerna
Den exakta orsaken till minskat cancerskydd efter normalt provsvar är inte känd. I samarbete med Kvalitetsgruppen inom klinisk cytologi (KVAST) kommer därför alla data om omgranskning av prov tagna före diagnos av cancer och höggradig cellförändring att begäras in och sammanställas för en nationell analys med syfte att närmare belysa den exakta orsaken. Denna genomgång kan leda till slutsatser huruvida det finns problem med provtagning, processen att framställa objektsglas (inga avvikande celler på glaset) eller i diagnostiken (fler missade avvikande celler än tidigare). Vidare kommer ökningen av höggradig cellförändring i screeningintervallet före cancerinsjuknande att utredas. Det fortsatta arbetet är nödvändigt för att kunna identifiera och åtgärda problemen.
Skyddseffekt av normalt prov fortsatt mycket hög
Skyddseffekten av ett normalt screeningprov är, trots den nu rapporterade försämringen, fortfarande mycket hög. Årligen har > 600 000 gynekologiska cellprov normala provsvar, och att cancer påvisas i nästa screeningintervall efter normalt cellprov är sällsynt (under 2002–2013 för 0,020 procent av dessa prov och för 2014–2015 för 0,026 procent av proven). De flesta cancerfall uppstår fortfarande hos kvinnor som inte deltagit i screeningen. Även under 2014–2015 hade endast ca 160/550 cancerfall uppstått hos kvinnor som deltagit och fått normala provsvar.
Socialstyrelsen har rekommenderat en ny primär metod för screening för livmoderhalscancer (där analys för HPV ingår) som har högre känslighet [5]. Metoden har hittills införts i sju landsting och samtliga landsting rapporterar att övergång planeras, i de flesta fall under 2018. Detta kommer att vara en viktig del i arbetet för att säkerställa en maximal säkerhet av programmet.
Potentiella bindningar eller jävsförhållanden: Joakim Dillner har tidigare varit mottagare av anslag från Merck och Sanofi Pasteur MSD för forskning om HPV-vaccin.