Hypokomplementemiskt urtikariellt vaskulitsyndrom (HUVS) är en sällsynt men potentiellt allvarlig immunkomplexmedierad vaskulit.
Hudbiopsi, inklusive immunfluorescensmikroskopi, är en central del av utredningen, och förekomst av antikroppar mot komplementproteinet 1q (anti-C1q) har hög sensitivitet för HUVS.
En ny svensk studie visar att den årliga incidensen av HUVS är 0,7 fall per miljon invånare (95 procents konfidensintervall 0,4–1,1). Tillståndet är vanligare bland kvinnor än bland män.
Allvarligt njurengagemang med glomerulonefrit eller lungengagemang med obstruktiv bild är inte ovanligt och understryker behovet av klinisk vaksamhet för tillståndet, noggrann utredning och vid misstanke kontakt med reumatolog.
Hypokomplementemiskt urtikariellt vaskulitsyndrom (HUVS) beskrevs första gången 1973 [1]. Tillståndet har länge betraktats som en separat immunkomplexmedierad autoimmun sjukdom med oklar etiologi, som utöver hudengagemang har potential att engagera leder, njurar, ögon och buk [2]. Därutöver är lungengagemang med spirometriska fynd som vid kroniskt obstruktiv lungsjukdom (KOL) vanligt förekommande och utgör även en ledande orsak till ökad dödlighet [3-6].
Stansbiopsi från urtikariella lesioner i hud, helst med immunfluorescensmikroskopi för att påvisa depositioner av komplement, är grundläggande i utredningen. Förekomsten av autoantikroppar mot komplementproteinet C1q (anti-C1q) har föreslagits vara »en regel utan undantag« [7].
Kunskapen om sjukdomens förekomst, kliniska manifestationer, prognos och behandling är ännu ofullständig och försvåras av den ibland ospecifika kliniska bilden som kan imitera andra inflammatoriska sjukdomar. Frånvaron av en unik ICD-kod försvårar epidemiologiska studier av tillståndet. Den hittills största studien är en riksomfattande fransk retrospektiv kohortstudie med 57 fall inklusive kliniska data och laboratoriefynd samt medicinsk behandling [6].
År 2018 publicerade vi epidemiologiska och kliniska karakteristika kopplade till HUVS från befolkningen i Skåne och Östergötland med en 16-årig rekryteringsperiod och en medianuppföljningstid av 94 månader [8].
Nomenklatur
Vid 2012 års konsensusmöte i Chapel Hill reviderades indelningen av vaskuliter [5]. Enligt Chapel Hill tillhör HUVS gruppen »immunkomplexmedierade småkärlsvaskuliter«, men termen »anti-C1q-vaskulit« adderades för att understryka betydelsen av denna autoantikropp vid tillståndet. HUVS definieras av ≥6 månaders urtikaria i kombination med låga komplementnivåer samt biopsiverifierad småkärlsvaskulit, glomerulonefrit, artrit, episklerit/uveit eller KOL [3].
Blodprov och biopsifynd
Typiska laboratoriefynd vid HUVS är låga nivåer av komplementproteiner (minst en av C1q, C3 och C4) eller reducerad klassisk komplementfunktion. Anti-C1q kan i regel påvisas. Målantigenet för anti-C1q vid HUVS skiljer sig vanligen från de anti-C1q-antikroppar som påvisas hos ca 30 procent av patienter med systemisk lupus erythematosus (SLE) och vars förekomst ofta är associerad med nefrit [9]. Anti-C1q vid SLE detekteras i regel endast med ELISA-teknik och binder inte separerade C1q-proteinkedjor, till skillnad från antikropparna vid HUVS, som förutom att binda den kollagenlika delen av C1q (ELISA) ofta även binder C1q B- och C-proteinkedjor och därigenom går att detektera med Western blot-teknik [10].
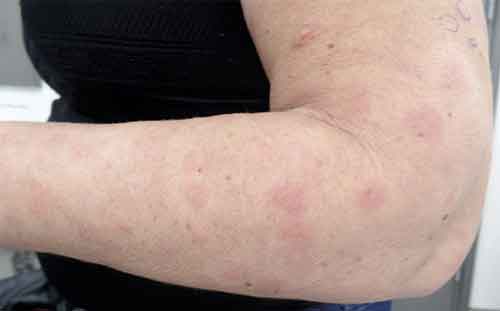
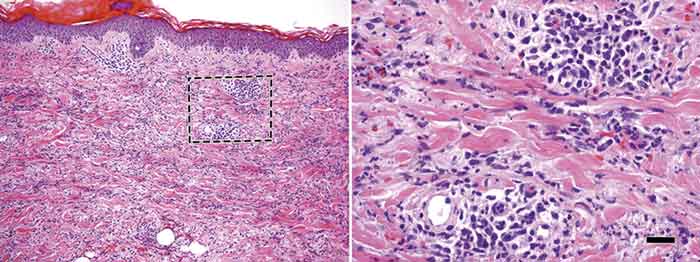
Hudbiopsi är väsentlig när HUVS-diagnosen ställs. Från typiska urtikariella utslag ses histopatologiskt vaskulit som engagerar små blodkärl (dvs kapillärer, venoler eller arterioler), ofta med leukocytoklasi (kärnsönderfall) och perivaskulära, neutrofila infiltrat (Figur 1) [2, 11]. Med immunfluorescensmikroskopi ses komplementkomponenter från den klassiska vägen (C1q, C3 och C4) i vävnad som uttryck för klassisk komplementfunktion, vilket ytterligare stärker diagnosen. Histopatologin vid njurengagemang av HUVS går inte att särskilja från den som ses vid proliferativ SLE-nefrit.
Svensk studie av HUVS
Vår svenska studie av HUVS, vars studieprotokoll genomgått erforderlig etikprövning, baseras på data från journaler och laboratorieregister. Samtliga nydiagnostiserade fall av HUVS i Skåne och Östergötland under åren 2000–2015 identifierades via reumatologklinikerna vid Skånes respektive Linköpings universitetssjukhus [8]. Registret vid Klinisk immunologi och Transfusionsmedicin, Lund, där alla C1q- och anti-C1q-analyser för bägge regionerna utförts sedan 1980-talet utgjorde en kompletterande datakälla.
Ur journaler från alla fall med positivt anti-C1q-test under åren 2000 till 2015 inhämtades uppgift om diagnos och kliniska manifestationer. Fall av klinisk SLE-diagnos uteslöts, och endast fall som uppfyllde samtliga nedanstående kriterier för HUVS inkluderades:
- minst ett positivt anti-C1q-antikroppstest (ELISA)
- patienten var mantalsskriven inom en av regionerna vid tidpunkten för HUVS-diagnos
- HUVS-diagnosen var baserad på Chapel Hill-definitionen och/eller typiska urtikariella hudlesioner kombinerade med låga nivåer av klassiska komplementproteiner i cirkulationen och minst två av följande manifestationer: biopsiverifierad hudvaskulit, artrit, glomerulonefrit, episklerit/uveit eller återkommande buksmärta.
Åren 2000–2015 identifierades 16 patienter med HUVS, varav 14 kvinnor (88 procent). Kliniska uppgifter insamlade från diagnosdag fram till den 31 december 2015 (eller död) sammanfattas i Tabell 1. Medianålder för diagnos var 51 år (kvartilavstånd [IQR] 40,7–56,7). Mediantid för uppföljning var 94 månader (IQR 46,5–136,2) och medianålder vid sista uppföljningen (n = 14) var 58 år (IQR 45,0–65,7). Mediantid av diagnosfördröjning, definierat som tid från första symtom relaterat till HUVS fram till diagnos, var 12 månader (IQR 5,0–19,7).
Diagnosen baserades på biopsi (hud eller njure) i majoriteten av fallen (81 procent), och 15 av 16 (94 procent) hade reducerade nivåer av klassiska komplementproteiner i serum eller plasma. Alla patienter testades positivt för anti-C1q med ELISA minst en gång under studietiden, medan Western blot utfördes hos 15 av 16, och bekräftades positivt hos 9 av dem (60 procent).
Kliniska manifestationer. Vid tidpunkten för diagnos var de vanligaste kliniska manifestationerna urtikaria (100 procent) följt av artrit (88 procent), biopsiverifierad glomerulonefrit, episklerit/uveit och dyspné (19 procent vardera) samt återkommande buksmärtor (13 procent). Den ackumulerade frekvensen av organengagemang under uppföljning var följande: urtikaria (100 procent), artrit (88 procent) och lungengagemang (63 procent). Den vanligaste inledande medicinska behandlingen var kortison (88 procent) följt av hydroxiklorokin (56 procent), mykofenolsyra (31 procent) och azatioprin (19 procent). Mediandos prednisolon vid diagnos var 30 mg/dygn (IQR 15–40).
Under uppföljningen diagnostiserades 8 av 16 patienter (50 procent) med KOL (enligt GOLD-kriterierna), varav 6 även med lungemfysem (38 procent). KOL-frekvensen är i linje med vad som tidigare rapporterats [4]. Av de patienter som erhöll KOL-diagnos var 5 rökare vid tidpunkten för HUVS-diagnosen, 2 var före detta rökare och 1 patient hade aldrig rökt.
En exrökande man, diagnostiserad med KOL och lungemfysem, genomgick lungtransplantation 22 månader efter HUVS-diagnosen. 2 patienter med njurengagemang utvecklade terminal njursvikt 36 respektive 49 månader efter att de erhållit HUVS-diagnos. Ingen av de 16 patienterna utvecklade SLE baserat på klassifikationskriterier under uppföljningstiden [12].
2 patienter avled under uppföljningsperioden: en 57-årig kvinna dog till följd av respiratorisk insufficiens, sepsis och njursvikt 52 månader efter sin HUVS-diagnos, och en 72-årig kvinna avled till följd av njursvikt efter 65 månader.
Förekomst. Den genomsnittliga årliga incidensen per miljon invånare uppskattades till 0,7 (95 procents konfidensintervall [95KI] 0,4–1,1) och var signifikant högre bland kvinnor än män (1,3 [95KI 0,6–1,9] mot 0,2 [95KI 0–0,4]; P = 0,003). Incidensen var något högre i Östergötland än i Skåne: 1,3 per miljon invånare (95KI 0,5–2,2) mot 0,5 (95KI 0,1–0,8); P = 0,03. Incidensen per år var stabil under hela studietiden. Vid slutuppföljning var 14/16 patienter fortfarande vid liv, vilket resulterade i en punktprevalens per miljon invånare på 9,5 (95KI 4,5–14,5) för alla patienter: 16,2 (95KI 7–25,4) för kvinnor och 2,7 (95KI 0–6,5) för män; P = 0,007. Prevalensen skiljde sig inte signifikant åt mellan Skåne och Östergötland. Den 1-, 5- och 10-åriga överlevnaden estimerades till 100 procent, 92 procent respektive 83 procent.
Sammanfattning
Våra resultat, baserade på 16 års data av anti-C1q-positiva fall från två svenska regioner med ett totalt upptagningsområde på ca 1,5 miljoner, indikerar att HUVS är ett sällsynt men ibland allvarligt tillstånd [8]. Svårt lung- och njurengagemang med organsvikt observerades i vissa fall.
Hos individer med oförklarat förhöjda inflammationsparametrar kombinerat med långvarig urtikaria bör HUVS uteslutas, gärna i samråd med reumatolog. Särskild uppmärksamhet förtjänar patienter med nytillkommen dyspné och proteinuri. Hudbiopsi, helst med immunfluorescensmikroskopi, utgör en viktig del av utredningen. Sänkt klassisk komplementfunktion, alternativt låga nivåer av komplementproteiner (C1q, C3 eller C4), stärker misstanken om HUVS, och anti-C1q-antikroppar kan i regel påvisas.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.