Samtliga regioner har inlett screening för kolorektalcancer i åldersgrupperna 60–74 år.
Införandet planeras vara klart 2026 och omfattar cirka 1,65 miljoner personer.
Screeningen sker vartannat år genom test av fekalt Hb med koloskopi vid positivt test.
Screening beräknas minska mortaliteten i kolorektalcancer med minst 300 fall per år.
Under perioden april 2021 till september 2022 inledde samtliga regioner screening för kolorektalcancer. Införandet beräknas vara slutfört hösten 2026, då cirka 1,65 miljoner medborgare i åldersklasserna 60–74 år ska ha erbjudits att delta. Här beskrivs översiktligt bakgrunden till och utformningen av screeningprogrammet.
Bakgrund
I Sverige insjuknar cirka 6 700 personer årligen i kolorektalcancer, den tredje vanligaste cancerformen. Den cancerspecifika 5-årsöverlevnaden är cirka 65 procent, men är uttalat stadiumberoende: drygt 95 procent i stadium I, men cirka 20 procent i stadium IV. Samtidigt uppfyller kolorektalcancer samtliga 10 kriterier för screening, definierade av Världshälsoorganisationen redan 1968 [1] och kompletterade av Socialstyrelsen ur ett svenskt sjukvårdsperspektiv [2].
2003 rekommenderade EU screening för kolorektalcancer i åldersgrupperna 50–74 år [3]. Stockholm och Gotland startade 2008‒2009 en organiserad populationsbaserad screening med guajakbaserat F-Hb-test för åldersklasserna 60–69 år. 2014 rekommenderade Socialstyrelsen screening med F-Hb-test för åldersklasserna 60–74 år vartannat år [4]. 2017 föreslog Regionalt cancercentrum syd F-Hb-baserad screening för åldersklasserna 50–74 år [5]. 2018 publicerade Regionala cancercentrum i samverkan konkreta förslag till utformningen av screening [6].
Internationellt finns screeningprogram i flertalet europeiska länder, i Nordamerika och delar av Sydamerika samt i ekonomiskt utvecklade länder i Asien [7].
Principer
Screening för kolorektalcancer erbjuds till samtliga i en definierad population utan selektion. Identifierade högriskindivider med till exempel hereditet, tidigare kolorektalcancer, inflammatorisk tarmsjukdom och polypossjukdomar ska däremot kontrolleras via särskilda uppföljningsprogram. Screeningens syfte är primärt att påvisa cancer i tidigare, asymtomatiska stadier och sekundärt att identifiera och avlägsna polyper (förstadier). Screeningen minskar därmed både mortalitet och incidens.
Principiellt skiljer man på organiserad, populationsbaserad screening och opportunistisk dito. Organiserad screening erbjuder aktivt samtliga medborgare i definierade åldersgrupper deltagande i ett strukturerat program med planerad uppföljning och kvalitetskontroll. Opportunistisk screening bygger däremot på att samhället tillhandahåller screeningmöjligheter, men den enskilde får initiera deltagande. Det medför risk för överscreening av lågriskindivider, och vanligen saknas strukturerad kontroll av kvalitet och resultat.
Screeningmetoder
För populationsscreening av kolorektalcancer har sigmoideoskopi, koloskopi och kontroll av F-Hb, där koloskopi erbjuds dem med positivt test, studerats ingående. Varje metod har för- och nackdelar, men en jämförelse faller utanför den här artikelns omfattning [8, 9]. Koloskopi betraktas ofta som referensmetoden, då polyper exstirperas direkt och eventuell cancer diagnostiseras under samma ingrepp, men den är resurskrävande och uppfattas av många som obehaglig, varför deltagandefrekvensen är relativt låg.
Internationellt dominerar därför screening med F-Hb-test följt av koloskopi vid positivt utslag, och detta är också den metod som har införts i Sverige. Genom upprepad testning vartannat år kan cancer och polyper som blöder mindre volymer eller intermittent upptäckas tidigare.
Fekalt hemoglobintest
Tidigare användes guajakbaserade test för påvisande av F-Hb, vilket detekterar hemdelen i Hb-molekylen. Nackdelarna är dock flera, främst att testet reagerar även på icke-humant hem, vilket kräver dietrestriktioner, tre olika provomgångar samt att testet är kvalitativt. Det har därför ersatts av fekalt immunkemiskt test (FIT), som detekterar den humana globindelen. FIT kräver enbart ett prov, har inga dietrestriktioner, är kvantitativt samt har överlägsna testdata jämfört med guajakbaserade F-Hb-test [10].
Gränsvärdet för FIT mäts i µg Hb/g feces och kan justeras för att få balans mellan falska och sanna testresultat, och hänsyn kan därmed tas till koloskopiresurserna. Vid gränsvärdet 20 µg Hb/g är sensitiviteten för kolorektalcancer 75 procent och specificiteten 95 procent, enligt metaanalyser [11].
Förutom storleken på tumörer och polyper inverkar flera faktorer på F-Hb-volymerna, bland annat kön och ålder [12, 13]. I Sverige, som ett av få länder, används därför könsdifferentierade gränsvärden, med 40 µg Hb/g feces för kvinnor respektive 80 µg Hb/g för män [14, 15].
Effekt
Screeningprogrammets effektivitet är avhängig flera faktorer, främst deltagandet över tid och koloskopikvaliteten. I Stockholm och Gotland är deltagandet nu 71 procent, vilket är högt jämfört med flera europeiska länder som ligger på 29‒73 procent, dock med olika programutformningar [16, 17]. Värderingar av populationseffekten måste beakta om den avser kumulativ testning eller enbart första testomgången och om den är beräknad på hela den inbjudna populationen (intention to screen) eller den andel som verkligen testade sig (screening per protocol).
En metaanalys av de första 4 randomiserade kontrollerade studierna av screening med guajakbaserade F-Hb-test (en från Göteborg [18]) visade en mortalitetsreduktion på 15 procent vid »intention to screen« respektive 25 procent vid »screening per protocol« [19]. På basen av detta beräknade Socialstyrelsen att minst 300 årliga dödsfall i kolorektalcancer kan undvikas [4]. Med FIT:s bättre egenskaper kan mortaliteten rimligen minska ytterligare. Observationsstudier av screening med FIT styrker detta; dock har de skiftande upplägg och är inte helt jämförbara. Till exempel har en amerikansk studie visat en minskning av incidensen med 25 procent och mortaliteten med 52 procent [20]. Från Taiwan rapporteras en sänkning av incidensen med 34 procent och mortaliteten med 40 procent (vid stadium II‒IV, baserad på drygt 5,4 miljoner personer) [21]. I Nederländerna har incidensen minskat från 214,3 till 181,5 och mortaliteten från 87,5 till 64,8 per 100 000 personer [22]. Från Belgien rapporteras en incidenssänkning från 152,7 till 115,2 per 100 000 personer och en 5-årsöverlevnad hos screeningupptäckta fall på 93,8 procent, jämfört med 66,7 procent hos symtomatiska [23]. En mindre metaanalys av tidiga studier med FIT beräknade en sänkning av incidensen med 21 procent och mortaliteten med 59 procent [24].
I Stockholm‒Gotlandsprogrammet har man observerat 2,7 procent FIT-positiva, av vilka 6,9 procent hade kolorektalcancer och 30 procent högriskadenom [14]. En analys av incidens och mortalitet för kolorektalcancer har inletts.
Organisation
Screeningen för kolorektalcancer är den första nationellt samordnade cancerscreeningen i Sverige. Samtliga regioner har slutit avtal med Gemensamt samordningskansli (GSK) hos Region Stockholm. GSK tillhandahåller samordningssjuksköterskor som bland annat besvarar medborgarnas frågor, datasystem, utskick av erbjudandebrev med provtagningsmateriel och påminnelsebrev samt centraliserad FIT-analys. Nationell samordning av information och kommunikation sker också, bland annat via 1177 Vårdguiden. En viktig aspekt är att den testade förstår att ett positivt FIT oftast inte innebär kolorektalcancer och att ett negativt FIT inte utesluter den.
Den enskilda regionen bestämmer vilka åldersklasser den vill bjuda in vilket år, utformar tilläggsinformation samt ansvarar för koloskopier av dem med positivt FIT. Specialutbildade screeningsjuksköterskor på regionernas screeningendoskopienheter sköter kontakten med patienterna och administrationen.
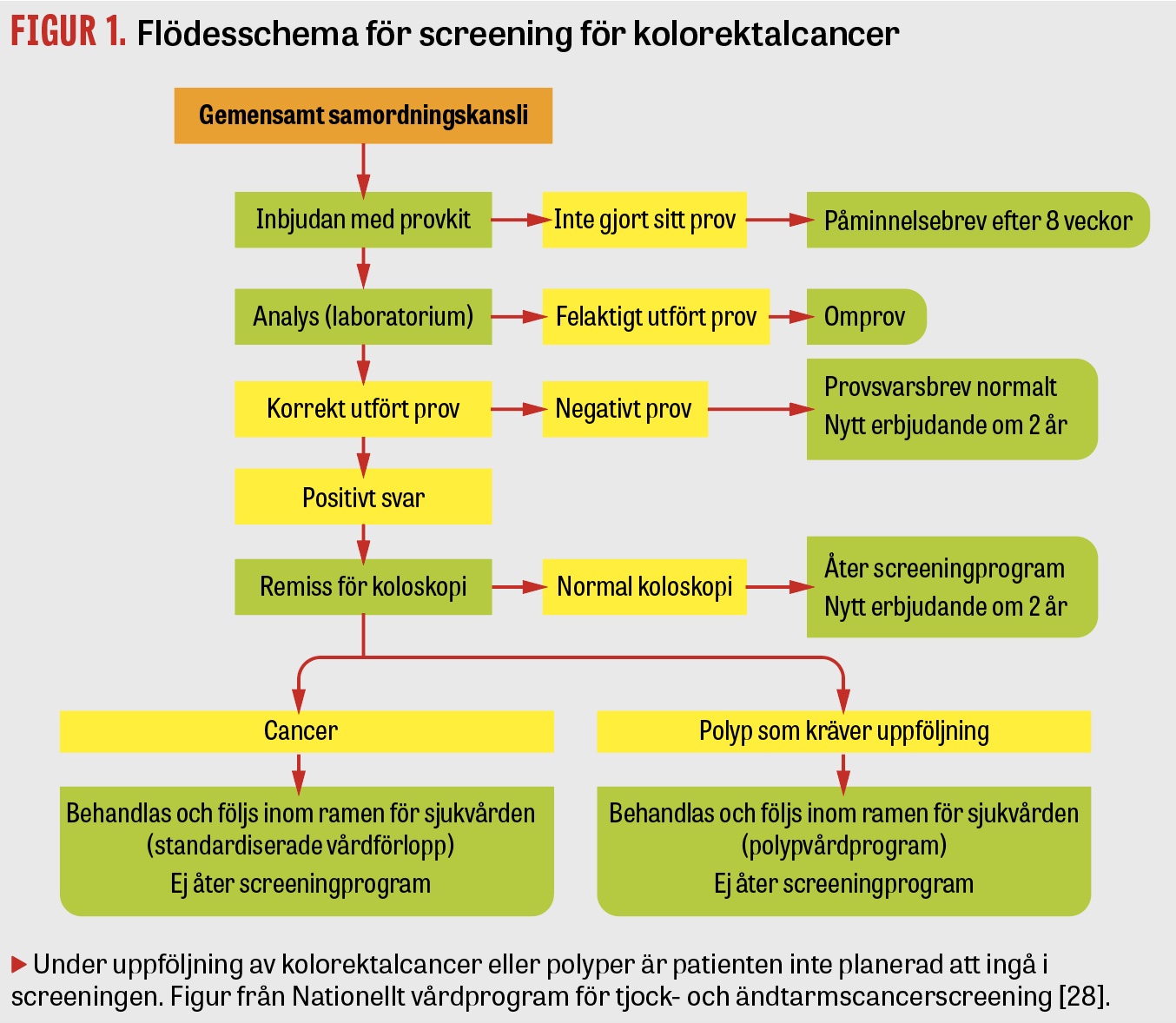
Ett nationellt kvalitetsregister, Svenskt register för koloskopier och kolorektalcancerscreening (Sverekks), startade våren 2019 [25]. Anslutning till registret är en förutsättning för att starta screening och borgar för en kontinuerlig kvalitetskontroll med återkoppling till både skopienhet och koloskopist. Registret innefattar Socialstyrelsens kvalitetsindikatorer [26] och kraven för högkvalitativ koloskopi, vilka är en grundbult för hög screeningeffekt [27]. Det översiktliga flödet i screeningprogrammet visas i Figur 1.
Ett nationellt vårdprogram för tjock- och ändtarmscancerscreening fastställdes av Regionala cancercentrum i samverkan i september 2022 [28].
Framtiden
Vad som är en optimal nedre åldersgräns för kolorektalcancerscreening diskuteras internationellt. Flertalet länder har 50 år [7], och i USA rekommenderar flera instanser 45 år [29, 30]. Framför allt koloskopiresurserna är avgörande för om åldersgränsen bör sänkas i Sverige.
Justeringar av gränsvärdet för FIT diskuteras också [13]. Enkelt uttryckt medför ett lägre gränsvärde fler både sant och falskt positiva utslag, men det viktigaste är att minimera frekvensen av intervallcancer (kolorektalcancer mellan screeningtillfällena), det vill säga falskt negativa resultat. Patienter med falskt positiva resultat erbjuds ju koloskopi och blir korrekt diagnostiserade, men de med falskt negativa resultat undersöks inte vidare. Samtidigt måste koloskopiresurser och undanträngningseffekter vägas in.
Screeningprogrammet är »blint«, då endast ålder och kön är kända. Forskning pågår om riskstratifiering som skulle väga in individuella riskfaktorer, till exempel rökning och obesitas, för att bland annat erbjuda olika screeningintervall [31]. Dessa data måste då hämtas från medborgarna eller journalsystem. Ett enklare förslag är att riskstratifiera baserat på ålder, kön och tidigare FIT-resultat [32].
Studier pågår i Sverige med »geomapping«, som lokaliserar områden med hög incidens, där invånare kan behöva ökad och mer riktad information om screeningprogrammet [33].
Det som nu prioriteras högst är att programmet införs fullt ut, att högt deltagande uppnås i hela landet och att den fortlöpande kontrollen håller hög kvalitet.
Läs även: Författarintervjun med Birger Pålsson
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Birger Pålsson är f d ordförande för den nationella arbetsgruppen för tjock- och ändtarmscancerscreening.
(uppdaterad 2023-07-18)