Diagnostiska nanopartiklar kan kraftigt förbättra avbildningstekniker och diagnossystem för bland annat cancer och hjärt–kärlsjukdomar.
Vägen dit är komplicerad vad beträffar design, funktion, kommersiell produktion, säkerhet och reglering.
Att designa målsökande nanopartiklar för anrikning i de celler eller den vävnad som ska diagnostiseras är en viktig forsknings- och utvecklingsutmaning.
Relativt få produkter/processer är ännu godkända för klinisk användning.
Biomarkörer är indikatorer på friska eller sjukliga biologiska processer och förutsätter extremt känsliga analysmetoder. Exempel ges på proteinmatriser (protein arrays) och enmolekyldiagnostik.
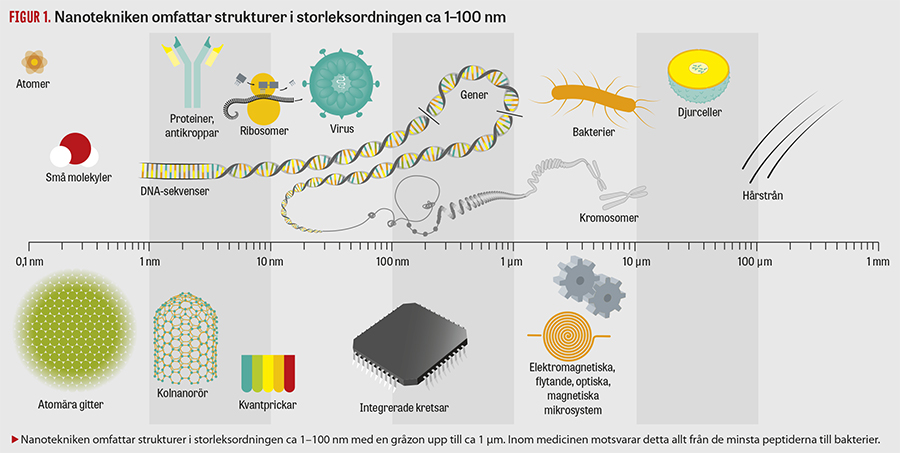
I »European technology platform on nanomedicine« (ETPN) ingår tre huvudområden: diagnostik, avbildning samt terapi (läkemedel, implantat och regenerativ medicin), vilka alla förutspås bidra till förbättrad prevention och behandling av sjukdomar [1]. Nanotekniken definieras oftast baserat på storleken hos de funktionella byggstenarna i nanoprodukterna, vilka inbegriper storleksområdet 1 till ca 100 nm med en gråzon upp till mikrometerskalan (ca 1 000 nm). Inom medicinen matchar dessa storleksmässigt allt från de minsta peptiderna till virus, bakterier och till viss del också cellers olika organeller och strukturer (Figur 1), vilka alla är viktiga målstrukturer inom nanomedicinska tillämpningar.
Forsknings- och utvecklingsverksamheten har som övergripande mål att med förbättrad precision och pålitlighet kunna identifiera de enskilda individer som löper ökad risk för sjukdom och att kunna diagnostisera sjukdom mycket tidigt i förloppet. Merparten av denna utveckling ligger fortfarande på laboratorie- och preklinisk nivå, där mängder av nya koncept är under snabb utveckling [2-4]. Detta illustreras till exempel av att antalet nanomaterial och processer godkända av den amerikanska läkemedelsmyndigheten FDA fortfarande är relativt litet [2].
Även om den stora effekten av nanomedicin bedöms komma successivt under de närmsta tio eller kanske tiotals åren, så gör nanomedicinska produkter som ännu inte är kliniskt godkända redan stor nytta inom den medicinska utvecklingen. Nya mättekniska koncept bidrar till exempel till in vitro-diagnostik och vid utvärdering av diagnostik och terapi vid djurförsök, medan tidsskalan för klinisk användning av nanopartiklar i hög grad är kopplad till säkerhets- och riskaspekter (se separat artikel i detta tema).
Nanoteknik för medicinsk diagnostik är ett så stort kunskapsområde att alla dess aspekter inte ryms inom ramen för denna artikel. Här ges i stället en översikt av hur nanotekniken skapar nya möjligheter för avbildnings- och diagnosmetoder, med ett avslutande exempel på hur diagnostik med enmolekylkänslighet är på väg att nå kliniken. Viktiga områden som inte tas upp, även om nanotekniken spås få stor betydelse där, är implanterbara biosensorer och portabla diagnostiska kit designade för användning i tredje världen eller i katastrofsituationer.
Avbildningstekniker och diagnostik
Nano- och mikropartiklar som används för avbildning varierar i storlek från 1 nm upp till 1 µm. Som beskrivs på annan plats i detta temanummer finns det ett brett spektrum av nanopartiklar, vilkas egenskaper varierar med exempelvis storlek, form, grundmaterial, yta, laddning och löslighet. Viktiga avbildningstekniker där nanopartiklar har stor potential är röntgenavbildning (inklusive DT), magnetisk resonanstomografi samt olika typer av optisk avbildning [3-6]. Nanopartiklar kan ge förbättrade prestanda för dessa tre, men även för andra avbildningsmetoder såsom PET och SPECT. Användning av nanopartiklar bygger på den grundläggande principen att de fungerar som kontrast- eller signalförstärkare genom att påverka växelverkan mellan den externa, avbildande strålningen och de strukturer som ska avbildas samt att nanopartiklarna genom kemiska eller biologiska modifieringar kan göras målsökande.
I röntgenavbildning ges kontrasten av elektrontätheten i de atomer (och molekyler) som används som kontrastmedel, vilket betyder att tyngre atomer (högt atomnummer) ger högre kontrast. Detta – och det faktum att de hör till de mest utvecklade nanopartiklarna vad gäller kontroll av storlek, form, kemisk ytfunktionalitet med mera – gör att guldnanopartiklar för närvarande tillhör de mest intressanta kontrastnanopartiklarna [7]. En lång rad andra tunga ämnen kan dock komma att användas längre fram, och många är under utveckling [5, 6]. Förutom signalstyrka och kontrast måste man samtidigt optimera kombinationen av röntgenstrålningens våglängd (kvantenergi), intensitet och partiklarnas storlek för att minimera skadorna av strålningen och dess sekundära effekter, till exempel elektronemission från nanopartiklar. Därtill måste utsöndringsförlopp och/eller metabol nedbrytning av partiklarna kartläggas och kontrolleras.
Gemensamt för design och utveckling av nanopartiklar som avbildningshjälpmedel är att man oftast på något sätt (undantag finns) gör dem målsökande, det vill säga väljer eller modifierar dem så att de binder till och anrikas i den vävnad eller celltyp som ska avbildas och diagnostiseras. Det senare kan ske på många olika sätt; i tumörer kan anrikning ske tack vare den så kallade EPR (enhanced permeability and retention)-effekten, i andra fall krävs mer sofistikerade målsökande nanopartiklar som med hjälp av bindningsmolekyler (till exempel antikroppar) på ytan specifikt och selektivt binder till den typ av celler eller vävnad som ska avbildas (Figur 2). Storlek och ytkemi kan till exempel användas för att styra endocytos, det vill säga upptag i celler, eller partiklarnas framkomlighet i extracellulär vävnad.
Nedan går vi något mer ingående igenom några centrala avbildningsprinciper för identifiering av nanopartiklar inom diagnostik in vivo.
Datortomografi. Modaliteten har utvecklats under senare år, och i dag finns teknik tillgänglig som möjliggör avbildning av vävnad med så kallad dubbelenergiteknik (dual-energy computed tomography, DECT). Tekniken tillåter samtidig avbildning med två röntgenenergier, vilket gör det möjligt att bättre diskriminera mellan olika vävnader och erhålla ökad information om vävnadens kemiska sammansättning jämfört med undersökning med en enda röntgenenergi. Tekniken möjliggör också framtida användande av nya nanopartikelkontrastmedel. Inom tre till fem år förväntas nya så kallade fotonräknande detektorer finnas tillgängliga för DT och komma till användning i kliniskt bruk. Dessa kommer att ge möjlighet att kvantitativt avbilda enskilda grundämnen med påtagligt högre upplösning och med reducerad stråldos. Pågående forskning med nanopartikelkontrastmedel som samtidigt har luminiscenta, magnetiska och röntgenabsorberande egenskaper har visat lovande prekliniska resultat. Denna forskning ger förhoppning om att i framtiden kunna använda samma nanopartiklar som kontrastmedel vid både magnetresonanstomografi (se nedan) och DECT-undersökningar. Den fluorescerande funktionen kan göra tumören synlig och möjlig att avgränsa från omgivande vävnad vid operativa ingrepp [8, 9].
Magnetresonanstomografi. I den fysikaliska nomenklaturen benämns denna princip »nuclear magnetic resonance«, NMR. Avbildningen sker via resonansväxelverkan mellan atomkärnors, oftast protoners (vätekärnors), magnetiska moment (kärnspinn) och yttre magnetfält, inklusive mätning av olika relaxationstider för de magnetiskt exciterade kärnorna [5]. Nanopartiklar med lämpliga magnetiska egenskaper kan påverka nämnda relaxationsprocesser så att den lokala kontrasten och bildsignalen förbättras. Lämpliga nanopartiklar för detta innebär i regel att de har superparamagnetiska egenskaper som ger stark växelverkan med det yttre magnetfältet och med protonernas magnetiska moment, utan att ha egen permanent magnetism. Nanopartiklar av vissa järnoxider, till exempel magnetit (Fe3O4), har sådana egenskaper. Nanopartiklarna görs oftast biokompatibla och målsökande (undantag för det senare gäller vid till exempel flödes- och cirkulationsmätningar) genom att de förses dels med ett skyddande, hydrofilt polymerskal, dels med bindningsmolekyler (Figur 2). De senare gör att partiklarna selektivt binder till specifika celler eller vävnader, vilket medför en anrikning av partiklar i det område man önskar avbilda.
Optisk avbildning. Optisk avbildning har ett mycket grundare avkänningsdjup än röntgen eller magnetresonanstomografi; de senare penetrerar hela kroppen, medan optisk avbildning bara når några mikrometer till några millimeter djupt beroende på våglängd och vävnadstyp [5]. Optisk avbildning har ändå stor användbarhet, dels för hudskiktsavbildning, dels i inre delar av kroppen med hjälp av fiberoptik och för vävnadsprov ex vivo. Anrikning av optiskt aktiva partiklar sker på samma sätt som vid röntgen eller magnetresonanstomografi, det vill säga med hjälp av aktiv och selektiv inbindning till de celler och den vävnad som ska avbildas. Den optiska förstärkningen kan till exempel ske genom att vanliga färgämnesmolekyler (som exempelvis används vid konventionell fluorescensmikrosopi) ersätts med så kallade kvantprickar (quantum dots). De senare har högre fluorescenstvärsnitt och bleks/åldras mycket långsammare, men är svårare att hantera. Man kan också få avbildningsförstärkning med hjälp av så kallade nanoplasmoniska effekter som förstärker ljusfältet i närheten av till exempel guld- och silvernanopartiklar. Ytterligare ett exempel ges under avsnittet om en-molekyldiagnostik nedan.
Teranostik. För samtliga typer av avbildning med hjälp av nanopartiklar gäller att partiklarna oftast förses med ett skyddande, biokompatibelt skal och dessutom specifika bindningsmolekyler som ska göra att partikeln binds enbart till önskad typ av celler eller vävnad. Steget är då inte långt till att förse nanopartikeln med ytterligare en funktion, nämligen en last av läkemedel (Figur 2). Det kan ske på olika sätt, till exempel genom att koppla ihop två typer av nanopartiklar eller genom att en enskild nanopartikel byggs med en inre kärna av avbildningsförstärkaren plus ett första skal av läkemedel och ett ytterligare skal av ett skyddande hölje för att klara transporten till målet och dessutom specifikt målbindande molekyler. Sådana partiklar bidrar då till både terapi och diagnostik: de blir teranostiska [3] och kan följas i realtid både på sin väg mot målet och efter inbindning där läkemedelsfrisättning sker.
Svårigheter och hinder. De tekniska och medicinska hindren för att uppnå önskad funktionalitet och säkerhet med diagnostiska och avbildande nanopartiklar är betydande. En stor utmaning är att ge partiklarna rätt ytfunktionalitet, så att de dels överlever transporten via flöde och diffusion fram till målregionen, dels binder in där, och bara där, när de väl nått dit. För den första delen, transporten, måste partikeln motstå eller klara av att olika proteiner eller andra biomolekyler binder till ytan eller modifierar den via enzymatisk nedbrytning, så att den inte förlorar sin diagnostiska eller avbildande och inte minst målsökande funktion. Sådana oavsiktliga modifieringar är vanliga genom så kallad koronaeffekt eller opsonisering, varvid antikroppar, komplementproteiner eller andra biomolekyler kapslar in nanopartikeln, inklusive dess specifika bindningsmolekyler, och den målsökande effekten går förlorad [11]. Om väl dessa svårigheter lösts återstår det mödosamma arbetet att visa att partiklarna kan utsöndras eller brytas ner utan att ge oönskade bieffekter av den typ som beskrivs i en separat artikel om nanotoxikologi i detta tema.
In vitro-diagnostik baserad på biomarkörer
Medan den nanoteknologiska utvecklingen av in vivo-diagnostik domineras av nanopartiklar liknande dem som utvecklas som bärare av nanoläkemedel eller för avbildning så är in vitro-diagnostik av biomarkörer med så kallade proteinmatriser (protein arrays, protein chips) ett annat snabbt växande område [12, 13]. Biomarkörer är substanser som kan mätas objektivt och fungerar som indikatorer på normala eller sjukliga biologiska processer, liksom på hur en specifik behandling fungerar [14]. Genom att bestämma närvaron och koncentrationen av sådana biomarkörer, ofta olika proteiner, som bildas via ett speciellt genuttryck kan man få en mer precis bestämning av ett sjukdomstillstånd än genom att bara bestämma förändringar i genuttryck. En proteinmatris består av ett antal isolerade areor (punkter), som var och en är preparerad med en specifik igenkännings- eller infångningsmolekyl, till exempel en antikropp. När det prov som ska analyseras tillsätts, binder matchande typ av molekyl i provet till antikropparna på ytan (steg 1 i Figur 3, som illustrerar detektion av biomarkörer baserad på konventionell ELISA – enzymkopplad immunadsorberande analys). Om en sådan igenkänningshändelse sker så bildar de två växelverkande molekylerna ett par, till exempel antikropp–antigenpar (steg 2 i Figur 3). Avläsningen av att händelsen skett görs oftast optiskt med hjälp av fluorescenta prober, till exempel genom en sekundär antikropp som antingen är fluorescensmärkt eller modifierad med ett enzym som omvandlar ett substrat till en optiskt detekterbar produkt (steg 3 i Figur 3). I en proteinmatris är varje brunn i mikrotiterplattan i stället ersatt med en ca 100 µm2 stor punkt på en plan yta, vilket väsentligt ökar det antal olika biomarkörer som samtidigt kan detekteras i ett prov.
Proteinmatrismetoden är under snabb utveckling och används inom diagnostik, proteomik, funktionsanalys av proteiner, antikroppskarakterisering och för uppföljning av läkemedelsbehandling. Inom diagnostik är de vanligaste målen att identifiera/bestämma antikroppar i blodprov, identifiera koncentration eller förekomst av biomarkörer för sjukdomar, bestämma tillstånd och faser i sjukdomsförlopp eller mäta effekter av olika terapier vid sjukdomsbehandling [12, 13].
En av de största utmaningarna inom den här typen av diagnostik är att man samtidigt som man i många fall behöver kunna sänka detektionsgränsen, det vill säga kunna detektera extremt låga koncentrationer av relevanta biomarkörer, också måste lyckas öka antalet olika sjukdomsrelevanta biomarkörer som kan detekteras samtidigt, det vill säga öka multiplexkapaciteten. Den senare aspekten vinner på möjligheten att göra punkterna mindre och mindre. Om till exempel varje analyspunkt i en matris upptar ytan 100 × 100 nm2, vilket i dag är tekniskt möjligt, så blir antalet analysareor (punkter) på en kvadratcentimeter 10 miljarder. Denna förtjänst motverkas dock av att man får alltför låga signaler på grund av ytterst få detekterade molekyler per unik punkt. Man måste därför balansera multiplexkapaciten (många analysareor per ytenhet) mot den detektionsgräns man måste nå, vilken alltså kräver en viss minsta analysarea.
Enmolekyldiagnostik. Ett koncept, som framgångsrikt lyckats väga förtjänsten av miniatyrisering mot en ultrakänslig detektion av låga koncentrationer av biomarkörer, illustreras i Figur 4 [16]. Konceptet går ut på att blanda antikroppsdekorerade (jämför Figur 2), mikrometerstora magnetiska kulor med det prov som ska analyseras. Avancerade framställningsmetoder har gjort det möjligt att konstruera i stort sett defektfria sfärer, vilket i sin tur väsentligt reducerat den bakgrund som sätter gränsen för känsligheten i konventionella ELISA-test eller proteinmatriser. Efter inkubering av kulorna med provet och enzymmodifierade antikroppar används en magnet för att fiska ut dem, varefter de sprids på en yta som är perforerad med brunnar, vilka var och en är liten nog att bara rymma en magnetisk kula. Därefter tillsätts substrat till brunnarna som tillsluts med en plastfilm innan man undersöker om brunnarna lyser eller inte. Och det räcker faktiskt med ett enda enzym, det vill säga en biomarkör, per brunn för att en signal ska kunna detekteras.
Klinisk diagnostik kan dock inte baseras på att man hittar ett enda protein i en brunn, men eftersom varje platta innehåller tiotusentals brunnar (och därmed lika många kulor och därför sammantaget en väldigt stor sensoryta) får man ett mycket gott statistiskt underlag och har (genom att räkna proteiner ett och ett) lyckats påvisa en känslighet under 1 femtomolar (fM) [16]. Multiplexkapacitet, det vill säga samtidig detektion av flera olika biomarkörer, kan åstadkommas genom att använda magnetiska kulor modifierade med andra antikroppar snarare än genom flera analyspunkter på en matris, men är svår att genomföra parallellt. (För mer detaljerad beskrivning, se www.quanterix.com, webbplatsen för det företag som kommersialiserat konceptet.)
Sammanfattning
Forskningsaktiviteten inom in vivo-avbildning och in vitro-diagnostik ökar snabbt. För in vitro-applikationer kan vi vänta oss en löpande introduktion av nya metoder och produkter under såväl de närmast kommande åren som på längre sikt. På in vivo-området går utvecklingen långsammare på grund av utmaningar kring nanopartikelstabilitet, avläsning och säkerhetsaspekter, och där kommer sannolikt det stora genomslaget och den snabbaste utvecklingen om 5–10 år. Intensiv forskning pågår just nu kring olika nanoteknikbaserade koncept som ska göra det möjligt att med enmolekylkänslighet detektera biomarkörerna direkt när de binder till analyspunkten på en proteinmatris eller en fri nanopartikel. Alternativt kan detektion ske genom att den sekundära antikroppen (steg 3 i Figur 2) märks på ett sådant vis att den kan visualiseras direkt, till exempel genom nanometerstora guldkulor eller kvantprickar, som sprider eller sänder ut ljus mycket effektivt [17]. Vi kommer också att se nya nanopartikelbaserade in vitro-metoder som efter en tid utvecklas för att appliceras in vivo. Som ett avancerat exempel kan nämnas att fluorescerande molekyler släcks ut när de befinner sig inom några nanometers avstånd från en nanopartikel av guld. Sådana utsläckta fluorescensmärkta bindare, till exempel antikroppar, sinnrikt kopplade till guldkulor, kommer dock att lysa när de binder till en biomarkör eftersom de då frigörs från nanopartikeln. Med sådana nanopartiklar har man nyligen lyckats detektera biomarkörer såväl in vivo som inuti celler [18].
För att detta koncept, liksom många andra av de exempel som nämnts, ska nå kliniken är säkerhetsarbetet en nödvändig hämsko för produktutvecklingen. Det är därför svårt att bedöma när dessa kommer att lämna laboratoriemiljön. De senaste årens ökade interdisciplinära samverkan mellan fysiker, kemister, biologer, ingenjörer och medicinare är dock en absolut förutsättning för att de framsteg som sker inom materialvetenskap och nanoteknik en dag ska komma att göra skillnad inom medicinsk diagnostik.
Potentiella bindningar eller jävsförhållanden: Bengt Kasemo är delägare i och konsult till Insplorion som utvecklar och säljer mät- och sensorsystem baserade på plasmonisk sensing samt konsult till Biolin Scientific som ingår i AddLife; Fredrik Höök är delägare i Gothenburg Sensor Devices som äger och utvärderar den kommersiella potentialen hos vissa patent som tas fram i den forskargrupp han leder.





![Figur 2. Multifunktionell nanopartikel innehållande läkemedel, kontrastförstärkare och komponenter som ökar permeabiliteten genom vävnad eller celler. Ytan är modifierad med PEG (polyetylenglykol), vilket gör partikeln inert och ökar cirkulationstiden, samt målsökande molekyler, till exempel antikroppar. Från [10] med tillstånd från Macmillan Publishers Ltd.](https://lakartidningen.se/wp-content/uploads/EditorialFiles/AE/%5bEIAE%5d/wFig2.jpg)
![Figur 3. Principer för ELISA (enzymkopplad immunadsorberande analys). Ytan i mikrotiterplattans brunnar är modifierad med en antikropp som binder specifikt till det protein som ska detekteras i provet (steg 1). För att verifiera att proteinet bundit till den primära antikroppen på ytan tillsätts därefter en enzymmodifierad sekundär antikropp som binder specifikt till en annan del av proteinet (steg 2). Om brunnen sedan sköljs före tillsättande av enzymets substrat (steg 3) kommer enzymet att producera en detekterbar (ofta fluorescerande) produkt vars koncentration/intensitet är proportionell mot koncentrationen av det eftersökta proteinet i provet. I en proteinmatris ersätts brunnarna i mikrotiterplattan av mikrometerstora analyspunkter på en yta. Från [15] med tillstånd från American Chemical Society.](https://lakartidningen.se/wp-content/uploads/EditorialFiles/AE/%5bEIAE%5d/wFig3.jpg)
![Figur 4. a) Primär antikropp på magnetisk mikropartikel inkuberas med prov och enzymmodifierad sekundärantikropp (jämför ELISA i Figur 3). b) och c) Utsortering i brunnar och tillsättning av enzymsubstrat. d) Avläsning. Från [16] med tillstånd från Nature Publishing Group.](https://lakartidningen.se/wp-content/uploads/EditorialFiles/AE/%5bEIAE%5d/wFig4.jpg)

















