Atopiskt eksem är en av de vanligaste hudsjukdomarna i Sverige.
Patogenesen utgörs av ett samspel mellan en defekt hudbarriär och ett abnormt immunsvar.
Både den defekta hudbarriären och det avvikande immunologiska svaret kan orsakas av genetiska faktorer, miljöfaktorer eller en kombination av båda.
Atopiskt eksem har en påtaglig, negativ inverkan på hälsorelaterad livskvalitet.
Nya, mer specifika läkemedel är under utveckling. Inom en snar framtid kan vi förhoppningsvis erbjuda bättre behandling även av de svårare formerna av atopiskt eksem.
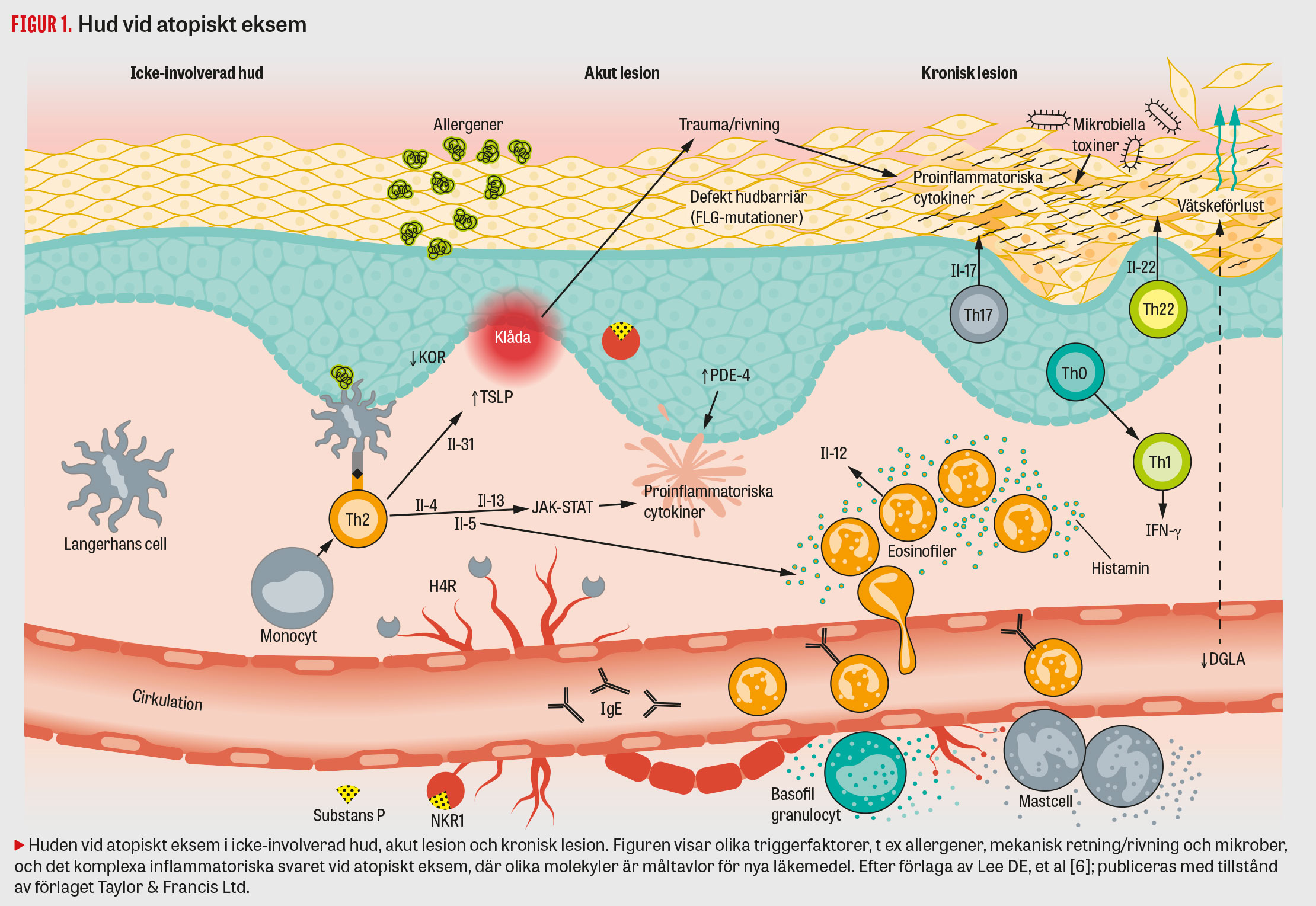
Figur 1
Atopiskt eksem/böjveckseksem/atopisk dermatit är en kronisk inflammatorisk, kliande hudsjukdom som vanligtvis debuterar i barndomen. Förekomsten har ökat, och sjukdomen drabbar minst 20 procent av barnen och ca 2–10 procent av vuxna [1].
Atopiskt eksem kan ha en stor negativ inverkan på livskvaliteten. Barn med måttligt till svårt atopiskt eksem och deras föräldrar skattar besvären lika högt eller till och med högre i jämförelse med andra kroniska sjukdomar hos barn, t ex epilepsi, astma och diabetes [2]. Det finns inget laboratorieprov för att diagnostisera atopiskt eksem, utan diagnosen ställs med hjälp av Williams kriterier [3], dvs en kombination av
- kliande utslag med typiskt utseende och typisk distribution
- generellt torr hud
- tidig debut
- egen anamnes eller familjeanamnes på annan atopisk sjukdom.
Defekt barriärfunktion och hyperaktivt immunsvar
Patogenesen är inte helt klarlagd, men hudens barriärfunktion är defekt vid atopiskt eksem, och detta i kombination med ett avvikande, hyperaktivt immunsystem och en Th2 (T-hjälparlymfocyter typ 2)-driven inflammatorisk process leder till sjukdom. Hudbarriären och de immunologiska mekanismerna har ett nära samspel, men vilken av dessa två mekanismer som är den primära debatteras.
Epidermis har som primär uppgift att utgöra en skyddande barriär för att minimera vätskeförluster och förhindra inträde av allergener, patogener och andra främmande ämnen i huden. Terminal differentiering av keratinocyter från epidermis resulterar i bildandet av ett tätt packat lipoproteinmatrix. Den semipermeabla barriär som hornlagret (stratum corneum) utgör bildar det yttersta lagret i överhuden.
Den defekta barriärfunktionen vid atopiskt eksem orsakar ökad vätskeförlust och kan orsaka ökad penetration av irriterande ämnen, mikroorganismer och allergener. Dessa kan interagera med det medfödda ospecifika och förvärvade specifika immunsvaret med aktivering av bl a lokala antigenpresenterande celler och immuneffektorceller som följd [4]. Detta resulterar i sin tur i ett inflammatoriskt svar i huden, vilket initialt främst är Th2-drivet, men även Th22-celler och i mindre utsträckning Th17-celler bidrar. Vid ett mer kroniskt eksem ses även Th1-celler, men färre Th22- och Th17-celler än i de akuta lesionerna.
Både den defekta hudbarriären och det avvikande immunologiska svaret kan orsakas av genetiska faktorer och/eller miljöfaktorer.
Den genetiska faktor som är starkast associerad med atopiskt eksem är mutationer i en gen (FLG) som kodar för proteinet filaggrin, vilket är centralt för bildandet av en normal hudbarriär i hornlagret. Det är inte bara mutationer som kan minska mängden filaggrinprotein och därmed leda till nedsatt barriärfunktion. Även andra faktorer, som variation i antalet filaggringenkopior, mekanisk skada, bristande vattenhalt i hornlagret på grund av låg luftfuktighet och inverkan av Th2-cytokiner, har betydelse för mängden filaggrinprotein [1].
Behandlingen hittills symtomatisk
Den behandling som hittills har varit tillgänglig för atopiskt eksem är symtomatisk och inriktad mot besvär som är kopplade till sjukdomen, dvs den rodnade, kliande, inflammerade och torra huden. Behandlingen består i att undvika triggerfaktorer, att använda mjukgörande krämer och lokalbehandlingar med utvärtes glukokortikoider och kalcineurinhämmare och ljusbehandling samt i de svårare fallen systemiska behandlingar med metotrexat, ciklosporin, azatioprin eller mykofenolsyra.
Dessutom finns patientutbildningar i form av »eksemskolor« och olika psykologiska terapier, främst för att bemästra klåda och rivbeteende. Ibland ges också perorala glukokortikoider under kortare tid samt behandling mot jästsvampar i huden. Vid sekundära allvarliga hudinfektioner kan lokala eller perorala antibiotika övervägas, men med största sannolikhet finns en onödig förskrivning av antibiotika vid atopiskt eksem [5].
Behandlingarna är inte alltid tillräckliga, och det finns ett stort behov av en mer effektiv och specifik behandling, särskilt för dem med svårt atopiskt eksem. Under de senaste åren har intresset ökat för att ta fram nya läkemedel mot atopiskt eksem. Nya preparat kommer sannolikt att introduceras i Sverige under de närmaste åren, och fler är under utveckling.
Nya behandlingar i kliniska prövningar
En ökande förståelse av sjukdomsmekanismen vid atopiskt eksem, inte minst på molekylär nivå, har möjliggjort kliniska prövningar av nya läkemedel mot atopiskt eksem (Figur 1).
De medel som prövas är bl a anti-interleukin (IL)-4R, anti-IL-4, anti-IL-5, anti-IL-13, anti-31RA (receptor A), anti-IgE, anti-CD-20, JAK-STAT-hämmare (Janus kinase signal transducers and activators of transcription) och JAK-SYK-hämmare (Janus kinase spleen tyrosine kinase), anti-IL-6, anti-PDE-4 (fosfodiesteras-4-hämmare), anti-IL-12/23, anti-IL-17A, anti-IL-22, anti-H4R (histamin 4-receptor), anti-NKR1 (neurokininreceptor 1), κOR-stimulerare (κ-opioidreceptor), anti-TSLP (thymic stromal lymphopoietin) och DGLA (dihomo-γ-linolenic acid) [6, 7].
Behandlingar som godkänts under 2017
Dupilumab är en monoklonal antikropp och det första godkända biologiska läkemedlet mot atopiskt eksem. Det godkändes av det amerikanska läkemedelsverket Food and Drug Administration (FDA) i mars 2017 för vuxna med medelsvårt till svårt atopiskt eksem. Det verkar genom att binda sig till alfasubenheten av interleukin 4-receptorn (IL-4Ra) och blockerar därmed både IL-4 och IL-13, två Th-2-cytokiner som spelar en viktig roll i inflammationssvaret vid atopiskt eksem.
I två randomiserade placebokontrollerade fas 3-studier med sammanlagt 1 379 vuxna patienter med medelsvårt till svårt atopiskt eksem hade närmare 40 procent läkt helt eller nästan helt efter 16 veckors behandling med dupilumab subkutant varje eller varannan vecka jämfört med 8–10 procent i placebogruppen [8]. Eksemets svårighetsgrad skattad med EASI (Eczema area severity index) reducerades med minst 75 procent hos ca 70 procent av dem med aktiv behandling jämfört med 31–38 procent av dem med placebo. Även klådan minskade signifikant. Ansökan om europeiskt godkännande är inlämnad, och företaget bedömer att preparatet kommer på den svenska marknaden under 2018.
Crisaborol, en fosfodiesteras 4-hämmare för utvärtes bruk, godkändes av FDA i januari 2017 för patienter med lätt till medelsvårt eksem. Mekanismen är inte helt kartlagd, men preparatet ökar intracellulärt cykliskt adenosinmonofosfat (cAMP), vilket tros minska det proinflammatoriska svaret vid atopiskt eksem.
I två randomiserade, vehikelkontrollerade fas 3-studier med sammanlagt 1 522 patienter med lätt till medelsvårt eksem sågs att en signifikant större andel efter 28 dagars lokalbehandling läkte helt eller nästan helt med aktiv behandling jämfört med enbart vehikel (ca 50 procent vs 30–40 procent) [9]. Ansökan om europeiskt godkännande beräknas bli inlämnad under 2018, och företaget bedömer att preparatet kan komma på den svenska marknaden 2019.
Exempel på andra nya behandlingsmöjligheter
Klåda är det centrala symtomet vid atopiskt eksem. Klådan leder till rivning och ytterligare skada av hudbarriären och därmed till ökad inflammation och klåda i en ond »klåd–rivcirkel«. Klådan är inte medierad via histaminreceptor 1 och därför är inte H1-receptorblockerare effektiva. Fortfarande är behandling med glukokortikoider eller kalcineurinhämmare den mest och bäst dokumenterade effektiva klådstillande behandlingen.
Koncentrationen av IL-31 är förhöjd vid atopiskt eksem. Denna cytokin, som främst bildas av Th2-lymfocyter, kan stimulera IL-31-RA på olika typer av celler, inklusive C-fibrer, och därmed frisätta klådmediatorer [1]. Nemolizumab, en monoklonal antikropp riktad mot IL-31-RA, har i en fas 2-studie utvärderats på vuxna patienter som inte fått tillräcklig hjälp av konventionell utvärtes behandling mot atopiskt eksem. I studien ingick 216 patienter som fick preparatet subkutant var fjärde vecka. Efter tolv veckor hade klådan minskat med ca 60 procent, jämfört med 20 procent i placebogruppen, men effekten på utbredningen av eksemen var dock inte lika stor [10].
Torr hud är ett centralt fynd vid atopiskt eksem. I två prospektiva randomiserade kontrollerade studier visades att man kunde förebygga atopiskt eksem genom dagliga smörjningar med mjukgörande krämer av nyfödda i högriskfamiljer. Man kunde påvisa en minskning av den kumulativa incidensen av atopiskt eksem med 50 procent vid 6 månaders ålder [11] respektive med 32 procent vid 8 månaders ålder [12]. Behandlingsmedlen mot torr hud är visserligen inte nya, men tillvägagångssättet att behandla asymtomatiska nyfödda i primärpreventivt syfte är nytt.
Resultaten är lovande, men om behandlingen endast skjuter upp eksemdebuten eller om den kanske till och med kan leda till att sjukdomen inte alls bryter ut får framtida studier visa. Dagliga smörjningar med oljor på den nyföddas hud kan visserligen förbättra hydreringen, men effekten på de lamellära lipidstrukturerna är oklar. Fler studier behövs därför inom detta område innan sådan behandling kan rekommenderas [13].
Fler och bättre behandlingsverktyg på gång
Atopiskt eksem är en multifaktoriell sjukdom som drabbar en stor patientgrupp och uppvisar en stor variation i svårighetsgrad. Det finns sannolikt flera subtyper, och behandlingen måste individanpassas.
Det första biologiska läkemedlet mot atopiskt eksem är nu registrerat i USA, och det kommer sannolikt inom kort även att introduceras i Sverige. Flera nya läkemedel är framtagna tack vare bättre förståelse av sjukdomsmekanismen bakom atopiskt eksem, och de kommer förhoppningsvis att kunna introduceras under de närmaste åren. Därmed får vi fler och bättre verktyg att hjälpa dem med atopiskt eksem, inte minst de svårast sjuka.
Potentiella bindningar eller jävsförhållanden: Maria Bradley har varit föreläsare betald av Novartis, AstraZeneca, AbbVie, LEO och Celgene samt deltagit i rådgivande möten med Sanofi Genzyme, Novartis och Lilly. Carl-Fredrik Wahlgren har varit föreläsare betald av Shire, Galderma och Novartis samt deltagit i rådgivande möten med CSL Behring och Sanofi Genzyme.



















