Diagnoskriterierna för diabetes är satta utifrån när mikrovaskulära komplikationer ökar märkbart, men makrovaskulära komplikationer ökar redan vid lägre glukosnivåer.
De olika diagnosmetoderna ersätter inte varandra utan kompletterar varandra.
För samtliga diagnosmetoder finns laboratoriemässiga begränsningar.
Basen i behandling är livsstilsintervention som vid behov kompletteras med blodtrycks- och lipidbehandling.
I normalfallet ges tidigt efter diagnos glukossänkande behandling, företrädesvis med metformin. Ett lämpligt behandlingsmål är HbA1c 42–52 mmol/mol, i den lägre delen av intervallet för yngre patienter.
Vid långvarig diabetes och hos sköra patienter bör HbA1c-målet vara högre.
Enligt beräkningar från Internationella diabetesfederationen 2015 var den globala förekomsten av diabetes 415 miljoner i åldersgruppen 20–79 år, motsvarande 9,1 procent av den vuxna befolkningen. Cirka 90 procent av dessa hade typ 2-diabetes. Antalet personer med diabetes förutspås öka till 642 miljoner år 2040, varav mer än 40 procent i Kina och Indien [1]. Studier från Sverige de tre senaste årtiondena har visat på en modest eller obefintlig prevalensökning, och studier från olika delar av landet och i varierande åldersgrupper har funnit en diabetesprevalens på 3–6 procent [2-8]. Såväl i Sverige som internationellt beräknas att varannan till var tredje vuxen med diabetes är odiagnostiserad.
Vid typ 2-diabetes får patienten vanligtvis symtom på hyperglykemi sent i förloppet. Vården har därför en viktig uppgift att identifiera personer med störd glukosmetabolism för att sätta in livsstils- och eventuell farmakologisk behandling, helst innan en diabeteskomplikation uppstått. De diagnostiska gränserna för diabetes för fasteplasmaglukos, plasmaglukos efter 2 timmar vid ett oralt glukostoleranstest (OGTT) liksom för HbA1c har lagts där frekvensen av diabetesretinopati märkbart ökar [9]. Förhöjda glukosnivåer omedelbart nedanför diabetesgränsen mätt som nedsatt glukostolerans (impaired glucose tolerance, IGT), förhöjt fasteglukos (impaired fasting glucose, IFG) eller mätt med HbA1c kallades tidigare »prediabetes«. Detta är ett oegentligt begrepp då alla inte utvecklar diabetes; däremot är risken för makrovaskulära komplikationer, inklusive död, förhöjd redan vid dessa glukosnivåer, framför allt vid IGT [9, 10]. I en metaanalys beräknades att 4–6 procent av patienter med isolerad IGT och 6–9 procent av patienter med isolerad IFG årligen progredierade till diabetes. Vid kombinerad IFG och IGT ökar motsvarande siffror till 15–19 procent [11]. Vid ett förhöjt HbA1c (42–48 mmol/mol) ses liknande årlig progression till diabetes på 7 procent [12]. Livslångt beräknar en expertpanel från American Diabetes Association att 70 procent av individer med »prediabetes« utvecklar diabetes, men en kinesisk studie har beskrivit en kumulativ risk på över 90 procent över en tjugoårsperiod [13].
Diagnoskriterier
Det är viktigt att varje läkare är väl förtrogen med diagnoskriterierna då en diabetesdiagnos har livslång konsekvens för patienten och vården. En studie från Västerbotten visade att diagnosen var satt i enlighet med WHO-kriterierna i 95 procent av fallen [14], medan en europeisk studie från fem länder visade överensstämmelse i 82 procent av fallen [15].
Från 1980 och framåt har WHO stått för de internationellt överenskomna diagnoskriterierna för diabetes mellitus. De nu gällande är från 1999 [10] med ett tillägg 2011 inkluderande HbA1c [9].
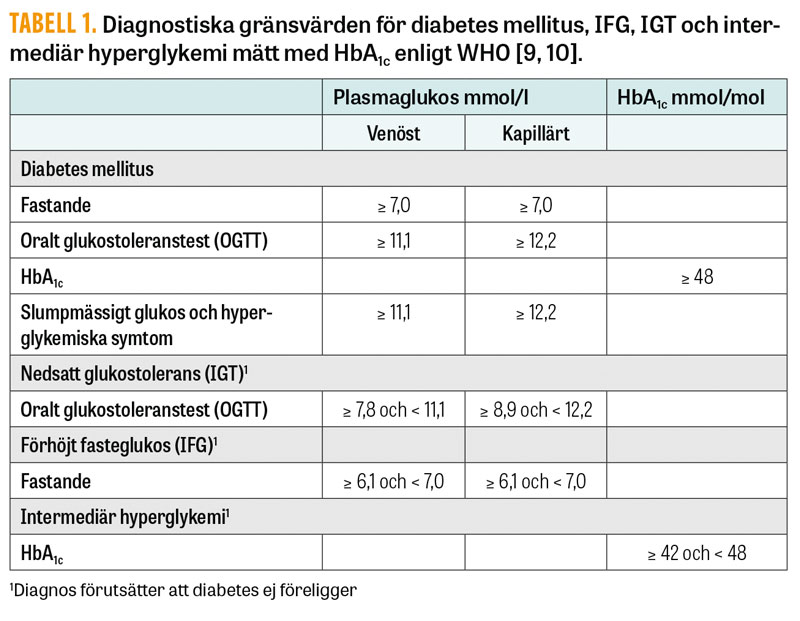
Diagnosen kan ställas med fasteglukosprov eller med plasmaglukosvärdet 2 timmar efter oralt intag av 75 g glukos (OGTT) liksom med HbA1c. Om inga symtom föreligger ska diagnosen konfirmeras med ytterligare ett prov vid ett annat tillfälle. Om HbA1c och något av glukoskriterierna (fastande eller 2 timmar efter OGTT) utfaller positivt samtidigt räcker ett provtillfälle. Dessutom räcker ett enstaka slumpmässigt taget plasmaglukosprov för diagnos om patienten har symtom på hyperglykemi. I Tabell 1 redovisas diagnostiska gränsvärden för diabetes, IFG, IGT samt intermediär hyperglykemi mätt med HbA1c. Observera att lägre gränser gäller för diagnos av graviditetsdiabetes, liksom delvis andra provtagningsintervall (fastande ≥ 5,1 mmol/l, 1 timme efter OGTT ≥ 10,0 mmol/l och 2 timmar efter OGTT ≥ 8,5 mmol/l), samt att dessa värden baseras på venös provtagning [16]. HbA1c ska inte användas för diagnostik hos barn eller unga < 20 år, vid misstänkt typ-1 diabetes, vid graviditet eller hos nyförlösta eller vid misstanke om kort diabetesduration (< 2 månader) [17].
Samstämmigheten mellan de olika diagnostiska metoderna är begränsad. Som exempel uppfyllde 28 procent av nydiagnostiserade individer med typ 2-diabetes diagnoskriterierna för både fasteglukos och 2-timmarsvärdet efter OGTT [18], och motsvarande siffror för HbA1c och fasteglukos var 47 procent i en annan studie [19]. Ingen av diagnosmetoderna för diabetes identifierar samtliga personer med ökad hjärt–kärlrisk på grund av störd glukosmetabolism. De diagnostiska metoderna ersätter därför inte varandra utan identifierar delvis olika grupper med förhöjd, men ibland något olika, kardiovaskulär risk [10, 18, 20]. Generellt sett nås störst chans att identifiera personer med diabetes med ett OGTT [19, 21].
Provtagningsöverväganden
Det finns självklara WHO-krav på att de metoder som används för diagnostik överensstämmer med internationell referens [10]. Detta fordrar kontinuerlig extern kvalitetssäkring av använda analysinstrument. Användning av såväl fasteglukos som OGTT och HbA1c har fördelar men även specifika metodologiska problem. Som exempel kan nämnas att fasteprov kräver minst 8 timmars fasta [22] samt att stress och akut sjukdom, fysisk aktivitet och kostintag påverkar glukosmätningar men inte HbA1c [18]. Variabiliteten vid glukosprovtagning, speciellt vid OGTT, är tämligen stor till skillnad från vid HbA1c som är stabilt vid upprepad provtagning. I en dansk screeningundersökning upprepades en glukosbelastning efter 2 veckor och då sågs en variation av fasteglukos på cirka ± 1 mmol/l och av 2-timmarsvärdet på cirka ± 3 mmol/l, och endast hos 76 procent kunde en diabetesdiagnos upprepas [23]. Vid dysglykemi som helhet (mätt som förekomst av antingen IGT eller diabetes) är variabiliteten inte så stor. I 93 procent av fallen bekräftades den onormala glukosomsättningen vid ett upprepat OGTT [24].
Födointag och fysisk aktivitet påverkar glukosmätningar, inte bara i direkt anslutning till måltid eller aktiviteten. Ett lågt kolhydratintag dagen före ett OGTT medför att den postprandiala glukosnivån påtagligt höjs [25]. Därför rekommenderar WHO att kolhydratintaget ska vara minst 150 g/dag under minst tre dagar före ett OGTT. Den fysiska aktiviteten ska vara den vanliga för patienten under samma tid, och dessutom ska aktuell medicinering och eventuell infektion värderas. Då glukosnivån i blodet normalt sjunker kontinuerligt 2 timmar efter glukosintaget måste provtagningen ske inom ± 5 minuter för att inte ett felvärde ska registreras [10].
HbA1c-nivån speglar den genomsnittliga glukosnivån under erytrocytens överlevnad, vilken normalt är drygt 100 dagar. Vid en kort överlevnad för erytrocyten eller vid stor andel nybildade erytrocyter blir HbA1c lågt, och det motsatta ses vid förlängd erytrocytöverlevnad. Hemoglobinopatier kan både påverka erytrocytöverlevnaden och analysen av HbA1c, och merparten av hemoglobinet måste vara HbA för att få ett korrekt analysresultat. Även vissa andra sjukdomar/medicineringar kan påverka uppmätt HbA1c-nivå [26]. För sammanfattning se Fakta 1.
Screening
I Socialstyrelsens nationella riktlinjer från 2017 anges att det är motiverat med riktad screening av personer som har ökad risk för att utveckla typ 2-diabetes [27]. I avsaknad av god evidens brukar med »ökad risk« nämnas förekomst av typ 2-diabetes bland första- eller andragradssläktingar eller förekomst av tillstånd som brukar associeras med insulinresistens, såsom övervikt/fetma, bukfetma, hypertoni, dyslipidemi och polycystiskt ovariesyndrom. Förekomsten av diabetes är högre bland icke-européer, och den ökade diabetesförekomsten ses dessutom vid ett lägre BMI, något som också påverkar indikationen för riktad screening [28]. För sjukvården är det dessutom viktigt att regelbundet följa upp glukosnivåer bland personer med tidigare graviditetsdiabetes, IFG, IGT eller förhöjt HbA1c samt bland patienter som behandlas med läkemedel som potentiellt är glukoshöjande, till exempel kortison, eller kraftigt viktökande, som vissa psykofarmaka.
Behandlingsmål
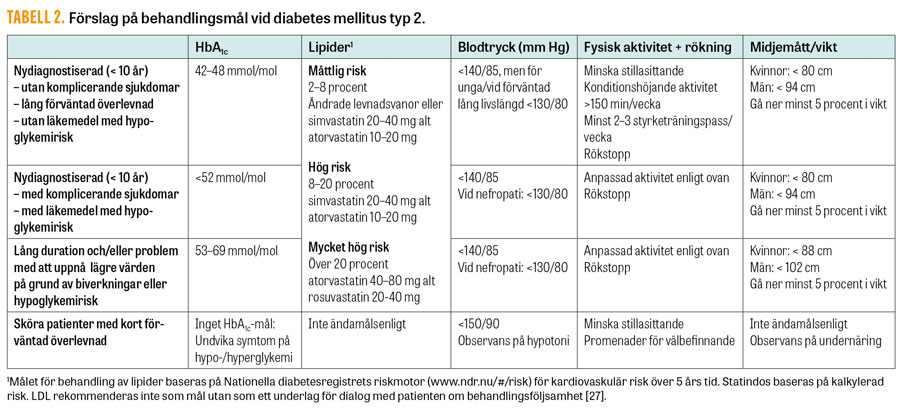
Under det senaste decenniet har riktlinjerna fokuserat på individualiserade behandlingsmål. Vilka värden som ska eftersträvas avgörs av den enskilda patientens riskprofil med hänsyn tagen till bland annat samsjuklighet, sjukdomsduration och förväntad livslängd. Behandlingen bör vara individanpassad och ha en multifaktoriell inriktning. Ett förslag på lämpliga behandlingsmål ges i Tabell 2. För glukosbehandling är målet att minska risken för hjärt–kärlsjukdom och mikrovaskulära komplikationer samt att öka livskvaliteten. Många studier har entydigt visat att risken för mikrovaskulära komplikationer reduceras av glukossänkande behandling och att framför allt ett HbA1c över cirka 62 mmol/mol är förenat med ökad risk [29, 30].
När det gäller makrovaskulära komplikationer har det fram till nyligen bara funnits en studie, UKPDS (United Kingdom prospective diabetes study), som visat att intensivare glukossänkande behandling (under median 10 år) medför minskad risk för hjärt–kärlsjukdom 17 år efter diagnos jämfört med en mindre intensiv behandling. Deltagande patienter var överviktiga med nydiagnostiserad diabetes där metforminbehandling påbörjades strax efter diagnos [31, 32]. Dessutom har pioglitazon visat en skyddande effekt för det sammansatta, men sekundära, effektmåttet död, hjärtinfarkt och stroke [33]. Studier där man givit mycket intensiv glukossänkande behandling till patienter med lång diabetesduration och dålig glukoskontroll har kommit att påverka våra behandlingsriktlinjer. I dessa studier sågs ingen positiv effekt [29, 34] eller till och med fler makrovaskulära händelser [35] av intensivbehandling jämfört med standardbehandling. Vid subanalyser sågs att negativa händelser i första hand uppträdde hos patienter med tidigare känd hjärt–kärlsjukdom (eller njursjukdom). Hos patienter utan tidigare känd hjärt–kärlsjukdom sågs däremot en minskning av hjärt–kärlhändelser [35, 36].
Våra behandlingsriktlinjer har som följd av dessa studier kunnat sammanfattas med att vi bör ge intensiv glukossänkande behandling, företrädesvis med metformin, vid diagnos eller tidigt i sjukdomsförloppet. Vid långvarig diabetes och existerande komplikationer bör behandlingsmålen vara mindre intensiva.
De senaste två åren har tre studier av tilläggsbehandling med antingen empagliflozin, liraglutid eller kanagliflozin till diabetespatienter med tidigare känd hjärt–kärlsjuklighet publicerats. Studierna visar minskad risk för nya hjärt–kärlhändelser, även vid mångårig diabetes och dålig diabeteskontroll [37-39]. Dessa studier har 2017 förändrat Socialstyrelsens prioritering av läkemedelsbehandlingen för patienter med dessa komplikationer till prioritetsgrupp 3 [27].
IFG, IGT och intermediär hyperglykemi mätt med HbA1c. Basen i behandlingen vid dessa tillstånd är att ge livsstilsråd framför allt beträffande rökning, fysisk aktivitet och kost. Dessutom skattas patientens allmänna risk för hjärt–kärlsjukdom, och vid behov initieras blodtrycks- och lipidsänkande behandling. Dessa åtgärder är även basen vid konstaterad diabetes. Bäst vetenskapligt stöd för hjärt–kärlskyddande riskminskning av intervention finns vid IGT [40-42]. Ju högre patientens glukos- och HbA1c-värden är, desto större är risken att patienten även utvecklar diabetes, och det är därför rimligt att följa upp utvecklingen av patientens glukosmetabolism och livsstil, förslagsvis efter 6 månader och därefter med regelbundna intervall [17].
Nydiagnostiserad typ 2-diabetes. De första 5–10 åren efter diagnos bör ambitionen vara att uppnå ett HbA1c kring eller strax över normalnivån för friska. Det exakta målet kan inte fastställas utifrån tillgänglig evidens, men de flesta experter är ense om nivåer kring 42–52 mmol/mol. Värden i den lägre delen av intervallet (42–48 mmol/mol) bör eftersträvas hos patienter med lång förväntad överlevnad (förslagsvis yngre än 55 år), vid avsaknad av andra komplikationer eller samsjuklighet samt hos patienter som behandlas med läkemedel utan risk för hypoglykemi. Dessa rekommendationer baseras på UKPDS-data men även på det faktum att typ 2-diabetes med kort duration ofta är relativt enkel att behandla med livsstilsåtgärder och en begränsad mängd farmaka.
Typ 2-diabetes med längre duration. Även vid längre diabetesduration anpassas behandlingsmålen efter patientens förväntade överlevnad, samsjuklighet samt eventuell hypoglykemirisk. Bra stöd för behandlingsmål saknas, men det är värt att komma ihåg att risken för mikrovaskulära komplikationer ökar vid HbA1c över cirka 62 mmol/mol [29, 30]. Intensiv behandling för att förbättra ett dåligt HbA1c och nå nära normala HbA1c-nivåer hos patienter med lång diabetesduration kan ej rekommenderas. I synnerhet gäller detta om patienten har hjärt–kärl- och/eller njurkomplikationer [35, 36].
Typ 2-diabetes vid hög ålder och samsjuklighet. Vid hög ålder med samsjuklighet, hypoglykemiproblematik eller vid kort förväntad överlevnad är det klokt och ofta nödvändigt att ha ett mindre intensivt behandlingsmål för HbA1c. HbA1c > 70 mmol/mol ökar dock risken för hyperglykemisymtom med påverkan på patientens livskvalitet, varför högre nivåer om möjligt bör undvikas. HbA1c > 70 mmol/mol indikerar också att patienten sannolikt har höga medelglukosvärden (> 10 mmol/l) med risk för glukosuri. Vid glukosvärden ≥ 15 mmol/l befinner sig patienten ofta i ett katabolt tillstånd, vilket bör undvikas. Patientens egen ambitionsnivå och inställning samt kognitiva möjlighet att följa behandlingen är av stor vikt. I vissa fall är det svårt att uppnå värden < 70 mmol/mol trots flera åtgärder, och man får då inrikta sig på att ha en behandlingsstrategi som minskar risken för hypoglykemi och ytterligare viktuppgång. Hos sköra patienter bör behandlingen inte i första hand inriktas på ett enskilt HbA1c-mål utan på att man undviker både hyper- och hypoglykemi. I praktiken innebär det ofta HbA1c-värden kring 70 mmol/mol.
Potentiella bindningar eller jävsförhållanden: Mikael Lilja och Stefan Jansson har erhållit föreläsararvode från AstraZeneca, Lilly och Novo Nordisk.
FAKTA 1. Tillstånd som kan påverka HbA1c [17, 26] och glukosprov [18, 22-25].
HbA1c – Ändrad erytrocytomsättning
- Hemoglobinopatier
- Anemi
- Behandling av anemi
- Njursvikt (kronisk)
- Leversvikt (kronisk)
- Splenomegali/splenektomi
- Reumatoid artrit
- Vissa läkemedel, till exempel anti-
- retrovirala vid hiv
HbA1c – Påverkad glykosylering
- Njursvikt (kronisk)
- Uttalad alkoholism
HbA1c – Påverkad labbanalys
- Hemoglobinopatier
- Mycket höga triglyceridnivåer
Fasteglukos
- Mindre än 8 timmars fasta
- Stress
- Akut sjukdom
- Fysisk aktivitet
- Glukos 2-timmarsvärde efter oralt glukostoleranstest
- Stress
- Akut sjukdom
- Fysisk aktivitet
- Lågt kolhydratintag dagarna innan
- Provtagning utanför »fönstret« ± 5 min