Läkemedelsbehandling av epilepsi är symtomatisk.
Som regel inleds behandling först efter upprepade oprovocerade anfall.
Läkemedel väljs med utgångspunkt från effekt vid patients typ av anfall/epilepsi, men hänsyn tas till biverkningsprofil och samsjuklighet.
Karbamazepin, lamotrigin och levetiracetam är förstahandsalternativ vid fokala anfall.
Valproat är förstahandsval vid generaliserade tonisk-kloniska anfall men ska undvikas till personer som kan tänkas bli gravida. Lamotrigin och levetiracetam är alternativ.
Oavsett läkemedel behöver dosen individualiseras.
Efter längre tids anfallsfrihet kan utsättning övervägas. Risken för återfall beräknas utifrån en rad kliniska faktorer.
Med närmare 20 nya antiepileptika registrerade i Sverige sedan 1990 har valmöjligheterna inom epilepsibehandling ökat radikalt. Däremot har nytillskotten inte på något avgörande sätt ändrat de principiella förutsättningarna för läkemedelsbehandling av epilepsi. Behandlingen är fortfarande att betrakta som symtomatisk och syftar till att minska risken för anfall så länge den pågår, men inget talar för att dagens behandling påverkar den underliggande sjukdomsprocessen och »botar« epilepsin. Målet är varaktig anfallsfrihet utan besvärande biverkningar. Behandlingen sköts i allmänhet av barn- eller vuxenneurologer, men många fler behöver förstå behandlingsprinciperna.
När ska man inleda behandling?
Behandling bör inte inledas om tveksamhet råder om diagnosen. Att en person fått diagnosen epilepsi innebär inte heller per automatik att behandling är motiverad. Ett beslut om att inleda sådan bör föregås av noggrann avvägning av nytta mot risker. Detta innebär individuell bedömning av risk för nya anfall utan behandling, risker och andra konsekvenser (t ex för körkort) om anfall skulle uppträda, möjligheter med behandling och risker för biverkningar. Patientens, och för barn även vårdnadshavarens, delaktighet i beslutsprocessen är avgörande.
Ett första epileptiskt anfall motiverar sällan behandling då färre än hälften kommer att få återfall [1]. Randomiserade studier har visserligen visat att behandling insatt redan efter ett första anfall kan reducera återfallsrisken med upp till 50 procent [2, 3], men behandling efter ett första jämfört med efter upprepade anfall påverkar inte möjligheten till anfallskontroll på sikt [2, 4]. Den som har haft ett andra oprovocerat anfall har betydligt högre risk för fortsatta anfall, cirka 70 procent [1].Risken för fortsatta anfall varierar dock. Förekomst av underliggande hjärnskada, neuroradiologiskt påvisad förändring i hjärnan, epileptiform aktivitet vid EEG och nattligt anfall talar för en ökad risk för återfall efter ett första anfall [3]. Undantag från grundregeln att inleda behandling först efter två oprovocerade anfall kan göras om återfallsrisken är hög och om konsekvenserna av ett återfall vore allvarliga för patienten. Omvänt kan det ibland vara rimligt att avvakta med behandling även om patienten haft upprepade anfall, om dessa varit mycket lindriga eller kommit med långa mellanrum (år). Den informerade patientens (och eventuell vårdnadshavares) inställning är avgörande, och det är sällan farligt att avvakta med insättandet tills patient och läkare är överens om att man har tillräckligt beslutsunderlag.
Val av läkemedel
Behandling inleds med ett antiepileptikum som monoterapi. Valet av läkemedel styrs i första hand av patientens typ av anfall/epilepsi: fokal eller generaliserad. Några antiepileptika har bara effekt vid fokala anfall och kan till och med förvärra sjukdomen om de ges till personer med vissa generaliserade epilepsiformer. Korrekt anfallsklassifikation är därför viktig inför val av läkemedel. Särskilt viktigt är att skilja generaliserade tonisk-kloniska anfall från fokala anfall som genom spridning utvecklas till bilateralt tonisk-kloniska anfall. Några antiepileptika har effekt vid flertalet anfallsformer, fokala som generaliserade. I viss mån finns ett samband mellan läkemedlens postulerade verkningsmekanismer (Figur 1) och effekt vid olika anfallstyper. Sålunda har natriumkanalblockerare ofta effekt huvudsakligen vid fokala anfall, medan antiepileptika med multipla verkningsmekanismer kan ha bredare effektspektrum. Verkningsmekanismerna är dock ofullständigt kända.
Fokala epilepsier
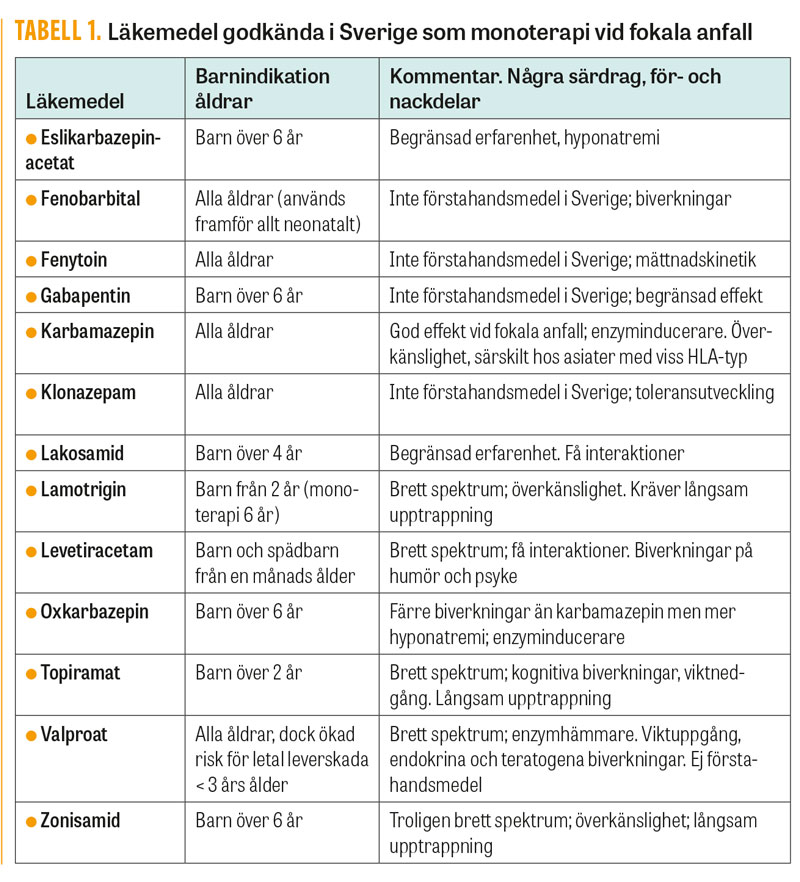
I dag finns 13 olika läkemedel godkända i Sverige för behandling i monoterapi av fokal epilepsi. Samtliga är godkända för behandling av vuxna medan färre läkemedel är registrerade för behandling av barn (Tabell 1). I de studier som ligger till grund för godkännandet har som regel det nya läkemedlet jämförts med etablerad behandling, vanligen karbamazepin. Inte i någon av dessa studier har nyare antiepileptika varit mer effektiva än karbamazepin [5]. Det har alltså varit svårt att visa skillnad i effekt mellan olika antiepileptika vid behandling av fokala epilepsier. Därför har andra faktorer som biverkningar och benägenhet för läkemedelsinteraktioner fått betydelse vid val av behandling. En stor randomiserad öppen studie fann att lamotrigin tolererades bättre än karbamazepin [6]. Läkemedelsverket utfärdade 2011 rekommendationer för val av antiepileptika. Här anges karbamazepin som ett förstahandsmedel vid fokal epilepsi, med lamotrigin och levetiracetam som alternativ, särskilt om karbamazepins enzyminducerande effekt och interaktioner förväntas ge problem. Detta är särskilt relevant för äldre med omfattande polyfarmaci, där lamotrigin eller levetiracetam ofta föredras [7]. Se i övrigt Tabell 1 för för- och nackdelar med de olika läkemedlen. Riktlinjerna från National Institute for Health and Care Excellence (NICE) [8] anger karbamazepin och lamotrigin som förstahandsval vid fokala anfall oavsett ålder.
Generaliserade epilepsier
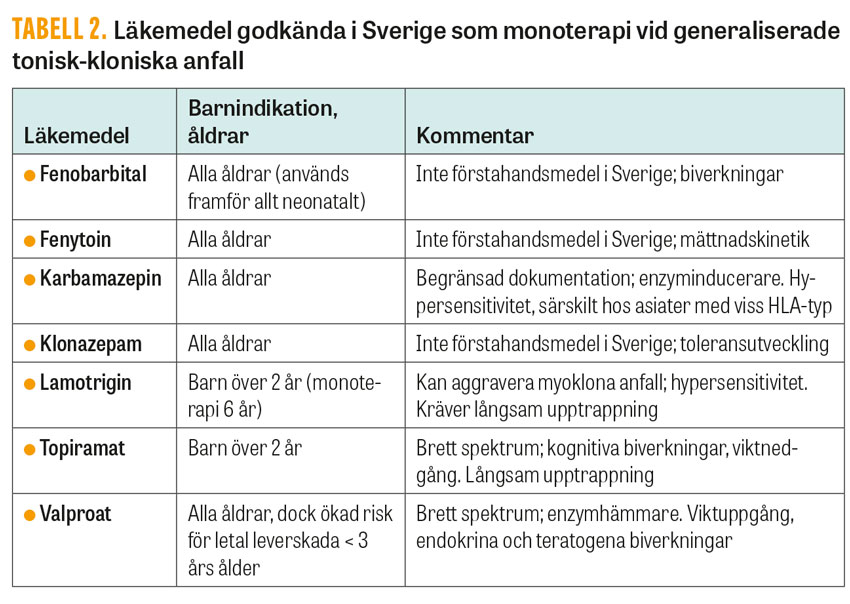
Det finns flera former av generaliserade epilepsier med olika anfallsmanifestationer. Vanligast är generaliserade tonisk-kloniska anfall. För monoterapi vid denna typ av anfall finns sju olika antiepileptika godkända (Tabell 2). Underlaget i form av väldesignade randomiserade studier är mycket mindre än vid fokala epilepsier [5]. En randomiserad öppen studie fann att valproat var mer effektivt än lamotrigin och topiramat [9] vid behandling av patienter med generaliserad epilepsi eller epilepsi som inte kunde klassificeras. Valproat kan därför ses som ett förstahandsmedel vid generaliserade tonisk-kloniska anfall [8], men ska undvikas till kvinnor i fertil ålder och flickor [10]. Levetiracetam används ofta som ett alternativ till valproat och lamotrigin trots att det inte godkänts som monoterapi på denna indikation.
Epilepsisyndrom
Att förutom anfalls- och epilepsityp också klarlägga om det föreligger ett epileptiskt syndrom är viktigt för val av behandling och kan ge vägledning om prognos. Epileptiska syndrom definieras av typisk klinisk bild, såsom anfallstyp(er), debutålder och EEG-mönster (se artikel »Nya reviderade klassifikationer av epilepsianfall och sjukdomstyp« av Zelano et al i detta tema).
Barndomsepilepsi med centrotemporala spikar är exempel på ett fokalt epilepsisyndrom. Det utgör 10–20 procent av alla barnepilepsier, ofta med debut i tidig skolålder och spontan remission före tonåren. Den vanligaste anfallstypen är nattligt fokalt motoriskt anfall utan medvetandepåverkan. Profylaktisk medicinering är inte nödvändig vid detta syndrom, men kan övervägas vid frekventa eller svåra anfall. I Sverige är oxkarbazepin av tradition förstahandsval [11].
Absensepilepsi i barndomen är ett vanligt generaliserat epilepsisyndrom, ofta med debut kring sex års ålder. Absenser är korta frånvaroepisoder utan förlust av muskeltonus och kan provoceras fram med hjälp av hyperventilation. Absensanfall förekommer även vid andra generaliserade epilepsisyndrom, såsom juvenil absensepilepsi och juvenil myoklon epilepsi. Etosuximid är förstahandsmedel mot absenser [12], valproat och lamotrigin kan vara alternativ om även andra anfallstyper föreligger, medan karbamazepin och oxkarbazepin bör undvikas.
Juvenil myoklon epilepsi, som brukar debutera i tonåren, är ett annat vanligt generaliserat epilepsisyndrom, där patienten har myoklona anfall och oftast även generaliserade tonisk-kloniska anfall. Välgjorda randomiserade studier saknas för denna epilepsiform [5], men flertalet personer kan bli anfallsfria på valproat, som är bäst dokumenterat och anses vara förstahandsmedel för pojkar och män. Lamotrigin är ett alternativ, liksom levetiracetam. Fenytoin, karbamazepin och oxkarbazepin bör undvikas då dessa läkemedel ibland kan förvärra särskilt myoklona anfall.
Utvecklingsmässig och epileptisk encefalopati
Vid vissa epileptiska syndrom ses en tillbakagång i barnets utveckling. Detta kan orsakas av sjukdomens underliggande etiologi, men också av en intensiv epileptisk aktivitet. Behandling med antiepileptika kan minska antalet anfall och i vissa fall även begränsa graden av encefalopati. Det syndrom som först beskrivits är Wests syndrom, som förutom psykomotorisk påverkan karaktäriseras av epileptiska spasmer med debut under spädbarnsåret. Bakomliggande etiologi är heterogen, ofta strukturell eller genetisk. ACTH och vigabatrin är farmakologiska förstahandsalternativ. Ett annat exempel är Dravets syndrom, som debuterar med långdragna, ofta ensidiga, feberutlösta epilepsianfall under det första levnadsåret. Då tillståndet oftast orsakas av mutationer i en gen kodande för natriumjonkanaler i centrala nervsystemet, kan vissa epilepsiläkemedel som blockerar dessa jonkanaler förvärra anfallssituationen. Stiripentol i kombination med klobazam och valproat anses för närvarande mest effektivt [13].
Nya genetiska analysmetoder och ökad kunskap om patofysiologi vid enskilda epilepsisyndrom har gett hopp om utveckling av läkemedel specifikt riktade mot orsaken till individens epilepsi – epileptogenesen. Det bästa exemplet är tuberös skleros, ett tillstånd associerat med läkemedelsresistent epilepsi och kortikala förändringar i hjärnan. Vid tuberös skleros orsakar mutationer i tumörsuppressorgener ett ökat uttryck av mTOR (mammalian target of rapamycin) och associerade proteiner. Behandling med selektiva mTOR-hämmare har nyligen visats verksam mot epilepsi vid tuberös skleros [14] och kan komma att bli en viktig behandlingsstrategi även vid andra typer av epilepsi med kortikala missbildningar.
Flickor och kvinnor i fertil ålder
De flesta kvinnor med epilepsi har normala graviditeter och föder fullt friska barn. Under senare år har det dock blivit uppenbart att användning av valproat under graviditet är förenad med större risker för fosterskador och risk för negativ effekt på barnets utveckling jämfört med många andra antiepileptika. Valproat ska därför inte användas av flickor, fertila eller gravida kvinnor, såvida inte andra behandlingsalternativ är otillräckliga eller inte tolereras [10]. Risk–nyttaavvägning av olika behandlingsalternativ inför planerad eller under pågående graviditet kräver stor sakkunskap och bör därför göras i samråd med specialist.
Dosering och terapistyrning
Behandling inleds med upptrappning till en första tänkt måldos. Upptrappningen syftar till att minska risken för biverkningar, och tiden varierar beroende bland annat på läkemedel (t ex från några dagar för levetiracetam till flera veckor för lamotrigin) [7]. Om patienten haft flera anfall på kort tid kan behandlingen i stället behöva inledas med en laddningsdos för att snabbt uppnå effekt. Vanligen siktar man på en relativt låg första måldos. Eftersom behandlingen är profylaktisk och anfall kommer med oregelbundna intervall kan det ta lång tid innan man vet om behandlingen och dosen är effektiv. Oavsett läkemedel varierar optimal dos mellan olika personer, men ibland även för samma person vid olika tillfällen. Variabiliteten beror i hög grad på skillnader och ändringar i läkemedlets omsättning, särskilt dess elimination. Bestämning av läkemedelskoncentration i serum används därför som ett hjälpmedel för att finna optimal dos. För en del antiepileptika anges riktområden för serumkoncentration. Dessa värden bör användas med urskiljning eftersom den individuella terapeutiska koncentrationen ofta ligger utanför angivet intervall. Ett bättre sätt är att mäta läkemedelsnivån vid befarad eller förmodad förändring i serumkoncentration för att kunna anpassa dosen för att upprätthålla en optimal effekt. Vid terapisvikt kan koncentrationsbestämning också användas för att klargöra om försämringen kan förklaras av ändrad serumkoncentration, till exempel på grund av läkemedelsinteraktion eller bristande följsamhet. Denna användning förutsätter att prov tas när patienten mår bra för att fastställa den enskilde patientens optimala koncentration, vilket sedan tjänar som jämförelse vid terapisvikt [15].
Behandling vid läkemedelsresistens
Om patienten fortsätter att ha anfall trots att det först insatta läkemedlet prövats i optimal dos försöker man i allmänhet att byta till ett annat lämpligt läkemedel. Mer än hälften av alla med nydebuterad epilepsi uppnår varaktig anfallsfrihet med första eller andra prövade monoterapin. Om så inte sker bör man överväga om diagnosen är korrekt, om man har valt rätt läkemedel i förhållande till patientens anfallstyp, om optimal dos prövats och om patienten tar sin medicin som ordinerat. Den som har epilepsi och fortsätter att ha anfall trots behandlingsförsök med två olika adekvata antiepileptika i relevanta doser uppfyller kriterierna för läkemedelsresistens [16]. Andra terapeutiska möjligheter, till exempel kirurgi, bör då övervägas, men för flertalet är fortsatta försök med läkemedelsbehandling, ofta i olika kombinationer, det rimligaste.
I Sverige finns 16 olika läkemedel godkända för tilläggsbehandling vid läkemedelsresistent fokal epilepsi och 9 godkända som tillägg vid generaliserade tonisk-kloniska anfall. Antalet möjliga kombinationer är närmast oändliga, och systematiska jämförelser mellan olika specifika kombinationer saknas. Utöver visad effekt som tilläggsbehandling vid aktuell typ av epilepsi styrs valet av tilläggsbehandling ofta av effekter (gynnsamma och negativa) på patientens eventuella samsjuklighet och önskemålet att undvika läkemedelsinteraktioner [17].
När ska man överväga att avsluta behandling?
Flertalet patienter blir anfallsfria under behandling, och hos många kan epilepsin så småningom läka ut. Det kan då bli aktuellt att överväga att avsluta behandlingen. Tidigare har praxis varit att ta ställning efter 1–2 års anfallsfrihet hos barn och efter 4–5 år hos vuxna, men detta måste bedömas individuellt. Det går inte att med säkerhet avgöra om fortsatt behandling behövs utan att pröva utsättning. En riskbedömning för återfall har nyligen presenterats baserad på följande faktorer: anfallsfri tid före uttrappning av antiepileptiska läkemedel (längre tid – lägre risk), antal år med epilepsi före remission (fler år – högre risk), ålder vid epilepsidebut (vuxen – högre risk), tidigare feberutlösta anfall (högre risk), antal anfall före anfallsfrihet (ökar risk), förekomst av självbegränsande epilepsisyndrom (lägre risk), intellektuell funktionsstörning (ökad risk) och onormalt EEG (ökad risk) [18].
Denna riskbedömning är komplicerad och kräver specialistkunskap men möjliggör en individuell värdering av risk för återfall som i extremfallen kan variera från 10 till 90 procent. Oavsett nivå på kalkylerad risk är det den informerade patientens inställning som avgör om man är villig att pröva att avsluta behandlingen. Konsekvenserna av ett återfall varierar bland annat med typ av anfall och livssituation, men kan vara betydande. En lägre andel (9 procent) av dem som får återfall i samband med utsättningsförsök återfår inte full anfallskontroll trots återinsatt behandling [18].
Slutsatser
Nya antiepileptika har ökat valmöjligheterna men inte nämnvärt förändrat behandlingsutfall eller principer. De har möjliggjort en högre grad av individualisering, vilket är viktigt i epilepsibehandling, avseende såväl indikation och val av läkemedel som dosering. Behandlingen är fortfarande symtomatisk, men framtiden kan innebära sjukdomsmodifierande precisionsmedicin riktad mot olika specifika epilepsisyndrom.
Potentiella bindningar eller jävsförhållanden: Torbjörn Tomson har erhållit anslag till graviditetsregistret EURAP från Bial, Eisai, GlaxoSmithKline, Novartis och UCB, arvode till sin klinik för föreläsningar från UCB, Eisai, Livanova och Sandoz samt arvode till sin klinik för medverkan i rådgivande kommitté för Eisai och UCB.
Olof Rask har erhållit arvode för föreläsningar från Novartis.