Alla laboratorieresultat, oavsett typ, har en större eller mindre osäkerhet.
Extern kvalitetssäkring (EQA) kan användas för att belysa hur riktiga resultaten är och vilka metodskillnader som finns.
Kvalitetsmål för hur noggranna resultaten ska vara bör bestämmas i diskussion mellan kliniker, laboratorier och EQA-organisatörer.
Laboratorieresultat ligger till grund för ett stort antal beslut i sjukvården. Vissa resultat är rent diagnostiska och leder direkt fram till en diagnos, medan andra avgör val av fortsatt utredning eller styr behandling på olika sätt. Felaktiga laboratorieresultat kan därmed leda till felaktiga beslut och i värsta fall felaktig diagnos med fel eller onödig behandling och tillhörande kostnader.
Alla laboratorieresultat har en viss osäkerhet. Det är vanligt att skilja mellan preanalytisk, analytisk och postanalytisk osäkerhet:
- Den preanalytiska osäkerheten omfattar allt i processen före undersökningen på laboratoriet, såsom provtagning på patienten och hantering och transport av provmaterialet.
- Den analytiska osäkerheten omfattar osäkerheten vid själva undersökningen på laboratoriet, dvs hur säkert resultatet från testet/instrumentet eller bedömningen är.
- Den postanalytiska osäkerheten omfattar rapportering till och tolkning av resultat hos beställaren.
I de flesta fall är den samlade osäkerheten försumbar i förhållande till referensintervalls- eller åtgärdsgränser, men i andra fall kan den påverka den kliniska handläggningen. Därför är det viktigt att känna till osäkerheten i resultatet. Hur stor är osäkerheten när laboratoriet rapporterar att HbA1c-värdet är 53 mmol/mol? Är det verkliga resultatet inom intervallet 43–63 mmol/mol eller är det inom 50–55 mmol/mol? Eftersom beslutsgränsen för diabetesdiagnos är 48 mmol/mol innebär osäkerheten att ett resultat inom det förstnämnda intervallet inte säkert är över beslutsgränsen, medan ett resultat inom det andra intervallet med säkerhet är över beslutsgränsen.
Hur osäkert är resultatet av ett snabbtest för streptokocker (Strep A-test)? Kan vi lita på att ett positivt resultat alltid blir positivt, även om testet upprepas 100 gånger? Eller blir det positivt vid endast hälften av tillfällena? Och hur stor är sannolikheten att en patient har halsfluss om testet blir positivt?
Om ett födelsemärke opereras bort, och provsvaret i utlåtandet från PAD-undersökning vid patologiavdelningen lyder »dysplastiskt nevus, höggradig dysplasi« – hur säkert är svaret? Skulle vi få samma svar om provet hade bedömts av en annan patolog?
Frågor av den här typen ställer kanske inte användaren så ofta. I allmänhet litar beställare och patient mycket på laboratorieresultatet, och det är laboratoriets uppgift att se till att osäkerheten i resultatet ligger på en kliniskt acceptabel nivå. Men vilka grunder finns det egentligen för att lita på ett resultat? Laboratorier kan testa sina metoder med interna kontroller, dvs provmaterial med känt innehåll, och kan på så sätt dagligen kontrollera att resultaten blir de förväntade.
Men det är också viktigt att känna till hur resultaten står sig i förhållande till resultat från andra laboratorier som använder samma eller liknande undersökningsmetoder. Equalis är en organisation som ägs av Sveriges Kommuner och landsting, Institutet för biomedicinsk laboratorievetenskap och Svenska läkaresällskapet och som har till uppgift att arrangera jämförelser av resultat från laboratorieundersökningar mellan laboratorier i och utanför Sverige, s k extern kvalitetssäkring (kompetensprövning, EQA). Verksamheten är helt finansierad av deltagaravgifter, och deltagandet är frivilligt.
Extern kvalitetssäkring
Extern kvalitetssäkring innebär att ett okänt provmaterial, identiskt för alla, undersöks av deltagande laboratorier. Utfallet visar hur harmoniserade resultaten är mellan deltagande laboratorier och vilka metodskillnader som finns. I de fall där ett sant värde är känt får vi även veta hur standardiserade och riktiga resultaten är.
Det är nödvändigt för ackrediterade laboratorier att på något sätt visa resultat av jämförelser med andra laboratorier, t ex genom att delta i EQA [1]. Laboratorierna publicerar i allmänhet inte resultaten av dessa jämförelser, men de används internt för att visa hur bra man klarar av att mäta på ett provmaterial och vid behov förbättra metoden.
Exemplet HbA1c
HbA1c är ett välkänt prov för uppföljning av patienter med diabetes, och det kan numera även användas för diagnos av sjukdomen [2]. Equalis började redan 1994 att regelbundet sända ut provmaterial till laboratorier som mätte HbA1c. De kvalitetsmål som vi i dag har är kliniskt relevanta och har tagits fram i samarbete mellan Equalis, barn- och vuxendiabetologer, diabetessjuksköterskor, Svensk förening för klinisk kemi samt patientföreningen Diabetesförbundet [3].
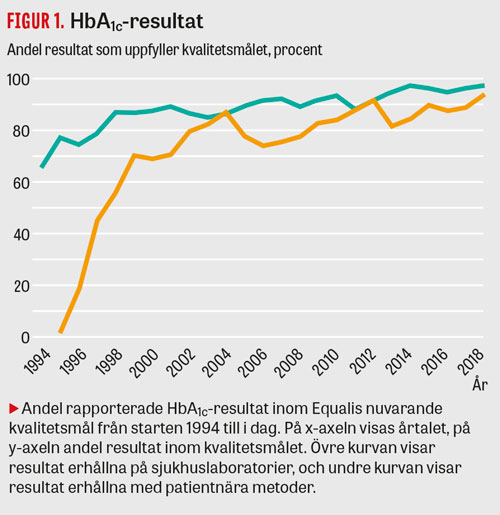
Kvalitetsmålen har med tiden skärpts till dem vi har i dag. I mitten av 1990-talet skulle dagens kvalitetsmål för HbA1c-analysen ha uppfyllts av endast drygt hälften av sjukhuslaboratorierna. I slutet av 1990-talet introducerades patientnära HbA1c-metoder, som då hade ungefär samma kvalitet som laboratoriemetoderna haft 10 år tidigare.
Tack vare återkoppling av resultaten från EQA till laboratorier och tillverkare samt ett internationellt standardiseringsarbete har noggrannheten successivt förbättrats så att kvalitetsmålet för både laboratoriemetoder och patientnära metoder i dag uppfylls på den svenska marknaden [4]. Ett HbA1c-resultat från ett laboratorium i Sverige på 53 mmol/mol varierar nu med högst ±4 mmol/mol om det skulle skickas till ett annat laboratorium i Sverige för kontrollmätning; i de allra flesta fall är variationen till och med mycket mindre än så.
Figur 1 visar hur stor andel av resultaten i Equalis kvalitetssäkringsprogram som uppfyllde det aktuella kvalitetsmålet från 1994 till september 2018. Under 2018 (till september) uppfyllde 97 procent av resultaten med sjukhuslaboratoriemetoderna och 94 procent av dem som rapporterats med patientnära metoder kvalitetsmålet.
Exemplet snabbtest för streptokocker
Halsprov för snabbtest av Streptococcus pyogenes (Strep A-test) är ett vida erkänt förfarande vid diagnos av halsfluss, den vanligaste halsinfektionen orsakad av bakterier. För diagnostiska test, där ett positivt utslag tolkas som utryck för en viss diagnos, brukar diagnostisk specificitet och sensitivitet beräknas i förhållande till etablerad standard. Diagnostisk specificitet är testets förmåga att detektera just S pyogenes och inte andra bakterier, dvs att resultatet blir negativt om patienten inte har en Streptococcus pyogenes-infektion. Diagnostisk sensitivitet är ett mått på att resultatet blir positivt om patienten har en S pyogenes-infektion, vilket har visat sig variera mycket mellan olika snabbtest [5].
Trots detta finns inga globala kvalitetsmål för ovanstående parametrar för snabbtest, och prioritering av hur viktiga parametrarna anses vara varierar i olika delar av världen, vilket speglas i utvecklingen av snabbtesten. Men hur upphandlas den typ av test som passar lokala riktlinjer?
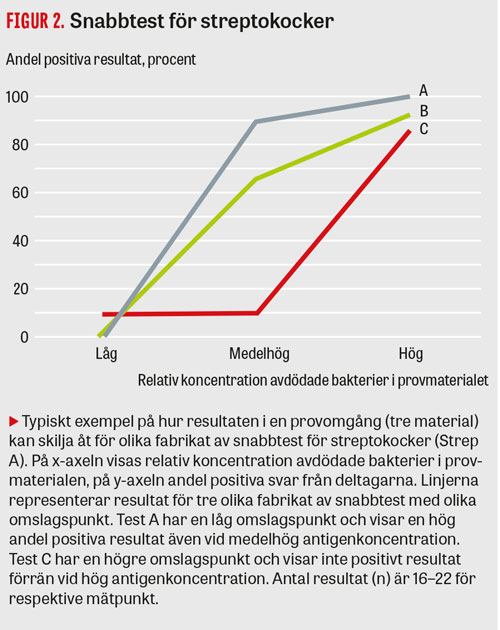
Equalis kvalitetssäkringsprogram för Strep A-test visar de analytiska egenskaperna av snabbtestet. Deltagarna erhåller material med avdödade bakterier i olika antigenkoncentrationer, okända för deltagarna, för mätning med snabbtest. I rapporterna från Equalis kan deltagarna sedan se både sina egna resultat och inrapporterade resultat från andra, avidentifierade, deltagare. Därmed fås en överblick av prestationen hos olika fabrikat av snabbtest på den svenska marknaden.
Figur 2 visar en sammanfattning av hur tre olika test (A, B och C) presterar. För provmaterial med låg respektive hög antigenkoncentration får en stor andel av deltagarna ett negativt respektive positivt resultat. För svagt positiva prov skiljer sig däremot testen åt på grund av att de har olika omslagspunkt (detektionsnivå eller analytisk sensitivitet).
I Sverige jobbas det aktivt för att minska antibiotikaanvändning vid faryngit [6] samtidigt som risken för allvarliga komplikationer vid halsfluss är liten. För att minska risken att fånga passiva bärare av streptokocker i testen är strategin att endast använda snabbtest om minst tre Centor-kriterier [7-9] är uppfyllda. Equalis resultat kan alltså användas dels för att se hur det »egna« snabbtestet presterar gentemot facit, dvs hur säkra resultaten är, dels för att ge vägledning vid val av testfabrikat.
SKUP (Skandinavisk utprövning av laboratorieutrustning för patientnära analyser) är ett skandinaviskt samarbete för oberoende utprövningar. I de senare SKUP-utprövningarna av Strep A-test ingår både provtagning och analys av halsprov från patienter på vårdcentraler, därmed finns även den preanalytiska delen med i beräkningar av testens analytiska kvalitet [10, 11]. Facit i SKUP-utprövningar är odlingsresultat av motsvarande patientprov. Snabbtestens analytiska kvalitet och användarvänlighet bör tillmätas större betydelse i förhållande till priset än vad som ofta är fallet vid dagens upphandlingar av test. SKUP:s rapporter finns publikt tillgängliga på www.SKUP.org.
Exemplet patologiområdet
Inom området patologi skickar Equalis ut digitalt provmaterial för bedömning av patologer. I verkligheten är det många variabler som bedöms vid en histopatologisk undersökning, men i Equalis omgångar väljs någon eller några variabler ut för bedömning, t ex den mest sannolika diagnosen av ett antal valbara alternativ i enlighet med en överenskommen klassifikation. Resultaten jämförs sedan med det förväntade resultatet, som är framtaget av en grupp experter, men även överensstämmelsen patologer sinsemellan bedöms.
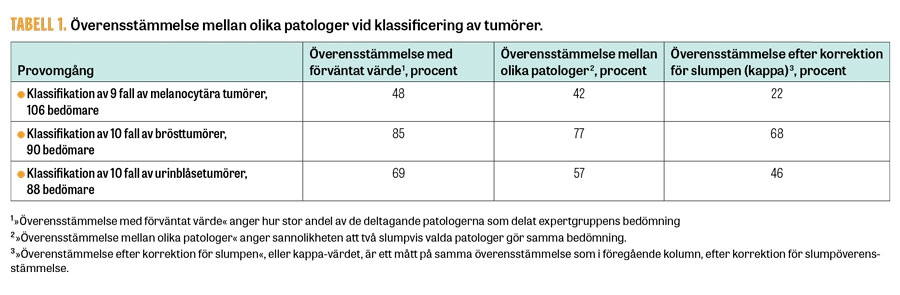
I Tabell 1 ges exempel från tre aktuella omgångar från Equalis i vilka ca 100 patologer deltagit och bedömt digitala bilder utvalda av en grupp experter. Frågeställningarna har gällt klassificering av tumörer i hudbiopsier, biopsier från urinblåsa och bröstpreparat. Att döma av resultaten är överensstämmelsen både mot det förväntade resultatet och mellan patologer bäst för klassificering av brösttumörer, medan det är sämst för klassificering av melanocytära tumörer i huden.
Diskussion
Ambitionen för EQA är förstås att provomgångarna ska motsvara den kliniska verkligheten så bra som möjligt. Genom att delta i den här typen av jämförelser kan laboratorierna visa sin kompetens och ackreditera sina laboratoriemetoder. EQA kan också visa hur prestanda för metoder och för enskilda laboratorier varierar över tid.
Den osäkerhet i laboratorieresultaten som vi gett exempel på här är förstås begränsad till den osäkerhet som uppstår under laboratoriearbetet och behöver av den anledningen inte säkert motsvara den som gäller för autentiska patientprov, där ju själva provtagningsproceduren också bidrar till osäkerhet i slutresultatet. Vidare kan provmaterialet bestå av samlat provmaterial som inte är helt representativt för en enskild patient (HbA1c), vara artificiellt framställt (Strep A-test) eller bestå av selekterade patientprov som är särskilt besvärliga eller svårbedömda (patologi).
För kvantitativa mätresultat är vi vana vid att uttrycka en mätosäkerhet numeriskt. Resultatet av en histopatologisk undersökning är däremot inte numeriskt, utan kan vara resultatet av en klassifikation av ett tillstånd eller en diagnos. Den osäkerhet som finns i resultatet kan ibland uttryckas verbalt i det fritt formulerade svaret från patologen. Däremot beskrivs sällan osäkerheten, eller graden av överensstämmelse, mellan olika bedömare på något numeriskt sätt. För att kunna beskriva hur stor den osäkerheten är och jämföra den med andra material behöver den mätas och uttryckas numeriskt på något sätt. De numeriska värdena för överensstämmelse av histopatologiska bedömningar som vi redovisar här (Tabell 1) är i samma storleksordning som har beskrivits för motsvarande bedömningar i internationella studier [12-14]. De är alltså inte exempel på anmärkningsvärt stora osäkerheter, men kan ligga till grund för diskussion om det är önskvärt att förbättra överensstämmelsen.
Sammanfattning
Sammanfattningsvis finns det således en osäkerhet i alla laboratorieresultat. Osäkerheten beror delvis på analysmetoden som sådan, delvis på hur analysen utförs vid det lokala laboratoriet och på egenskaper i det enskilda patientprovet. Vi vill poängtera att osäkerheten inte är något fel i betydelsen misstag, utan ett omvänt mått på hur noggrant resultatet är.
Hur noggrannheten kan beskrivas i en siffra varierar beroende på om resultatet är ett numeriskt värde (HbA1c), ett resultat av typ »negativt/positivt« (Strep A-test) eller ett svar på nominalskalan (ett kategoriskt svar, t ex histopatologisk diagnos).
Av flera skäl är det viktigt för både laboratorier och användare av laboratorieresultat att känna till storleken av denna osäkerhet [15]:
- Noggrannheten har betydelse för hur det enskilda resultatet ska bedömas.
- Användarna behöver tillsammans med laboratoriet diskutera och ta ställning till om noggrannheten är tillräckligt bra som den är, dvs om kvalitetsmålen uppnås [16, 17]. Om den inte är det, måste det arbetas för att förbättra noggrannheten till önskvärd nivå.
Arbetet med HbA1c är ett bra exempel på ett systematiskt förbättringsarbete som successivt lett fram till den höga kvalitet analysen har i dag. För flera andra analyser gäller också att den analytiska kvaliteten successivt har förbättrats.
En förutsättning för att i framtiden kunna förbättra noggrannheten av laboratorieresultatet, där så behövs, är att känna till hur stor den är i dag. Ett av verktygen för att beskriva noggrannheten är extern kvalitetssäkring.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.