Transfusioner ska ges på medicinsk indikation och efter en helhetsbedömning av den enskilda patienten.
För underburna barn bör olika transfusionsgränser för erytrocytkoncentrat användas beroende på postnatal ålder och sjukdomsgrad.
Hemodynamiskt stabila fullgångna barnintensivvårdspatienter behöver oftast inte transfunderas vid hemoglobinnivå >70 g/l.
Protokoll för massiv transfusion till barnpatienter ska finnas. Ett sådant protokoll bör innefatta balanserad transfusion av erytrocytkoncentrat, färskfrusen plasma och trombocytkoncentrat.
Vid leversjukdom kan transfusioner bidra till ökad blödning.
Nyfödda har generellt höga hemoglobinnivåer, men nivåerna ligger därefter lägre än hos vuxna under resten av uppväxten. Särskilt under spädbarns- och småbarnsåldern präglas det hemostatiska systemet av en mycket dynamisk process som i litteraturen benämns som »developmental hemostasis«, vilket återspeglas i de åldersrelaterade referensintervallen [1]. Riktlinjer för transfusioner skiljer sig därför åt mellan neonatalperioden och övriga åldrar, men även andra hänsynstaganden behöver tas vid olika pediatriska tillstånd. I denna artikel diskuteras några av de vanligaste situationerna inom pediatriken där blodtransfusioner kan bli aktuella.
Transfusioner under den neonatala perioden
Erytrocytkoncentrattransfusion är en av de vanligaste behandlingarna på neonatalavdelningen. Studier har visat att ca 80 procent av nyfödda med födelsevikt <1 500 g får erytrocytkoncentrat vid åtminstone ett tillfälle under vårdtiden på neonatalavdelning. Neonatal anemi är vanligt förekommande, och alla nyfödda (både fullgångna och underburna) får sjunkande Hb under den fysiologiska adaptationen till en relativt syrgasrik extrauterin miljö. Hos underburna sjunker Hb snabbare och kraftigare på grund av ytterligare faktorer: fysiologiska (lägre EPO-nivå, minskat svar på EPO), patofysiologiska (infektion, hemolys, försämrad erytrocytproduktion) och iatrogena (blodprovstagning) [2, 3]. Lågt Hb tolkas ofta som en markör för minskad syrgastransportkapacitet och försämrad syresättning i vävnaden, vilket kan förbättras med erytrocytkoncentrattransfusion. Optimal syresättning i vävnaden är särskilt viktig för nyfödda i deras utveckling, inte minst för hjärnan.
Transfusion har dock sina risker. Bland dessa finns transfusionsassocierad lungskada, transfusionsassocierad cirkulatorisk belastning, järnöverskott, infektion och hemolytiska reaktioner.
Trots Hb:s betydelse för vävnadens syresättning är det oklart vid vilken Hb-nivå nyttan av erytrocytkoncentrattransfusion överväger riskerna hos underburna. Frågan kompliceras ytterligare av att syrgaskonsumtionen sannolikt är högre hos svårt sjuka än hos stabila patienter, samtidigt som fetalt Hb successivt minskar med postnatal ålder, vilket påverkar syretransporten på vävnadsnivå. Vidare högerförskjuts hemoglobinets dissociationskurva när fetalt Hb byts ut mot transfunderat adult Hb. Dessa faktorer talar för att olika transfusionströsklar bör användas vid olika postnatal ålder och vid olika sjukdomsgrad (oftast graderat enligt andningsunderstödsnivåer hos nyfödda) (se Tabell 1) [4, 5]. Gällande transfusionsvolym kan större volymer (15–20 ml/kg) vara fördelaktiga genom att antalet donatorexponeringar minskar.
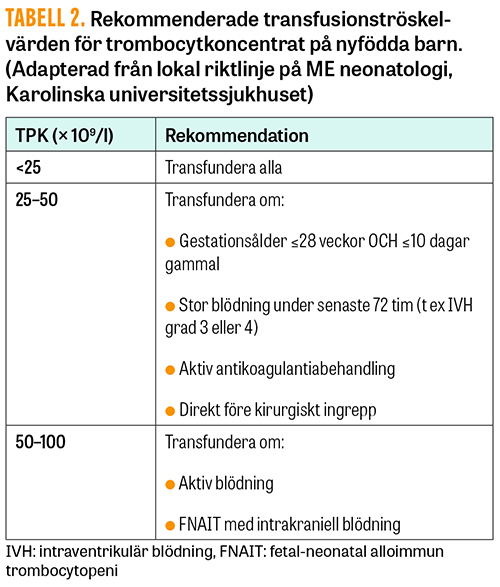
Trombocyttransfusion är i nuläget den enda behandlingsformen för icke-immunmedierad trombocytopeni. Nyfödda transfunderas generellt vid högre trombocytnivåer än större barn och vuxna på grund av dels bristande evidens för transfusionsbeslut, dels den kända hyporeaktiviteten hos trombocyter, dels den stora blödningsrisken hos underburna/sjuka nyfödda [6]. I nuläget är trombocytpartikelkoncentrationsnivå (TPK) den enda markören som används för att styra transfusion, men andra metoder är under utveckling. Tilltagande evidens tyder på att blödningsrisk är multifaktoriell och ska relateras till gestationsålder (≤28 veckor), postnatal ålder (≤10 dagar) och kliniskt status (t ex infektion, nekrotiserande enterokolit) (se Tabell 2). Nyligen har en randomiserad studie visat en stark association mellan antal trombocyttransfusioner och ökad morbiditet och mortalitet, vilket bör övervägas vid transfusionsbeslutet [7]. Transfusion görs med 10–15 ml/kg av trombocytkoncentrat från slumpmässigt utvald donator under 30–60 min.
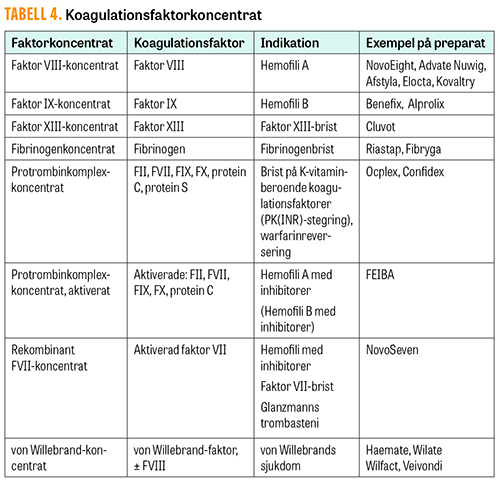
Generellt är PK(INR) och APTT förlängda hos nyfödda jämfört med vuxna, och avvikande värden hos nyfödda har begränsningar i att kunna förutspå kliniska blödningar [8, 9]. Generellt är färskfrusen plasma förstahandsval som behandlingsmetod vid akut blödning i kombination med koagulationsrubbning. 10–15 ml/kg färskfrusen plasma anses vara en effektiv dos. Det saknas dock data för huruvida färskfrusen plasma till icke-blödande neonatala patienter minskar risken för blödning. Vid svår blödning i kombination med svår koagulationsrubbning bör koagulationsfaktorkoncentrat övervägas (se Tabell 4).
Transfusion inom barnintensivvård
Blodtransfusion är vanligt förekommande inom barnintensivvården. Inför beslut om eventuell blodtransfusion bör inte bara Hb-värdet tas i beaktande, utan även andra faktorer behöver vägas in, till exempel respiratorisk/cirkulatorisk instabilitet, pågående blödning och underliggande sjukdomar [10].
För fullgångna, hemodynamiskt stabila barn rekommenderar internationella riktlinjer att transfusion inte påbörjas när Hb överstiger 70 g/l [11]. TRIPICU-studien från 2007 randomiserade hemodynamiskt stabila intensivvårdade barn till transfusionsgräns Hb 70 g/l eller Hb 95 g/l [12]. Ingen skillnad fanns mellan grupperna i kliniskt utfall, men transfusionsbehovet reducerades kraftigt i gruppen med lägre transfusionsgräns. Hemodynamisk stabilitet definierades som ett medelartärtryck högre än –2 SD för åldern och att kardiovaskulärt stöd (vasoaktiva läkemedel eller vätskebehandling) inte ökats under de senaste två timmarna.
Högre transfusionsgränser kan behövas för vissa grupper, till exempel vid medfödd hjärtsjukdom, hemodynamisk instabilitet och chock, svår hypoxisk andningssvikt, akut hjärnskada eller sicklecellsjukdom med akut bröstsyndrom. Det finns dock mycket få kliniska tillstånd som motiverar en transfusionsgräns Hb >100 g/l.
Indikation för tillförsel av färskfrusen plasma föreligger främst vid balanserad transfusion i samband med större blödning, men även i utvalda fall för att korrigera koagulationsrubbningar. Användning av färskfrusen plasma som volymsubstitution rekommenderas inte.
Transfusion vid traumatisk blödning hos barn
Grundprinciperna för hantering av pediatrisk traumatisk blödning skiljer sig inte från dem som används inom vuxentrauma, och traumainducerad koagulopati förekommer även hos barn [13]. Vid stor traumatisk blödning är huvudprincipen att undvika tillförsel av större mängd kristalloid vätska och i stället tidigt initiera massivt transfusionsprotokoll med balanserad transfusion av erytrocytkoncentrat, färskfrusen plasma och trombocytkoncentrat enligt principer för hemostatisk resuscitering [14]. På Karolinska universitetssjukhuset initieras massivt transfusionsprotokoll genast vid uppenbar stor traumatisk blödning, och i övriga fall senast vid utebliven stabilisering efter tillförsel av 20 ml/kg kristalloid vätska.
Stor traumatisk blödning hos barn är relativt sällsynt, och inget evidensbaserat protokoll för pediatrisk massiv transfusion finns. Enligt det protokoll för massiv transfusion som används på Karolinska ges erytrocytkoncentrat, färskfrusen plasma och trombocytkoncentrat i kvot 20:20:10 ml/kg till barn med vikt <50 kg. 5–10 ml/kg av erytrocytkoncentrat och färskfrusen plasma bör ges omväxlande. För barn >50 kg används vuxenprotokoll med kvoten 4:4:1. Vid stor traumatisk blödning är målvärdet för Hb 100 g/l och för TPK 100 × 109/l.
Transfusion vid övrig pediatrisk blödning
Vid mindre, ej livshotande blödning hos hemodynamiskt stabila barn rekommenderar internationella riktlinjer att blodtransfusion ej ges vid Hb >70 g/l [14]. Vid stor blödning kan transfusionsgränsen behöva vara högre – motiverar en transfusionsgräns högre än Hb 100 g/l – och även tillförsel av färskfrusen plasma och trombocyter ska övervägas. På Karolinska initieras balanserad transfusion av erytrocytkoncentrat, färskfrusen plasma och trombocyter senast efter att 20 ml/kg erytrocytkoncentrat transfunderats.
Transfusioner inom barnonkologi och barnhematologi
Inom barnonkologi och barnhematologi föreligger frekvent behov av transfusioner, vilket beror på barnets grundsjukdom och/eller behandling av sjukdomen. Trots att det rör sig om relativt få barn är det en heterogen grupp med olika behov och i många fall individualiserade behandlingar. Dessa barn behandlas primärt på sex barnonkologiska centrum men vårdas även på sina hemsjukhus. Behov av transfusion ska inte beslutas efter ett enskilt provsvar, utan en helhetsbedömning rekommenderas inklusive den bakomliggande onkologiska/hematologiska sjukdomen [15].
Transfusion med erytrocytkoncentrat ges generellt sett vid ett Hb-värde <80 g/l, men vid strålbehandling samt vid behandling med platinapreparat önskas ett Hb-värde >100 g/l för att minska risken för biverkningar (t ex hörselnedsättning). Vid stamcellstransplantation används filtrerade och bestrålade produkter så länge immunsuppressionen så kräver, och transfusionsgränsen kan vara lite mer liberal innan benmärgsanslag skett. Till barn med kroniska anemier (t ex talassemier, sicklecellanemi, Diamond–Blackfans anemi) följs riktlinjer från WHO [16] samt lokala riktlinjer från Vårdplaneringsgruppen för pediatrisk hematologi inom Barnläkarföreningen [17]. Matchade erytrocytkoncentrat ges till dessa barn för att minska risken för immunisering. Målet är vid de flesta kroniska anemier att som lägst hålla Hb-nivån på 95–100 g/l. Vid upprepade transfusioner under lång tid ges järnbindande behandling (kelering). Vid svår anemi kan volymen erytrocytkoncentrat behöva reduceras och infusionstiden förlängas; i övrigt se Tabell 3.
Trombocyttransfusion ges generellt sett till barn med onkologisk sjukdom vid TPK <15–20 × 109/l samt under 50 × 109/l inför lumbalpunktion. Till barn med hematologisk sjukdom och dem som planeras för stamcellstransplantation intas en mer restriktiv hållning vid trombocytopeni; för att minska risken för immunisering ges trombocyttransfusion först vid blödningssymtom. Matchade trombocyter används i särskilda fall. Vid idiopatisk/immunmedierad trombocytopen purpura (ITP), som är relativt vanlig hos småbarn, saknas i princip indikation för trombocyttransfusion [17].
Plasmaprodukter behöver sällan användas inom barnonkologi och hematologi, men kan behöva ges till barn med oklar koagulationspåverkan. I första hand strävas efter att ge faktorkoncentrat med den specifika koagulationsfaktor som det är brist på (Tabell 4). Granulocyttransfusion ges endast i särskilda väl utvalda fall.
Transfusioner inom barnhepatologi
De flesta koagulationsfaktorer bildas i levern, och nedsatt leversyntesfunktion kan leda till påverkan på rutinkoagulationsanalyser, såsom PK(INR) och fibrinogen, vid både akut och kronisk leversjukdom. I levern bildas även koagulationshämmande proteiner (t ex antitrombin, protein C och protein S). Vid leversjukdom fås en ny balans mellan koagulationsfaktorer och hämmare, vilket innebär att lägre nivåer av koagulationsfaktorer kan tolereras utan ökad blödningsrisk, även om balansen kan vara skörare. Man bör därför undvika att korrigera koagulationssystemet i frånvaro av blödning. Barn med gallstas kan utveckla K-vitaminbrist som kan leda till ytterligare sänkning av K-vitaminberoende koagulationsfaktorer, och detta kan öka blödningsrisken. K-vitaminsubstitution rekommenderas därför vid gallstas. Det är även vanligt att trombocytnivåerna är sänkta vid leversjukdom sekundärt till bland annat hypersplenism. Denna trombocytopeni kan delvis kompenseras av att faktor VIII och von Willebrand-faktor ofta är förhöjda vid leversjukdom [18, 19].
Blödningar från gastrointestinala varicer beror främst på ökat tryck i portakretsloppet (portal hypertension). Transfusioner kan i dessa fall leda till ytterligare tryckstegring och därmed ökad blödning. I stället rekommenderas sänkning av portatrycket med hjälp av vasoaktiva läkemedel (t ex oktreotid) följt av ligering eller sklerosering av varicerna. Vid utebliven effekt av ovanstående och allvarlig blödning kan erytrocytkoncentrat övervägas vid Hb 70–80 g/l och trombocyttransfusion vid TPK <20–50 × 109/l. Färskfrusen plasma bör undvikas på grund av risk för volymbelastning, och koagulationsfaktorkoncentrat kan i stället övervägas vid uttalad koagulationsrubbning i samråd med barnhepatolog eller barnkoagulationskonsult.
Inför invasiva ingrepp bör individuell bedömning göras av huruvida eventuell preoperativ behandling behövs baserat på typ av ingrepp, eventuell uppvisad blödnings- eller trombostendens, koagulationsstatus och om riskfaktorer föreligger som kan tippa balansen mot ökad blödningsrisk, t ex infektion, njursvikt, akut leversjukdom, akut-på-kronisk leversvikt, fokala leverförändringar eller hematologisk sjukdom. Trombocyttransfusion kan bli aktuell vid högriskingrepp om TPK är < 50 × 109/l. Eventuell behandling med koagulationsfaktorkoncentrat (t ex fibrinogenkoncentrat) ges i dialog med barnhepatolog och eventuellt barnkoagulationskonsult [20].
Läs författarintervjun:
5 frågor till Emöke Deschmann
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
(uppdaterad 2021-03-17)