En sällsynt diagnos definieras inom EU som en sjukdom som berör färre än 1/2 000.
Ca 300 miljoner människor i världen och 400 000 svenskar är drabbade.
Det finns ca 7 000 olika sällsynta diagnoser.
Den kliniska bilden varierar från ett avgränsat symtom till multipla symtom från flera organ, ofta även med kognitiv och motorisk påverkan.
Minst 72 procent är genetiskt orsakade, och 70 procent debuterar i barndomen.
Många patienter är odiagnostiserade och får inte optimal vård.
I dag finns behandling för endast 5 procent av alla sällsynta diagnoser.
Med modern gensekvensering kan sjukdomsorsakande mutationer identifieras, vilket ger möjlighet till skräddarsydd behandling och prevention styrd utifrån individens genetiska förutsättningar, det vill säga precisionsmedicin.
Sällsynta diagnoser (rare diseases; även kallade sällsynta hälsotillstånd eller sällsynta tillstånd) definieras inom EU som sjukdomar som förekommer hos 1/2 000 eller färre. De utgör en stor och heterogen grupp av sjukdomar som innefattar uppskattningsvis 7 000 olika tillstånd [1-3]. Även om varje individuell sjukdom är ovanlig är sällsynta diagnoser som grupp mycket vanligare och mer betydelsefulla än namnet antyder. Man räknar med att 3,5–5,9 procent av alla människor har en sällsynt diagnos, vilket innebär att över 400 000 personer i Sverige är påverkade [1]. Gemensamt för dem alla är den speciella problematik som beror på att diagnosen är sällsynt och därmed ofta okänd. För många tar det lång tid att få en diagnos, och även efter bekräftad diagnos finns utmaningar i form av begränsad kunskap inom vården och samhällets olika funktioner. Andra får aldrig en diagnos och informeras inte heller om möjligheten att remitteras för utredning. Riktad behandling finns i dag endast för 5 procent av alla sällsynta diagnoser [4], men utvecklingen går snabbt framåt och hundratals nya behandlingar är på väg att godkännas under de närmaste fem åren. I Tabell 1 finns exempel på sällsynta diagnoser där genetisk diagnos påverkar valet av behandling.
Genetisk diagnostik
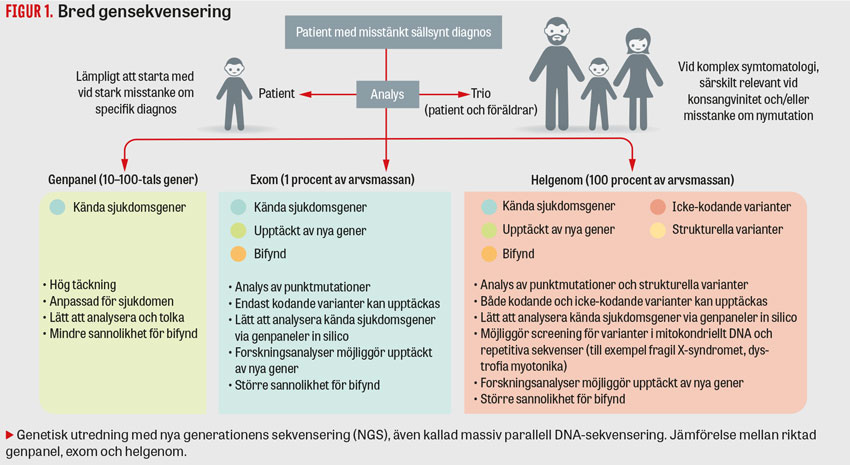
Genetiskt orsakade sällsynta diagnoser inkluderar kromosomavvikelser, monogena sjukdomar samt mitokondriella sjukdomar. I januari 2021 har nästan 6 000 olika gener kopplats till monogena sällsynta diagnoser [5]. Identifiering och karakterisering av genetiska sjukdomar genomgår för närvarande en dramatisk förändring, vilket markant förbättrat möjligheterna att diagnostisera genetiska orsaker till sällsynta sjukdomar. Tekniken NGS, nya generationens sekvensering (även kallad massiv parallell DNA-sekvensering), har möjliggjort att man vid en och samma analys kan sekvensera stora delar av eller hela arvsmassan (Figur 1). Beroende på frågeställning och tillgänglig utrustning kan man välja att sekvensera 1) genpaneler som innehåller ett begränsat antal gener som kan vara aktuella vid de symtom patienten uppvisar, 2) hela exomet, det vill säga alla kodande delar (exon) i alla 20 000 humana gener eller 3) hela arvsmassan (så kallad helgenomsekvensering), det vill säga såväl kodande (exon) som icke-kodande delar, både inom gener (intron) och mellan gener (intergen sekvens) (Figur 1). Tekniksprånget har lett till bättre klinisk diagnostik, och det är i dag enklare, snabbare och billigare att ställa en genetisk diagnos jämfört med för ett antal år sedan, då man endast kunde analysera en gen i taget med sammantaget hög analyskostnad för varje patient. Den första humana genomanalysen publicerades 2003 till en kostnad av tusen miljoner dollar, och under många år var kostnaden alldeles för hög för implementering i klinisk diagnostik [6]. I dag kostar en klinisk helgenomanalys ca 10 000 kr i reagenskostnader, och sedan tillkommer övriga kostnader inkluderande bioinformatik, datalagring samt dataanalys och klinisk tolkning.
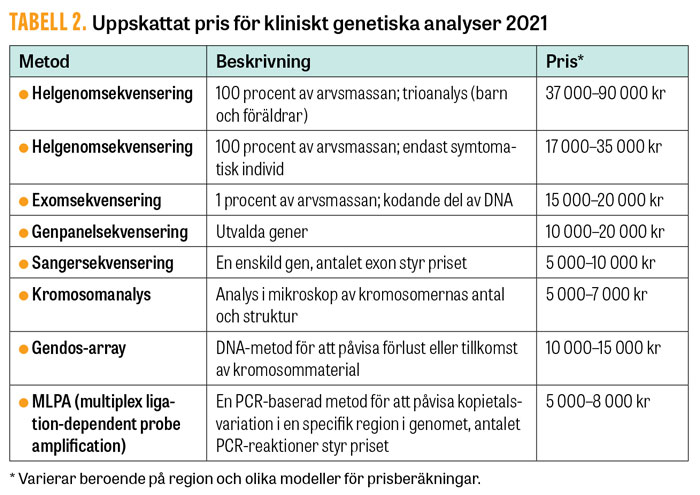
Diagnostik med exomsekvensering i hälso- och sjukvården har redan gett stor patientnytta. Internationella studier har visat att den genomsnittliga andelen av pediatriska patienter som får en genetisk diagnos vid exomsekvensering är 27 procent för enstaka patienter och 34 procent vid trioanalyser [7], det vill säga samtidig analys av till exempel ett barn med symtom och dess båda föräldrar. För högt selekterade patientgrupper kan upp till 90 procent erhålla en diagnos [8]. Helgenomsekvensering som inkluderar 100 procent av arvsmassan och människans alla ca 20 000 gener är bara marginellt dyrare än traditionella genanalyser (Tabell 2).
Data från helgenomsekvensering kan även bearbetas med olika bioinformatiska program för att utöver punktmutationer detektera andra typer av genetiska varianter (till exempel deletioner, duplikationer, expansioner och insertioner), vilket innebär att analysen har potential att ersätta flera traditionella genetiska analyser, som gendos-array, Sangersekvensering och MLPA (multiplex ligation-dependent probe amplification), vilket ytterligare ökar kostnadseffektiviteten (Tabell 2). I Fakta 1 beskrivs ett tydligt exempel på hur en diagnos kunde ställas direkt med helgenomsekvensering efter att både exomsekvensering och gendos-array givit inkonklusiva resultat.
Ett fåtal studier har publicerats som tydligt visar klinisk nytta av helgenomsekvensering som första genetiska analys: svenska resultat har visat att andelen av 100 individer remitterade för gendos-array som fick en genetisk diagnos ökade med 15 procent (från 12 till 27 procent) [9], och andra har visat att ca 40 procent av patienterna med stark misstanke om genetisk sjukdom fick en exakt genetisk diagnos [10]. Med helgenomsekvensering först skulle en diagnos också kunna ställas mycket snabbare jämfört med de metoder som innebär analys av en gen i taget. En klinisk helgenomanalys tar i dag ca 3 månader och en akut analys kan göras på några dygn [11]. En snabbare och förbättrad sjukdomsdiagnostik innebär även möjlighet till fosterdiagnostik och i allt högre utsträckning möjlighet till medicinsk behandling som kan anpassas till den aktuella sjukdomen, det vill säga precisionsmedicin.
Eftersom många sällsynta sjukdomar med en likartad och överlappande klinisk bild kan orsakas av olika gener har det tidigare ofta krävts analys av ett flertal gener innan en diagnos kan ställas. Sammantaget har helgenomsekvensering stor potential att innebära bättre, billigare och snabbare genetisk diagnostik för individer med en misstänkt genetiskt orsakad sällsynt diagnos.
Diagnostik och databearbetning
Analys med helgenomsekvensering kan göras på två principiellt olika sätt: antingen analyseras bara patientens genom eller så görs en så kallad trioanalys, som omfattar patientens samt båda föräldrarnas genom (Figur 1). I båda fallen behövs alltid en tydlig klinisk beskrivning av patientens symtombild inklusive eventuell dysmorfologi. Det är också viktigt att varje individ förstår omfattningen av utredningen och att det kan innebära att man identifierar andra genetiska sjukdomar än den man initialt utreds för, så kallade bifynd. Om forskningsanalyser planeras inhämtas alltid samtycke. Därefter tas oftast ett blodprov, men även andra vävnader kan vara aktuella. DNA extraheras ur provet och sekvenseras. Efter sekvenseringen analyseras patientens genomdata i flera steg med olika bioinformatiska program för att vaska fram tänkta sjukdomsframkallande genvarianter (Figur 2).
I klinisk diagnostik analyseras inte alla gener, utan data filtreras så att endast varianter i kända sjukdomsgener som matchar patientens kliniska symtom är synliga och genomgår bedömning. Sådana bioinformatiskt utformade in silico-genpaneler finns till exempel för metabola sjukdomar, immunologiska sjukdomar, skelettdysplasier och intellektuell funktionsnedsättning [12]. Särskilt när endast patientens genom analyseras måste analysen av tekniska skäl begränsas till en genlista, typiskt med maximalt några hundra gener. Vid trioanalys (då barnets/patientens genom jämförs med föräldrarnas) och mer komplex symtomatologi kan man filtrera mot samtliga kända sjukdomsassocierade gener. Patientens varianter jämförs sedan med kända normalvarianter som finns i stora databaser [13, 14], och slutligen sammanställs en lista med varianter som genomgår klinisk bedömning. Varianttolkning är ett tidskrävande steg där det bedöms om en genvariant verkligen kan förklara patientens sjukdomsbild. För punktmutationer delas sannolikheten för att genvarianten ska vara sjukdomsorsakande upp i 5 klasser enligt internationellt etablerade kriterier [15]. Varianter av klass 4 (sannolikt patogena) och 5 (patogena) kan i svaret anges som sjukdomsorsakande om patientens symtom stämmer överens med den sjukdom som man vet att mutationer i den aktuella genen orsakar. För systematisk fenotypbeskrivning används termer ur HPO (Human phenotype ontology) [16], och matchningen mellan klinisk bild (fenotyp) och genotyp kan även underlättas med hjälp av olika databaser såsom Clinvar [17], Matchmaker exchange [18], Orphanet [19] och OMIM (Online Mendelian inheritance in man) [5]. Om en mycket sällsynt variant eller en helt »ny« gen identifieras kan det ta lång tid, ibland flera år, att säkerställa associationen då det krävs att flera obesläktade individer uppvisar samma symtom och har varianter i samma gen. Ibland kan man också gå vidare med funktionella studier för att visa att varianter i den aktuella genen orsakar de symtom som uppvisas. Detta kan ofta göras med analys av patientceller, men ibland krävs det studier i olika djurmodeller, till exempel bananfluga, zebrafisk eller mus, där den genetiska förändring man vill undersöka skapas med traditionell mutagenes eller Crispr/Cas9-metodik.
För optimal analys av NGS-data krävs det kontinuerlig utveckling av bioinformatiska verktyg för dataanalys, annotering, standardisering, lagring och datadelning. Prediktionsverktyg behöver förbättras, till exempel för små förändringar såsom insertioner, deletioner och strukturella varianter. För att underlätta tolkning av data och öka andelen patienter som får en genetisk orsaksdiagnos behöver genetiska varianter som identifierats inom klinisk diagnostik rapporteras till databaser där man sparar kliniskt relevanta varianter (Clinvar) eller oklara varianter (Matchmaker exchange) [17, 18]. Man behöver även samla aggregerade frekvensdata i stora databaser som kan användas för att filtrera bort normalvarianter. Tillgängliga databaser (Swegen, gnomAD [genome aggregation database]) [13, 14] som samlar genetisk information från tusentals individer i normalbefolkningen innehåller oftast en övervikt av individer med europeiskt ursprung och information saknas från stora delar av världen, vilket försvårar analys av individer med annat ursprung. För att bygga bättre databaser krävs att data delas mellan regioner och länder.
Nationellt samarbete
Eftersom den svenska hälso- och sjukvården är decentraliserad till 21 regioner och regionalt finansierad medan universiteten är statligt finansierade finns det begränsningar i möjligheten att implementera nya fynd och teknologiska framsteg inom klinisk rutin. Det regionala styret av sjukvården har också försvårat jämlika möjligheter till diagnostik med NGS och inneburit problem med att dela genomdata. Många storskaliga sekvenseringsprojekt har påbörjats inom forskning, till exempel Swegen där 1 000 svenska individer helgenomsekvenserats [13], men full klinisk implementering av teknologin i hälso- och sjukvården har varit svårare att få på plats. För att stärka nationellt samarbete i Sverige initierades Genomic Medicine Sweden (GMS) med sällsynta diagnoser som ett prioriterat område. Målet för GMS-RD (Genomic Medicine Sweden Rare Diseases) har varit att möjliggöra NGS-sekvensering i hela landet på lika villkor för alla patienter i landet.
Implementering av helgenomsekvensering i Sverige
Ett tätt samarbete mellan Karolinska universitetslaboratoriet och Clinical Genomics-faciliteten inom Science for Life Laboratory (Scilifelab), Solna, har möjliggjort klinisk helgenomsekvensering i Stockholm sedan 2015. Detta arbete har bland annat inneburit att helgenomsekvensering nu erbjuds som första diagnostiska test vid intellektuell funktionsnedsättning hos nyfödda, barn och vuxna [9].
Sedan 2019 utförs helgenomsekvensering för misstänkta genetiska sällsynta sjukdomar i klinisk rutin vid GMC (Genomiskt medicincentrum) i tre sjukvårdsregioner: GMC Karolinska (Stockholms sjukvårdsregion), GMC Väst (Västra sjukvårdsregionen) och GMC Syd (Södra sjukvårdsregionen). Analysen är i uppstartsfas även vid andra GMC. Vid en kartläggning på uppdrag av GMS-RD i september 2020 framkom att det på nationell bas sammantaget utförts totalt 3 532 kliniska helgenomanalyser för sällsynta sjukdomar hos enstaka patienter, där hela genomet eller utvalda paneler analyserats. Av dessa har 1 187 patienter (34 procent) fått en molekylärgenetisk diagnos. Under samma tidsperiod har även 948 trioanalyser (ca 2 844 individer) utförts med en uppklarningsfrekvens på 36 procent (340 patienter).
Etiska överväganden
Helgenomanalys ställer flera etiska frågor på sin spets, särskilt då analyserna ibland medför att även friska anhöriga analyseras för jämförelse. Att många gener analyseras på en och samma gång innebär inte bara större chans att patienten får en orsaksdiagnos utan också en risk för att data tolkas fel, vilket i värsta fall leder till ett felaktigt svar. Dessutom finns möjligheten att bifynd (kallas även sekundära fynd) görs, det vill säga varianter i andra gener som inte har med sjukdomen att göra, men som kan påvisa till exempel risk för en annan sjukdom. Om det finns förebyggande åtgärder eller andra medicinska skäl att informera om varianterna rapporteras sådana bifynd. Detta ställer stora krav på att korrekt information ges innan analysen beställs. Genetiska varianter av oklar signifikans som kan vara relevanta men inte är fastställda som orsak till sjukdom är mycket svåra att rapportera på ett bra sätt och övertolkas ofta inom vården.
Det finns även risker kopplade till informationshantering och integritet då genetisk information lagras i databaser. Mot denna risk måste också ställas det motsatta etiska argumentet, att lagring av individers genetiska information är till stor hjälp för framtida diagnostik och därför kan gynna både patienten direkt och i förlängningen alla patienter.
Utmaningar
En utmaning är mängden genvarianter som påvisas vid varje analys, eftersom varje helgenom genererar miljontals varianter. Att tolka och handskas med denna datamängd kräver komplexa multidisciplinära arbetsflöden. Samarbete mellan kliniska genetiker, andra specialister inom klinisk medicin och laboratoriemedicin, bioinformatiker och molekylärbiologer/sjukhusgenetiker är en nyckelfaktor för diagnostiken. En noggrann fenotypisk bild av patienten är nödvändig för att koppla genetiska fynd till sjukdomsbild, och utan denna koppling finns stor risk för feldiagnostik. Genetisk variantbedömning kräver erfarenhet och kunskap såväl molekylärt som medicinskt. Inga algoritmer finns i dag som automatiskt kan klassificera alla varianter. Kompletterande biokemiska eller immunologiska analyser är till stor hjälp inom vissa sjukdomsområden. I andra fall kräver funktionella analyser nära koppling till en intresserad forskare, vilket nödvändiggör att sjukvård och akademi arbetar nära varandra. När nya behandlingar kommer ut på marknaden är det också nödvändigt att få ett system på plats för att hitta de få individer i landet som kan ha nytta av terapin, det vill säga ett register som omfattar genetiska data alternativt de individer som har en genetiskt bekräftad diagnos. Inom GMS arbetar vi för att etablera en nationell genomikplattform som skulle möjliggöra sådan datadelning, men ett otydligt regelverk gör att arbetet går långsammare än vi hade önskat.
Vård och behandling av personer med sällsynta tillstånd involverar många olika specialister och stödinsatser från samhället. Olika expertteam är nödvändiga för att koordinera och samla kompetens. I dagens fragmenterade sjukvård kan detta vara svårt, och för att stödja befintliga och befrämja bildandet av nya expertteam finns CSD (Centrum för sällsynta diagnoser) på sex av landets universitetssjukhus. Den nationella kunskapsstyrningen med nationella programområden (NPO) har också ett stort uppdrag att verka för förbättrat omhändertagande och inrättande av kvalitetsregister, som saknas för flertalet av dessa diagnoser. Sverige är också involverat i flera viktiga internationella samarbeten, till exempel flera olika europeiska referensnätverk (European Reference Networks, ERN) och UDNI (Undiagnosed Diseases Network International).
De individer som inte får en genetisk orsaksdiagnos är fortfarande många, men nya tekniker är under utveckling, vilket gör att vi kan blicka optimistiskt in i framtiden. För att uppnå snabb klinisk implementering krävs utöver resurser för kliniska analyser även resurser för forskning med ett starkt samarbete mellan hälso- och sjukvård, universitet, tekniska högskolor och andra intressenter såsom läkemedelsindustrin. Flera nya särläkemedel (läkemedel för sällsynta diagnoser) är på väg, men för att kunna nå hela vägen fram till individbaserad vård krävs oftast en genetisk diagnos. En viktig drivande faktor är att involvera individerna med sällsynta tillstånd själva och deras anhöriga. Den kunskap som patienter och patientföreningar har är enormt viktig för att föra utvecklingen vidare, och former för detta behöver arbetas fram.
Läs även:
Författarintervju med Maria Johansson Soller
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Fallbeskrivning
Fallet rör en 5-årig flicka som är första barnet till friska, icke-besläktade föräldrar. Det finns inga andra individer i familjen med liknande symtom. Förlossningen igångsattes efter en normal graviditet i vecka 38 + 1 på grund av minskade fosterrörelser och tillväxthämning. Vid födelsen var vikten 2 260 g (–4 SD), längden 43 cm (–4 SD) och huvudomfånget 30 cm (–5 SD). I nyföddhetsperioden noterades bilateral kongenital höftluxation, infällda tummar och svårigheter att suga. På grund av utebliven utveckling, avvikande neurologi och tilltagande mikrocefali utfördes upprepade EEG- och MR-undersökningar. Dessa visade multifokal epileptisk aktivitet med låg bakgrundsaktivitet samt en progressiv bild med uttalad mikrocefali och underutveckling av hjärnan med tunn corpus callosum, vitsubstansförlust och avvikande hjärnvindlingar. Genetisk utredning med gendos-array och trioanalys med exomsekvensering utfördes under det första levnadsåret utan att någon orsak kunde påvisas. Vid förnyad kontakt med mottagning för klinisk genetik vid 4,5 års ålder uppvisade flickan en grav intellektuell funktionsnedsättning med avsaknad av kommunikativ förmåga, epilepsi med frekventa myoklona ryckningar och spastisk kvadriplegi utan frivilliga rörelser. Hon matades enbart via gastrostomi och var funktionellt blind, men reagerade på ljud och kunde lätt bli skrämd. Hon hade även skolios. Längden var –3,5 SD, vikten –2 SD och huvudomfånget –10 SD. En utvidgad genetisk utredning med helgenomsekvensering inklusive strukturell analys utfördes som visade att patienten bar på två olika varianter i PHGDH-genen, vilket innebär att hon har diagnosen fosfoglyceratdehydrogenasbrist – en defekt i serinsyntesen.
De påvisade två varianterna är nedärvda från vardera föräldern, och en av varianterna är en strukturell avvikelse som bland annat resulterar i deletion av ett exon som inte varit möjlig att upptäcka med de tidigare utförda analyserna. Efter diagnos och verifiering av sänkta nivåer av serin och glycin i plasma och likvor påbörjades behandling med serin 200 mg/kg per dygn med förhoppning om att detta skulle förbättra flickans symtom. Tyvärr reagerade hon med panikartade oupphörliga skrik och accentuerade sömnsvårigheter, varför behandlingen tillfälligt behövde utsättas men kommer att tas upp igen. Föräldrarna har erhållit genetisk vägledning och information om diagnosen och att det föreligger 25 procents upprepningsrisk. Fosterdiagnostik inklusive preimplantatorisk genetisk testning kan erbjudas vid en eventuell kommande graviditet.
Fakta 2. Faktorer som försvårar möjligheterna/tillgången till genetisk diagnos
Kliniska faktorer
- Ospecifika symtom
- Sällsynthet och icke identifierat syndrom
- Uppdelat omhändertagande i vården utan helhetssyn
- Symtombild som ändras med ålder
Tekniska faktorer
- Tekniska problem vid genomsekvensering
- Icke standardiserade metoder
- Icke fullständiga databaser
Datadelning
- Data delas inte
- Datadelningsstandard saknas
- Integritetsfrågor
- Lagstiftning
- Fragmentering av data
Funktionella bevis för varianteffekt saknas
- Finns inte inom sjukvårdsrutin, kräver forskningssamarbete
- Saknas bra funktionella analysmetoder
- Genens funktion inte känd
Ofullständigt kartlagda sjukdomsmekanismer
- Icke kodande delars funktion okänd
- Mosaikism, metylering, oligogen nedärvning med mera