Komplexa sjukdomar utgörs av vanliga folksjukdomar där arv, miljö och livsstil påverkar sjukdomsrisken.
Kunskap om genetik och underliggande mekanismer utgör en bas för precisionsmedicin, utöver anamnes och status.
Precisionsmedicin inkluderar även användning av olika omikdata för att studera genaktivering (transkriptomik), kemisk modifiering av DNA (epigenetik) och proteinuttryck (proteomik).
Relativt få precisionsmedicinska tillämpningar sker i vården avseende patienter med komplexa sjukdomar i dag.
Stor potential finns för utökad användning av precisionsmedicin, framför allt vid diagnostik och terapival.
En gemensam nationell satsning behövs för att ytterligare utveckla och implementera precisionsmedicin kliniskt.
Komplexa sjukdomar utgörs till stor del av våra vanliga folksjukdomar, som har gemensamt att ärftlighet, miljöfaktorer och livsstil både påverkar risken att insjukna och svårighetsgrad hos de drabbade. Kunskap om genetik och underliggande sjukdomsmekanismer utgör en bas för precisionsmedicin. De enorma framsteg som gjorts inom genomikområdet de senaste åren har möjliggjort analyser av DNA, RNA, proteiner och metaboliter i förhållande till olika sjukdomar, inklusive de komplexa sjukdomarna. Tillgång till omikdata, tillsammans med anamnes och kliniska undersökningar, har således öppnat för helt nya möjligheter [1].
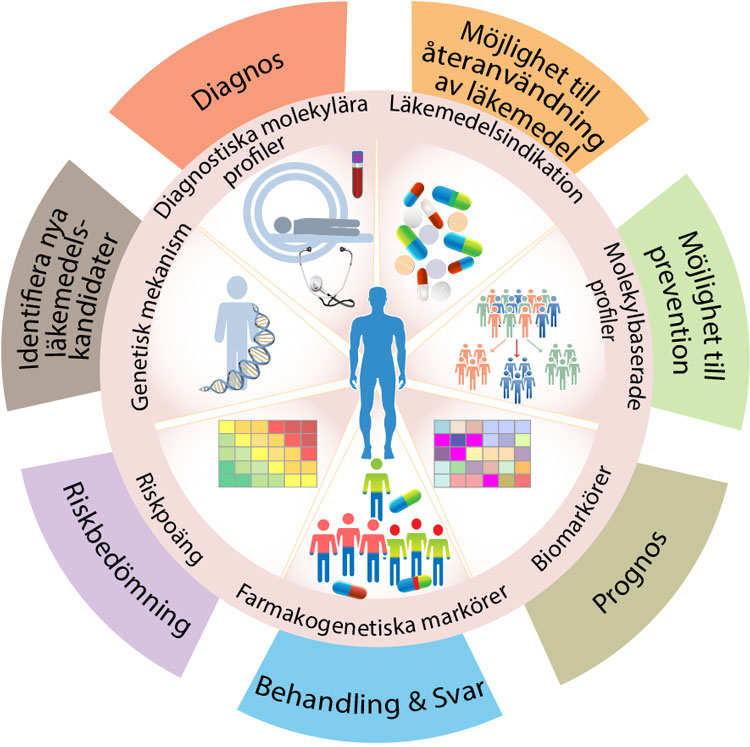
Vi kommer i denna artikel att belysa och exemplifiera tillämpning av precisionsmedicin vid olika komplexa sjukdomar och tillstånd och diskutera vilken nytta precisionsmedicin kan förväntas ge de närmaste åren (Figur 1). Allergisjukdom, hjärt–kärlsjukdom, diabetes och stroke tillhör i dag de allra vanligaste folksjukdomarna i Sverige. Även om vi saknar en komplett förståelse av hur dessa sjukdomar utvecklas har stora framsteg gjorts när det gäller att öka kunskapen om underliggande genetiska faktorer och hur genetik och livsstil samverkar vid sjukdomsutveckling. Precisionsmedicin inkluderar användning av flera olika omikanalyser, vilket möjliggör nya diagnostiska hjälpmedel som kan vägleda specifik behandling. Som exempel tas biologiska läkemedel upp, vilka har revolutionerat vården av patienter med kroniska inflammationssjukdomar, som IBD (inflammatoriska tarmsjukdomar) eller reumatoid artrit. För rätt patient är dessa läkemedel ofta mycket effektiva med specifika verkningsmekanismer. De är dock förenade med höga direkta läkemedelskostnader och kräver ofta ett avancerat behandlingsupplägg. Därför behövs kliniskt pålitliga test och biomarkörer för att välja rätt medicin till rätt patient vid rätt tidpunkt, och för att kunna följa behandlingsresultaten på individnivå.
Allergi – möjligheter till individanpassad behandling
Allergiska sjukdomar är en heterogen grupp som bland annat innefattar astma, eksem och allergisk rinit. Dessa sjukdomar drabbar en stor del av befolkningen – uppemot var fjärde svensk rapporterar någon form av allergi. Var och en av dessa sjukdomar kan undergrupperas genom sina kliniska manifestationer, utlösande faktorer och underliggande molekylära mekanismer. Sådana undergrupperingar illustrerar både möjligheter och svårigheter med individanpassad behandling. En stor fördel vid IgE-medierad allergisk inflammation är att utlösande omgivningsfaktorer, exempelvis pollen vid hösnuva, ofta kan identifieras och valideras med laboratorieprov. En annan fördel är att underliggande cellulära och molekylära mekanismer är väl definierade: allergenet tas upp av antigenpresenterande celler som presenterar det för T-celler. Hos allergiska individer resulterar det i att T-celler differentieras till T-hjälparceller typ 2 (Th2), som frisätter cytokiner med välkända effekter. IL-4 aktiverar exempelvis IgE-produktion och IL-5 eosinofila celler. Upptäckterna av dessa mekanismer har lett till precisionsmediciner riktade mot exempelvis IgE, IL-4 och IL-5 eller deras receptorer. Användandet av sådana mediciner styrs av klinisk bild samt laboratorieprov som speglar de underliggande mekanismerna och deras styrka. Exempelvis är anti-IgE-behandling indicerad vid svår astma med förhöjt värde av IgE. Doseringen styrs av IgE-nivåer i perifert blod [2]. Detta exempel, liksom mediciner riktade mot Th2-cytokiner, anses ha stor klinisk potential [3].
Trots de väldefinierade mekanismerna och diagnostiken varierar dock terapisvaret hos patienterna utan att man säkert kan förklara orsakerna. Detta gäller också medicinering riktad mot Th2-cytokiner, och även i samband med allergen immunterapi. Orsakerna har varit föremål för omfattande diskussioner [3]. En viktig förklaring kan vara att de ovan beskrivna cellulära och molekylära mekanismerna är förenklade. Enbart helgenomanalyser av mRNA-uttryck i allergenstimulerade T-celler från patienter med hösnuva visar att tusentals gener ändrar uttryck jämfört med friska kontroller [4]. Analyser av vilka signalvägar dessa representerar tyder på inblandning av ett stort antal mekanismer som inte säkert är kopplade till Th2-differentiering. Dessutom varierar dessa mekanismer vid olika tidpunkter i den allergiska inflammationen [4]. En rimlig förklaring till varierande terapisvar är alltså heterogena mekanismer på grund av individuella eller tidsberoende skillnader mellan olika patienter med samma diagnos. En annan viktig förklaring är att många patienter med symtom på astma, eksem eller rinit inte har påvisbar IgE-medierad allergi. Omfattande forskning pågår för att nå en mer detaljerad cellulär och molekylär förståelse av behandlingsbara mekanismer hos patienter med olika former av allergiska eller allergilika sjukdomsbilder [3].
Kardiovaskulär sjukdom och stroke – genetiska studier
Under de senaste 15 åren har stora internationella genomtäckande associationsstudier (GWAS) identifierat över 60 000 genetiska variationer associerade med tusentals sjukdomar och egenskaper (Figur 2) [5, 6]. I dag vet man att genetisk predisposition för komplexa sjukdomar oftast utgörs av ett stort antal genvarianter som var för sig har en liten effekt, men som sammantagna förklarar en stor del av ärftligheten. Till exempel förklarar de genetiska varianter för typ 2-diabetes som hittills identifierats ungefär hälften av den ärftlighet man kommit fram till i tvilling- och familjestudier [7]. När det gäller genvarianter vid koronarsjukdom och vaskulära riskfaktorer har kunskapen ökat explosionsartat de senaste åren [5, 8].
Trots att stroke är en mycket vanlig sjukdom (1 av 4 drabbas av stroke någon gång under sin livstid), har genetiska studier av stroke inte varit lika omfattande som av koronarsjukdom. Nyligen har dock större genomtäckande studier även av stroke utförts [9]. Många av de lokus som identifierats är specifika för ischemisk eller hemorragisk stroke respektive för någon av subtyperna av ischemisk stroke: kardiell emboli, storkärls- eller småkärlssjukdom [9]. I ca 1 av 4 fall av ischemisk stroke förblir orsaken okänd, så kallad kryptogen stroke. Förhoppningen är att de genetiska studierna i kombination med andra omikstudier kommer att bidra med ökad kunskap om underliggande mekanismer i denna gåtfulla grupp. Detta skulle möjliggöra mer precisionsinriktad sekundärprevention i syfte att reducera återkommande stroke och andra vaskulära händelser.
Ett annat långsiktigt mål är att kunna använda den genetiska informationen för mer precisionsinriktad primärprevention. Utifrån de genomtäckande studierna av både kardiovaskulär sjukdom och vaskulära riskfaktorer kan man skapa så kallade genetiska riskpoäng (polygenic risk score, PRS), med syfte att skatta genetisk risk på individnivå. Med hjälp av genetiska riskpoäng för koronarsjukdom och ischemisk stroke har man kunnat visa att den del av befolkningen som har högst genetisk riskpoäng har lika hög risk för framtida koronarsjukdom respektive
stroke som individer med monogen hyperkolesterolemi [8, 10]. Då betydligt fler personer har hög genetisk riskpoäng än monogen hyperkolesterolemi finns stor potential att med hjälp av genetiska riskpoäng identifiera en större andel av befolkningen som har hög risk för vaskulära händelser. Dessa studier visar också att genetiska riskpoäng inte är korrelerat till traditionella vaskulära riskfaktorer, och således bidrar med prediktiv förmåga utöver dessa. Vidare talar simuleringar för att nuvarande riktlinjer för primärprevention av kardiovaskulär sjukdom och stroke är otillräckliga för de individer som har allra högst genetisk riskpoäng. En potentiell fördel med genetisk testning är att individer med påtagligt ökad kardiovaskulär risk kan identifieras innan de utvecklat kliniska riskfaktorer såsom hypertoni. Ytterligare kunskap, och inte minst resultat från interventionsstudier, krävs dock innan användning av genetiska riskpoäng kan implementeras kliniskt.
Hittills har de genetiska studierna fokuserat på sjukdomsrisk. Det finns nu studier som talar för att genetiska faktorer även kan ha betydelse för utfall efter ischemisk stroke [11]. Ett problem inom strokefältet är att en lång rad substanser som i djurexperimentella studier funnits gynna återhämtning efter stroke inte har haft någon effekt hos människa. Vad gäller läkemedelsutveckling visar nya rön att substanser vars måltavlor har humant genetiskt stöd har större chans att ha effekt än substanser utan genetiskt stöd [12]. Genomtäckande studier av utfall efter stroke och andra komplexa sjukdomar har således potential att ge vägledning till framtida läkemedelsutveckling. Ett annat långsiktigt mål är att genetisk information tillsammans med annan omik samt förfinade radiologiska och andra kliniska utredningar ska bidra till utvecklingen av precisionsmedicin vid komplexa sjukdomar i syfte att optimera återhämtning och utfall.
Ärftliga faktorer – samspel med kost och livsstil
Frågan om det finns samspel mellan genetisk risk och livsstil av betydelse för typ 2-diabetes och andra kardiometabola sjukdomar har ställts i många studier. Studierna tyder på att livsstil, till exempel intag av kostfetter, medelhavskost och fysisk aktivitet, är associerad med typ 2-diabetes oberoende av den genetiska risken [13]. Liknande resultat har observerats i samspelsstudier för kranskärlssjukdom: i en svensk-amerikansk studie där hälsosam livsstil klassificerades baserat på ett poängsystem bestående av fyra faktorer från de strategiska målen för American Heart Association (icke-rökare, BMI < 30 kg/m2, regelbunden fysisk aktivitet och hälsosam kost) var hälsosam livsstil associerad med en väsentligt minskad risk för kranskärlssjukdom inom varje kategori av genetisk risk [14]. Studier avseende riskfaktorers samspel vid fetma har gett mera övertygande bevis för genetik–livsstilsinteraktioner, då riskökningen på grund av fysisk inaktivitet, högt intag av stekt mat eller sockersötade drycker och låg socioekonomisk status verkar vara särskilt stor för individer med hög genetisk risk för fetma [13].
Vår livsstil spelar stor roll för risken att utveckla fetma, typ 2-diabetes, hjärt–kärlsjukdom och stroke. Emellertid råder en stor osäkerhet kring hur de mest effektiva individanpassade preventionsåtgärderna skulle se ut samt hur man bäst kan ge råd om livsstilsförändringar. Flera studier tyder på att »en åtgärd passar alla«-strategin inte är effektiv. Exempelvis har en hög interindividuell variation i postprandialt glukossvar påvisats i en uppmärksammad stor studie där glukosnivån mättes kontinuerligt under en vecka hos 800 deltagare [15]. Baserat på dessa resultat utformade forskarna en maskininlärningsalgoritm som integrerade information från blodvariabler, antropometri, kostvanor, fysisk aktivitet och tarmflora. Resultaten visade att denna algoritm kunde förutspå individuella glykemiska svar efter måltider. Studien innefattade också en randomiserad kontrollerad dietintervention baserad på denna algoritm, vilket gav signifikant lägre glykemiska svar efter måltider [15]. Resultatet tyder på att individanpassade kostrekommendationer kan ha större nytta än universella och att maskinlärningsbaserade metoder kommer att spela en viktig roll i framtida individanpassade precisionsmedicinska koncept.
Biologiska läkemedel – välja rätt medicin till rätt patient
Introduktionen av biologiska läkemedel har revolutionerat såväl behandlingsalgoritmer som livskvaliteten för många patienter med kroniska inflammationssjukdomar. Ett betydande antal preparat finns i dag på marknaden och fler förväntas bli godkända inom de kommande åren. Behovet av att kunna förutspå en enskild patients framtida sjukdomsförlopp och svar på olika läkemedel blir allt viktigare i takt med att behandlingsalternativen ökar. I brist på prognostiska och prediktiva markörer riskerar behandlingsbeslut att baseras på läkemedelskostnader och behandlande läkares personliga erfarenheter.
Hand i hand med utvecklingen av biologiska läkemedel har vår molekylära kunskap kring sjukdomar som reumatoid artrit, MS, astma (se ovan) och IBD vuxit och flera behandlingsstrategistudier har initierats för att värdera nyttan av olika biomarkörer och molekylära signaturer. I likhet med resultat avseende systemisk lupus erythematosus (SLE) påvisades redan 2011 att patienter med IBD kan klassificeras i två grupper med helt olika sjukdomsförlopp utifrån CD8-positiva T-cellers expressionsprofil [16]. Uppföljande arbete ledde till utvecklandet av det CE-certifierade prognostiska testet Predictsure IBD [17]. Värdet av att stratifiera IBD-patienter utifrån testet studeras i den pågående PROFILE-studien, samtidigt som det redan saluförs i delar av Europa. Likväl har data avseende prognostiskt värde av proteinprofiler i serum för IBD nyligen publicerats, och dess potentiella roll kommer att värderas i NORDTREAT – en nordisk studie [18].
Behovet av prediktiva test avseende enskilda biologiska läkemedel är stort. Med hjälp av gensekvensering visades att bärare av HLA-DQA1 har en dubblerad risk att utveckla antikroppar mot infliximab och adalimumab [19]. Resultaten har replikerats i retrospektiva kohorter och i dag finns det kollegor som beställer testet inför insättande av biologisk läkemedelsbehandling. Därtill pågår studier i syfte att värdera det prediktiva värdet av exempelvis expressionsprofiler i vävnad, in vitro-stimulering av immunceller och mikrobiomet i tarmen, varav exempelvis 3TR är diagnosöverskridande och utförs inom EU:s IMI 2-program [20].
Sammanfattning
Utifrån forskningsnivå och klinisk kompetens avseende komplexa sjukdomar har vi i Sverige mycket goda förutsättningar att driva och fortsätta utveckla precisionsmedicin. Vi har i denna artikel belyst några vanliga komplexa sjukdomar där precisionsmedicinska verktyg har stor potential att förbättra den kliniska förståelsen och handläggandet. Även om kunskap och kliniskt behov finns så behöver vi kraftsamla resurser och infrastruktur för att kunna omsätta teori och modeller i kliniken. Här behöver företrädare för de komplexa sjukdomsgrupperna samarbeta och samordna utbildningsinsatser med övriga intressenter inom svensk sjukvård där genetik och genomik används (för övergripande satsningar nationellt, se separat artikel om Genomic Medicine Sweden i detta tema).
Exempelvis har modellen med beräkning av genetisk riskpoäng visats kunna påvisa klart förhöjd sjukdomsrisk på individnivå. Den kliniska användningen vid komplexa sjukdomar behöver dock studeras ytterligare, särskilt i kombination med traditionella riskfaktorer som rökning eller kost och utifrån kostnadseffektivitet. Individer med hög genetisk riskpoäng behöver kanske ha andra terapimål avseende exempelvis blodtryck, kolesterolnivåer eller blodsocker än personer med »normal« genetisk riskpoäng. Det finns i dag få exempel där dessa poäng används för diagnostik eller terapival. Användningen av genetiska riskpoäng har däremot kommit längre inom cancervården, framför allt vad gäller prostatacancer och bröstcancer.
När det gäller behandling så finns i dag exempel på test som möjliggör en mer individanpassad vård för patienter med komplexa sjukdomar, exempelvis vissa inflammationssjukdomar. Fler är under utveckling, men mycket återstår innan precisionsmedicin ligger till grund för uppföljningsprogram och terapival för våra stora folksjukdomar. Implementering av precisionsmedicin i kliniken och betydelsen vid terapival (farmakogenomik) diskuteras mer utförligt i särskilda artiklar i detta tema.
Inom Genomic Medicine Sweden startades under hösten 2019 en nationell arbetsgrupp för komplexa sjukdomar. Målet är att identifiera ett antal vanliga komplexa sjukdomar där man identifierat genetiska kopplingar och implementerat kunskapen på olika sätt i den kliniska verksamheten. Arbetet med att ta fram en nationell strategi för hur precisionsmedicin vidare kan implementeras kliniskt har också påbörjats.
Potentiella bindningar eller jävsförhållanden: Erik Melén har erhållit ersättning från Chiesi, Astra Zeneca, Novartis och Sanofi för deltagande i rådgivande kommitté och har anslag från ERA Permed. Bo Jacobsson har utfört kliniska diagnostiska prövningar för Ariosa, Natera, Vanadis och Hologic och kliniska probiotikastudier i samarbete med Biogaia och Fukopharma, varit medforskare i IMPACT-studien där Roche samt Thermo Fisher betalat analyser, medverkat i studie där Diagen tillhandahållit reagenser och analysutrustning samt arrangerat vetenskapliga möten med kommersiella partner. Jonas Halvarson har varit föreläsare eller rådsgruppsledamot för Abbvie, Aquilion, Celgene, Celltrion, Dr Falk Pharma och Falk foundation, Ferring, Gilead, Hospira, Index Pharma, Janssen, MEDA, Medivir, MSD, Olink Proteomics, Novartis, Pfizer, Prometheus Laboratories, Sandoz, Shire, Takeda, Thermo Fisher Scientific, Tillotts Pharma, Vifor Pharma och UCB och erhållit forskningsanslag från Janssen, MSD och Takeda. Mikael Benson har anslag från Vinnova, Cancerfonden, Cocozzastiftelsen och EU.
Samtliga författare ingår i arbetsgruppen för komplexa sjukdomar, Genomic Medicine Sweden.