Standardiserade spermieparametrar ger endast begränsad information om graviditetschansen. Kvantifiering av spermiernas DNA-strängbrott är prediktiv för fertilitet och kan adderas till underlaget inför valet av behandling.
Möjligheter till förbättring av sädeskvaliteten genom farmakologiska, kirurgiska eller livsstilsrelaterade interventioner är än så länge begränsade. Nya, effektiva terapier bör utvecklas.
Nedsatt spermiekvalitet är kopplad till testosteronbrist och kortare förväntad livslängd.
Andrologisk undersökning bör vara en naturlig del av infertilitetsutredningen och förutom spermaanalys inkludera en grundlig klinisk, endokrinologisk och i vissa fall genetisk undersökning.
Definition. Hos ca 80 procent av infertila par hittar man vid utredning någon form av patologi hos ena eller bägge parterna, men i 15–20 procent av fallen visar standardundersökningar inget onormalt hos någon av dem. Det betyder inte att normal sädeskvalitet är en garanti för normal fertilitet, och män med nedsatt sädeskvalitet kan också åstadkomma en spontan graviditet. Chansen för konception minskar dock om spermiekoncentrationen är lägre än 40 × 106/ml [1].
Epidemiologi
Om 15–20 procent av alla par är ofrivilligt barnlösa [2] och den manliga faktorn bidrar med ca 50 procent så har ca 8–10 procent av alla män nedsatt fertilitet [2]. Huruvida en tidsrelaterad nedåtgående trend i manlig fertilitet eller geografiska skillnader i sädeskvalitet existerar är omdebatterat. En del epidemiologiska studier har indikerat en kraftig reduktion i spermiekoncentrationen under de senaste 50–60 åren, mest uttalat i Europa och i USA [3]. Dessa studier har dock fått kritik gällande de metodologiska aspekterna. Vad som däremot är entydigt är att testikelcancerincidensen ökar, och eftersom det finns en koppling mellan testikelcancer och nedsatt fertilitet kan man inte utesluta att också antalet män med fertilitetsproblem verkligen ökar.
Orsaker
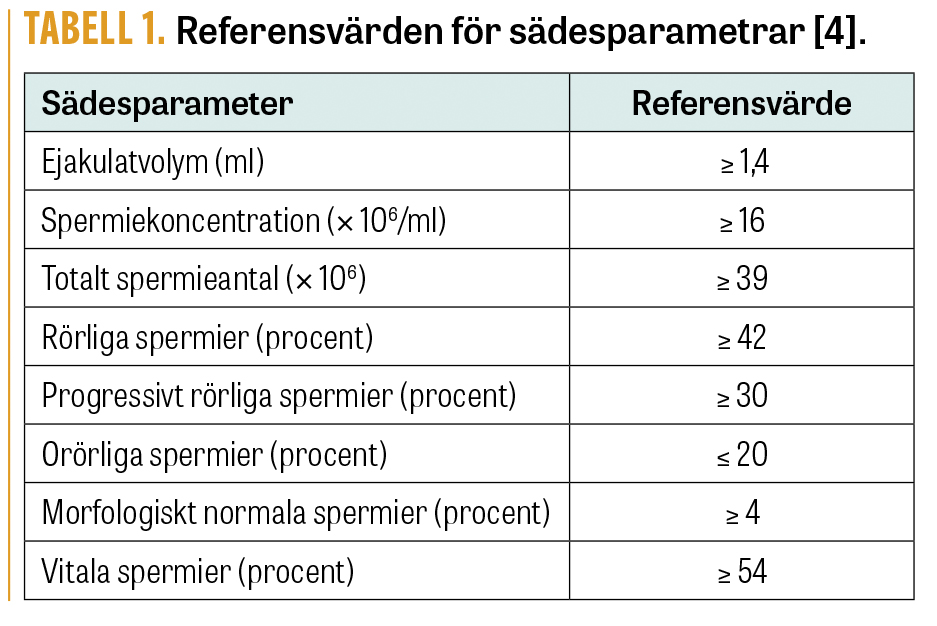
Diagnosen manlig infertilitet baseras uteslutande på en spermaanalys. Hur man bedömer sädeskvalitet, och vilka kriterier som används för att rubricera fertiliteten som nedsatt, beskrivs i detalj i Världshälsoorganisationens manual för detta ändamål [4]. För de viktigaste referensvärdena, se Tabell 1. Dysfunktionen som leder till en försämrad sädeskvalitet kan ligga på en eller flera av följande nivåer:
a) Hypotalamus/hypofys (5 procent)
b) Testes (80 procent)
c) Posttestikulärt (epididymis, vas deferens, vesiculae seminales, prostata eller uretra) (15 procent)
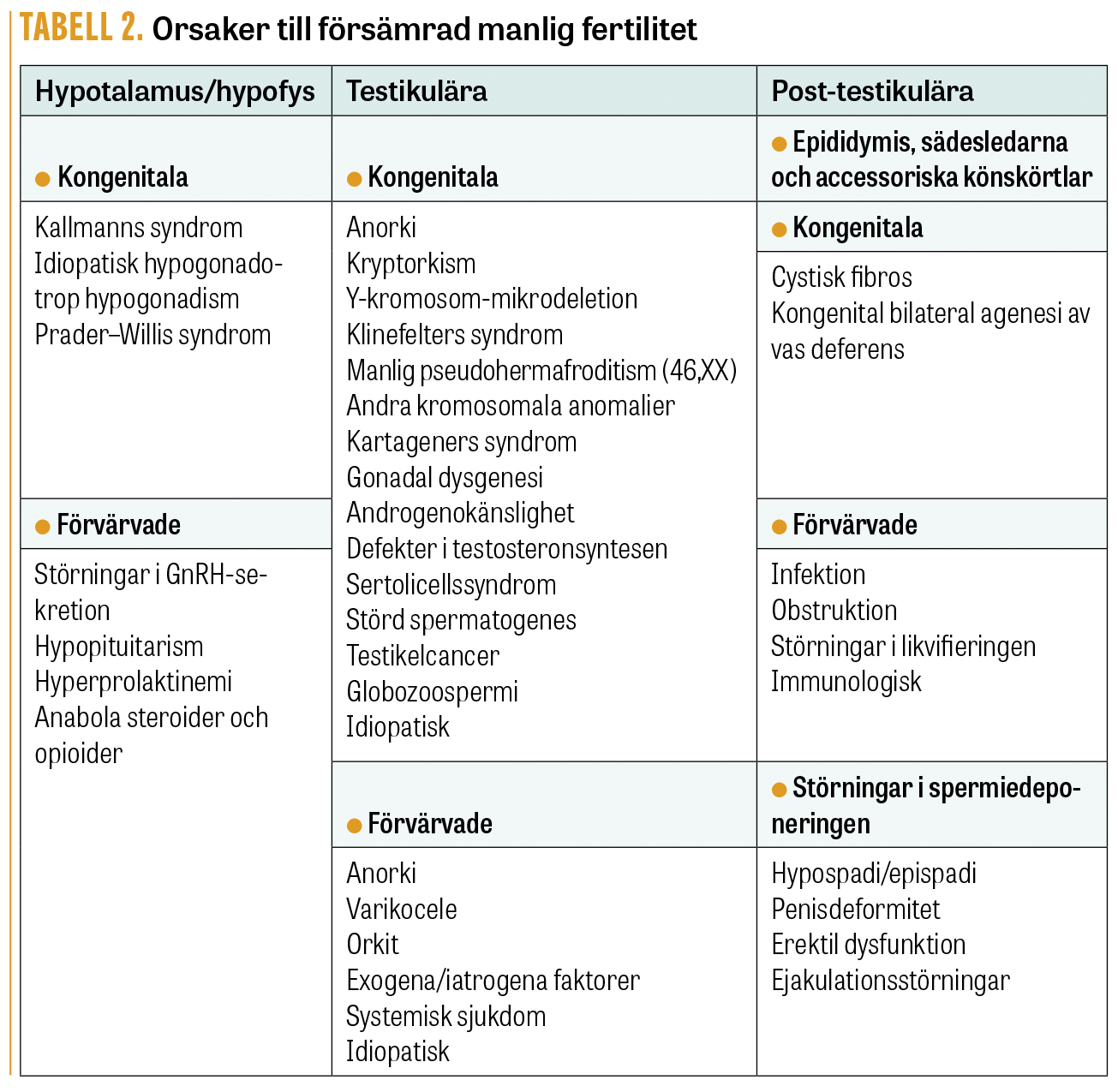
I Tabell 2 är orsaker till funktionsstörningar på dessa tre nivåer specificerade. Primär testisdefekt anses vara den främsta orsaken till försämrad sädeskvalitet. Etiologin är okänd i minst 40–50 procent av fallen, men livsstils- eller miljörelaterad maternell exponering tidigt under graviditeten har föreslagits spela en roll för sönernas fertilitet som vuxna män [5]. Vissa studier indikerar att även prekonceptionell exponering av båda föräldrarna kan spela en roll [6].
Överlevare av en malign sjukdom i barndomen eller i det tidiga vuxenlivet är en växande grupp patienter med infertilitetsproblem, men även andra patologiska tillstånd som till exempel fetma och olika systemiska sjukdomar kan ha en negativ effekt på testikelfunktionen och på hypotalamus-/hypofysnivån. Liknande gäller för en åldersrelaterad försämring av fertiliteten. Både hög ålder och allmän sjuklighet hos pappan kan också påverka graviditetsutfall negativt, till exempel mammans risk för preeklampsi och barnets perinatala karakteristika och mortalitetsrisk under tidig barndom [7].
Diagnos
Anamnes. Traditionellt utförs infertilitetsutredningar av gynekologer, och den manliga partnern kommer ofta i skymundan; i enstaka fall remitteras dessa män till en androlog. Helst bör dock både den kvinnliga och den manliga partnern undersökas vid ett och samma tillfälle av en läkare med både gynekologisk och andrologisk expertis, alternativt av en gynekolog respektive en androlog. Detta tillvägagångssätt har fördelen att man med all information samlad snabbt kan fatta beslut gällande behandling eller behov av ytterligare utredning tillsammans med de berörda och att det blir lättare att förmedla information om livsstilsrelaterade faktorer eller om den sexuella aktiviteten och eventuella förändringar som kan behöva göras. Förfarandet har också en positiv psykologisk effekt då den manliga partnern känner sig lika mycket delaktig som den kvinnliga och eventuella skuldkänslor som kan finnas vid fynd av onormala reproduktionsparametrar hos den ena av dem kan dämpas.
Förutom den information som är gemensam för paret bör den manliga partnern specifikt frågas om följande:
- tidigare barn eller graviditeter med den aktuella eller andra partner
- släktskap (ökad risk för genetisk störning)
- kryptorkism och andra sjukdomar eller operationer i urogenitalregionen
- puberteten – ålder, förlopp
- tidigare eller aktuella allvarliga eller kroniska sjukdomar samt eventuell medicinering
- livsstilsfaktorer som tobak, alkohol, anabola steroider, droger
- sexuell funktion (erektion, libido, ejakulation).
Fysisk undersökning. Den fysiska undersökningen bör förutom reproduktionssystemet också omfatta allmänt hälsostatus, först och främst antropometriska parametrar såsom längd, vikt, midjemått och blodtryck, då det finns ett samband mellan försämrad manlig fertilitet och övervikt och metabolt syndrom. Förbättring av fertiliteten har observerats efter behandling av komorbiditeter [8].
Bedömning av kroppsproportioner och gynekomasti samt inspektion, palpation och ultraljudsskanning av manliga genitalier bör också ingå som klinisk rutin vid andrologiska undersökningar.
Spermaanalys. På grund av den stora intraindividuella variationen i sädeskvaliteten bör bedömningen att orsaken till infertiliteten helt eller delvis finns hos mannen baseras på minst två spermaprov. Endast resultat från laboratorier som följer Världshälsoorganisationens manual samt deltar i extern kvalitetskontroll kan anses pålitliga. Standardparameterna är volym, koncentration/antal, rörlighet, morfologi och vitalitet. Avvikelse i en eller fler av dessa är indikativ för påverkan av den manliga reproduktionsfunktionen, men kan i de flesta fall inte bidra med information om etiologin eller patogenesen bakom störningen.
Ejakulatvolym <1 ml i kombination med pH ≤ 7 indikerar agenesi av vas deferens och/eller av vesiculae seminales. Mycket låg volym ses även i samband med retrograd ejakulation. Kombinationen normal vitalitet och inga eller några få procent rörliga spermier ses i samband med Kartageners syndrom, medan globozoospermi, som beror på en akrosomdefekt, karakteriseras av att majoriteten av spermierna har runda huvuden.
Spermieparametrars användbarhet i prediktivt syfte vid assisterad befruktning är dessvärre begränsad. Även om spermaanalysen är hörnstenen i den andrologiska undersökningen kan den behöva kompletteras med till exempel en analys av andelen spermier med intakt kromatin. Studier har visat att en hög andel spermier med DNA-fragmentering indikerar lägre graviditetschans både vid naturlig befruktning och i samband med standard-in vitro-fertilisering (IVF). Om däremot intracytoplasmatisk spermieinjektion (ICSI) tillämpas påverkar DNA-fragmentering varken chansen för graviditet eller för att få ett barn [9]. 25 procent av män i oförklarligt infertila par har normala standardspermieparametrar, men hög andel spermier med DNA-fragmentering. Även om randomiserade studier saknas, finns det indirekt evidens för att man genom att mäta DNA-fragmenteringen hos dessa män kan optimera behandlingen genom att undvika intrauterin insemination (IUI) och eventuellt även standard-IVF [10, 11].
Hormonanalyser. Män i infertila par som har försämrad sädeskvalitet har ökad risk för testosteronbrist, och bör därför erbjudas endokrinologisk utredning, som bidrar till att hitta orsaken till eventuell fertilitetsstörning och till att identifiera män med ökad risk för långtidsföljder av infertilitet (se nedan). Standardanalyser är testosteron, SHBG (sexualhormonbindande globulin), FSH (follikelstimulerande hormon) och LH (luteiniserande hormon). På grund av dygnsvariation av testosteron måste provtagningen ske fastande, före kl 10 på förmiddagen. Genom att mäta FSH och LH kan man fastslå om störningen i reproduktionsfunktionen relaterar till en hypotalamisk/hypofysär (hypogonadotropisk) eller testikulär (hypergonadotrop) defekt. Normala FSH- och LH-nivåer utesluter dock ej dysfunktion i testiklarna.
Ca 20–35 procent av alla män med nedsatt sädeskvalitet har tecken på dysfunktion i testosteronproducerande Leydigceller [12-14], varför testosteronanalysen rekommenderas för den patientgruppen. Hos patienter med låga testosteronnivåer i kombination med lågt eller relativt lågt FSH och LH kan även prolaktinkoncentrationen kontrolleras för att utesluta ett prolaktinom. Inhibin B är en markör för sertolicellfunktionen, men ingen obligatorisk del av standardutredningen. Insulinlik peptid 3 (INSL3) är en ny och lovande markör för Leydigcellfunktionen, men analysens roll i den kliniska utredningen är än så länge oklar.
Genetiska test. I en studie som omfattade 2 078 ofrivilligt barnlösa par som behövde assisterad befruktning för att kunna bli föräldrar fann man en genetisk orsak hos 4 procent av någon i paret, lika fördelat på män och kvinnor (1,97 procent per person). Risken för att hitta kromosomanomalier är högst bland män med inga eller få spermier i ejakulatet [15]. I bakgrundsbefolkningen är motsvarande andel 0,85 procent [16]. Att undersöka ärftliga faktorer vid infertilitet kan därför ibland vara befogat. Det kan för de drabbade kännas viktigt att få en förklaring till barnlösheten, men kan också vara vägledande för efterföljande handläggning av paren och för släktingar till dem.
Genetisk testning är välgrundad hos män med idiopatisk oligozoospermi (< 5 × 106 spermier/ml) eller icke-obstruktiv azoospermi. Den kan också vara motiverad vid fler än tre spontana aborter hos par som försöker bilda familj. Den vanligaste genetiska defekten hos både kvinnor och män är kromosomavvikelser, vilka detekterats hos ca 13 procent av män med azoospermi och 4 procent med oligozoospermi [17]. En extra X-kromosom (47,XXY, Klinefelters syndrom) ses hos 3–4 procent av infertila män [18], och i bakgrundsbefolkningen är prevalensen 1:500 (0,2 procent). Cirka 75 procent av alla män med 47,XXY-karyotyp är odiagnostiserade [19]. Detta i sin tur beror på att fenotypen är varierande. Mest karakteristiskt för män med Klinefelters syndrom är, förutom infertilitet och azoospermi, att de har små fasta testiklar (oftast <5 ml). Deras egna spermier är dock till >90 procent normala, utan någon extra kromosom, varför risken för Klinefelterpappors barn att ärva kromosomavvikelsen inte är ökad i förhållande till dem vars pappor har normal karyotyp. Spermier bildas med normal könskromosomuppsättning [20], och med hjälp av assisterad befruktning kan ungefär hälften av dessa män också få biologiska barn [21].
Hos män med bilateral agenesi av vasa deferentia är genetisk testning också motiverad. Dessa män är ofta bärare av två mutationer i cystisk fibros (CF)-genen men saknar andra symtom på CF. Då 1:35 bär på anlaget bör man också undersöka om den kvinnliga partnern är heterozygot för CF-mutationen, eftersom deras barn i så fall har 50 procents risk att få sjukdomen.
Ungefär 5 procent av alla män med svår oligozoospermi eller icke-obstruktiv azoospermi är bärare av Y-kromosom- deletioner [22]. Dessa inträffar oftast i den så kallade azoospermifaktor (AZF)-regionen, vilken i sin tur är uppdelad i områdena a, b och c. Medan mikrodeletioner i AZFa och AZFb ofta är associerade med svåra defekter i spermatogenesen, kan deletioner i distala delen av AZFb eller AZFc, som också kallas DAZ (deleted in azoospermia), förekomma samtidigt med viss spermieproduktion. Den kliniska implikationen är att man vid azoospermi och deletioner i distala AZFb och i AZFc kan finna spermier med mikrokirurgisk spermieaspiration/-extraktion (TESA/TESE) från testiklarna, medan deletioner i AZFa i princip alltid innebär utebliven spermatogenes. För män med Y-mikrodeletion och ofrivillig barnlöshet kan assisterad befruktning vara en lösning.
Behandling
Gonadotropinbehandling. Man vet sedan länge att behandling med gonadotropinfrisättande hormon (GnRH) eller gonadotropiner (FSH + koriongonadotropin [hCG] eller LH) vid hypogonadotrop hypogonadism i 75–85 procent av fallen leder till spermieproduktion. De senaste årens forskning har också indikerat att FSH-behandling av män med oförklarlig oligozoospermi kan stimulera spermieproduktionen. Såväl dosen FSH som behandlingstiden tycks spela en roll för utfallet: mer än 200 IE rFSH i minst 3 månader krävdes för positiv inverkan på spermieproduktionen (Tabell 3) [23]. I en metaanalys fann man positiv effekt av FSH-behandlingen på graviditetschansen, både spontant och efter assisterad befruktning [24]. FSH kan också ha en positiv inverkan på spermiemorfologi och -motilitet och motverka spermiekromatinbrott. FSH-behandling av män är inte klinisk rutin, men kan hos utvalda grupper bli en av framtidens nya infertilitetsterapier.
Kirurgi och assisterad befruktning. Kirurgiska procedurer används först och främst hos män med azoospermi. Vid obstruktiv azoospermi kan spermier antingen aspireras från epididymis (PESA) eller från testiklarna (TESA) och därefter användas vid ICSI. En del medfödda anomalier kan leda till att mittlinjecystor i prostata bildas, vilket i sin tur resulterar i ductus ejaculatorius-obstruktion. Det finns fallbeskrivningar där man korrigerat för defekten (transuretral resektion) och samtidigt fått förbättrade spermieparametrar [25], men denna teknik används sällan eftersom utgången är osäker, samtidigt som risken för komplikationer inte är försumbar och dessa män ändå oftast måste genomgå PESA/TESA.
Vid icke-obstruktiv azoospermi är spermatogenesen defekt. Tekniker för att hämta spermier från dessa patienters testiklar beskrivs annorstädes i detta temanummer.
Effekten av varikocelekirurgi på den manliga fertiliteten och chansen för graviditet in vivo eller in vitro är fortfarande omdiskuterad, eftersom större randomiserade högkvalitetsstudier saknas [26, 27].
Livsstilsrekommendationer. Trots många rapporter om att livsstilsfaktorer som rökning, övervikt och alkoholkonsumtion är kopplade till försämrad spermiekvalitet finns ännu inga bevis för att ändringar i livsstil leder till förbättrad fertilitet. Även om livsstilsförändringar skulle vara effektiva i relation till generell hälsa är det också osäkert om de påverkar utfallet av assisterad befruktning. Detta gäller också dietförändringar eller tillskott av olika näringsämnen, till exempel antioxidanter.
Långtidsföljder. Flera studier har visat att infertilitet kan vara en tidig markör för framtida morbiditet och mortalitet [26]. Infertila män har högre risk för hjärt–kärlsjukdomar och diabetes [18], aggressiv prostatacancer [28] och neurologiska sjukdomar [29] än fertila män. De har också högre risk för prostatacancer tidigt i livet [30], hypertension, metabolt syndrom och hypogonadism [12, 14]. Skånska män som var barnlösa under 1970-talet hade också högre kardiovaskulärt betingad mortalitet än de som under samma period var fäder [31]. De bakomliggande orsakerna är ännu inte klarlagda, men forskning pågår för att öka kunskapen om hur de som har högst risk för framtida sjukdomar ska kunna särskiljas från bakgrundsbefolkningen. Dessa män skulle i så fall kunna erbjudas prevention och uppföljning, eftersom kontakten med fertilitetskliniker ofta är den första och ibland den enda sjukvårdskontakten unga män har.
Forskningsbehov och perspektiv. Sedan introduktionen av IVF och inte minst ICSI har mycket av forskningen handlat om optimering av metoderna för assisterad befruktning. De andrologiska aspekterna av infertilitet är fortfarande i hög grad outforskade. I detta avseende är till exempel FSH-behandling av män med oligozoospermi eller åtgärder för att minska spermie-DNA-fragmentering angelägna forskningsområden. Det räcker inte heller att begränsa utredningen av den manliga partnern till en analys som bara fastställer om det finns spermier i ejakulatet eller ej. Om utredningen visar att fertilitetsstörningen huvudsakligen finns hos den manliga partnern bör man hitta strategier för att åtgärda den. Effektiva åtgärder mot manlig infertilitet skulle minska behovet för IVF och hormonstimuleringar av den kvinnliga partnern med de biverkningar dessa medför.
Om manlig infertilitet är en tidig biologisk markör för osteoporos, vissa cancertyper samt metabola och kardiovaskulära sjukdomar, så skulle yngre män utan klara sjukdomstecken och som sällan har kontakt med sjukvården representera en målgrupp för sjukdomsförebyggande screening. Detta förfarande skulle potentiellt minska risken för framtida sjukdomar för den enskilde individen och ge samhället lättnader i de kostnader som behandlingar av dessa folksjukdomar för med sig.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.