Vetenskapliga artiklar som bygger på oredlig forskning kan snedvrida metaanalyser, riktlinjer, klinisk praxis och folkhälsopraxis. I artikeln ges en rad exempel.
Oredlig forskning redovisar ofta spektakulära resultat och stora effekter samt citeras ofta okritiskt.
Det är mycket vanligt att artiklar som dragits tillbaka på grund av oredlighet fortsätter att citeras utan förbehåll, även i metaanalyser.
Flera element i hanteringen av vetenskapliga artiklar minskar risken för att oredlig forskning får genomslag i praxis.
Oredlig forskning kan leda andra forskare på fel spår och minskar förtroendet för det enskilda universitetet och vetenskapen i stort.
Det vetenskapliga underlag vi lutar oss mot för klinisk praxis, kliniska riktlinjer och folkhälsoinsatser snedvrids om det bygger på oredlig forskning. Följderna blir särskilt allvarliga när artiklar som dragits tillbaka på grund av oredlighet fortsätter att citeras okritiskt över lång tid. Oredlig forskning kan också skada förtroendet för hälso- och sjukvårdens vetenskapliga underlag i stort. Jag utgår i denna artikel från några uppmärksammade fall av oredlighet som kan få oss att skärpa vår kritiska blick. Dessutom diskuteras de skyddssystem som finns och som ger en viss motståndskraft mot den oredliga forskningens skador. Slutligen går jag igenom några av de åtgärder som föreslagits för att komma till rätta med problemen kring oredlig forskning.
Konsekvenser för klinisk praxis
Joachim Boldt, tysk anestesiolog. Fallet Boldt är ett särskilt anslående exempel på hur oredlig forskning påverkat klinisk praxis och orsakat omfattande patientskador [1-3]. Boldt var något av en stjärna i tysk intensivvård, hade ett gott internationellt renommé och var en högproduktiv forskare. Vid 46 års ålder, innan hans forskarkarriär fick ett abrupt slut, hade han publicerat 348 vetenskapliga arbeten.
Boldts mest uppmärksammade forskning rörde plasmaersättningsmedlet hydroxietylstärkelse (HES), marknadsfört som Hemohes i många länder, däribland Sverige. Boldt publicerade från 1980-talet och framåt en lång rad artiklar där han fann att svårt sjuka intensivvårdspatienter hade fördelar av att behandlas med HES jämfört med salt-/sockerlösningar och albumin [1, 2].
Många av Boldts artiklar publicerades i Anesthesia & Analgesia, den officiella tidskriften för International Anesthesia Research Society. Redaktören började få larmsignaler från uppmärksamma läsare: stämde verkligen Boldts resultat? En visselblåsare beskrev dem som »magiska«. Redaktören lusläste artiklarna och övertygades om att data måste vara fabricerade.
En utredning av det tyska läkarförbundet bekräftade misstankarna om forskningsfusk. Boldt och flera av hans medarbetare fick sparken från sina arbetsplatser 2011, och de artiklar som visat sig bygga på fabricerade eller manipulerade uppgifter började dras tillbaka. Med 164 återkallade artiklar ligger Boldt nu tvåa på den föga hedrande listan över flest återkallade artiklar (överträffad bara av en japansk anestesiolog) [4].
Boldts artiklar hade bidragit till att HES i många länder kommit till utbredd användning inom intensivvården. Inte före 2013, då en kanadensisk metaanalys sammanställde resultaten från 38 kliniska prövningar av HES i intensivvård, klarnade bilden: när Boldtgruppens resultat uteslöts ur analysen medförde HES ökad risk för njursvikt och död [5]. En uppskattning från London School of Hygiene and Tropical Medicine kom fram till att 200–300 personer avled varje år enbart i Storbritannien för att de behandlats med HES till följd av Boldts fabricerade resultat [2]. Den europeiska läkemedelsmyndigheten EMA förbjöd användning av HES i europeisk intensivvård 2018.
Scott Reuben, amerikansk smärtforskare. Reuben fabricerade patienter i analgetikastudier och rapporterade genomgående gynnsamma effekter av läkemedlen. Chefredaktören för Anesthesia & Analgesia, en av de tidskrifter som publicerat artiklar av Reuben, sa senare: »Vi talar om miljoner patienter över hela världen, där smärtbehandling efter operation har påverkats av dr Reubens forskningsfynd« [6]. Hans forskning fortsatte att citeras åtminstone 10 år efter avslöjandet [7]. I ett tidigt skede fick hälften av citeringarna kommentarer om att oredlighet förekommit, men med åren kom Reubens resultat att citeras okritiskt. Det förefaller som om hans forskningsfusk fortsätter att påverka klinisk praxis.
Yoshihiro Sato, japansk osteoporosforskare. Under 15 år publicerade Sato och hans grupp resultaten från 33 randomiserade prövningar vid osteoporos. År 2016 hade hans prövningar citerats 1 158 gånger, inklusive i 68 systematiska översikter, kliniska riktlinjer och liknande. Tre år senare hade 27 av hans artiklar återkallats på grund av fabricering av data, plagiering och annan oredlighet. Vid förnyad granskning visade det sig att 13 av riktlinjerna/de systematiska översikterna skulle ändras om Satos studier uteslöts (plus 8 osäkra). Bara en av de 68 riktlinjerna/systematiska översikterna hade korrigerat sin analys efter återkallelserna [8]. De falska vetenskapliga spår Sato lämnat efter sig har fortsatt att snedvrida det vetenskapliga underlaget för klinisk praxis.
Konsekvenser för folkhälsa
Någon gång händer det att en artikel med fabricerade data från några få patienter får väldiga konsekvenser för folkhälsan. När den brittiske gastrokirurgen Andrew Wakefield publicerade en artikel i Lancet 1998 om ett samband mellan trippelvaccination (för mässling, påssjuka och röda hund) och autism hos 12 barn fick hans resultat enorm spridning i medierna. I Storbritannien sjönk andelen vaccinerade barn från omkring 92 till 80 procent som lägst (i London under 50 procent) [9, 10]. I USA fick antivaccinationsrörelsen ett stort uppsving. Mässlingsepidemier med dödsfall bröt ut i båda dessa länder. Wakefields resultat visade sig bygga på oredlig forskning, och hans läkarlegitimation återkallades [11].
Hans Eysenck tar ändå priset när det gäller negativa folkhälsoeffekter av oredlig forskning [12, 13]. Han var en central gestalt i internationell psykologiforskning och publicerade över 1 600 vetenskapliga artiklar och ett 80-tal böcker. Hans budskap om att personlighetstyp (undertryckt aggressivitet) är en större riskfaktor för cancerdöd än rökning, byggt på fabricerade data, välkomnades av tobaksindustrins marknadsavdelningar (samma industri som även hade finansierat forskningen). Eysencks slutsatser levde kvar i läroböcker och kunskapsöversikter fortfarande mer än 20 år efter hans död, men exakt hur många liv som skördades på grund av hans forskningsfusk är förstås svårt att uppskatta.
Andra exempel på forskningsresultat som byggt på oredlighet och som haft stort publikt genomslag och potentiella folkhälsoeffekter:
- Hormonbehandling i anslutning till klimakteriet har gynnsamma hälsoeffekter på hjärta, kärl och ämnesomsättning [14].
- Nestlés modersmjölksersättning kan förebygga barnallergi [15].
- NSAID-preparat, såsom ibuprofen, minskar risken för munhålecancer hos rökare [16].
Den oredliga forskningens profil
Fallet Joachim Boldt är ett drastiskt exempel på hur oredlig forskning genom snedvridna resultat direkt påverkar utfallet av systematiska översikter och klinisk praxis. Men fallet är inte unikt: åtskilliga analyser av artiklar som dragits tillbaka på grund av oredlighet visar ett tämligen samstämmigt mönster.
Större genomslag. Tillbakadragna artiklar har före avslöjandet om oredlighet haft större genomslag än andra artiklar. Påfallande många har hundratals citeringar, några av dem över 1 000 [17]. I anslutning till publiceringen uppmärksammas originalartiklarna i konventionella nyhetsmedier och på sociala medier ungefär dubbelt så ofta som matchade icke återkallade artiklar [18]. Skillnaderna i medieuppmärksamhet kvarstår även sedan man i analyserna exkluderat de artiklar som berättar om att forskningen varit oredlig [19].
Större rapporterade effekter. En granskning av drygt 3 000 metaanalyser visade att författare som publicerat återkallade artiklar redovisar i genomsnitt större effekter/skillnader än vad andra författare gör [20]. Även om en intervention skulle ha en viss reell effekt ger uppblåsta resultat byggda på oredlig forskning en överdriven bild av hur stor effekten faktiskt är.
Fortsatt okritisk citering
Det finns en omfattande vetenskaplig litteratur som belyst problemet med att vetenskapliga artiklar fortsätter att citeras trots att de återkallats. Det är vanligt att redan tillbakadragna artiklar från randomiserade prövningar inkluderas i systematiska kunskapsöversikter och kliniska riktlinjer, oftast utan att återkallelse nämns. I ungefär två tredjedelar av metaanalyser som citerade återkallade artiklar hade återkallelserna skett mer än ett år före publiceringen, och inklusionen av deras resultat skulle alltså vara undvikbar [21].
Liknande observationer gjordes vid en granskning av 525 systematiska kunskapsanalyser och 62 kliniska riktlinjer, vilka alla citerat artiklar som återkallats. I 67 procent av fallen hade en redan återkallad artikel inkluderats i det vetenskapliga underlaget utan kommentar (Figur 1). Om en artikel återkallats efter publiceringen av en systematisk översikt eller riktlinje var det sällsynt ‒ 3 procent av fallen ‒ att analyserna korrigerades [22].
»Fejkresistent« system?
Jag har här tagit upp exempel, några av dem synnerligen allvarliga, på hur resultat från oredlig forskning kan snedvrida systematiska kunskapsöversikter, kliniska riktlinjer och klinisk praxis. Det finns dock en del som talar för att oredligheten ganska sällan har avgörande effekter på dessa typer av sammanfattande kunskapsstöd – systemet tycks ha en viss motståndskraft mot att smittas av fabricerade resultat, något som analogt med faktaresistens skulle kunna kallas »fejkresistens«.
Vid en granskning av 229 metaanalyser som citerade återkallade artiklar fann Fanelli et al att citeringarna i hälften av fallen inte återfanns i dataanalysen utan bara i introduktionen eller diskussionen, och då nästan utan undantag omnämndes i positiva ordalag [21].
Sedan gick författarna vidare till frågan: vad betyder inklusionen av en artikel byggd på oredlig forskning för kunskapsunderlagets tillförlitlighet? Som väntat ökade konfidensintervallen (färre observationer), men metaanalyser inkluderar ofta ett stort antal studier, så varje enskild studie, om än byggd på oredlig forskning, bidrar relativt litet till det sammanvägda utfallet. Fanelli et al fann därför att effektstorleken av en intervention blev bara måttligt mindre när de återkallade artiklarna uteslöts ur metaanalyserna [21]. Endast stora studier med fabricerade data har tillräcklig statistisk kraft för att påverka metaanalysernas sammanvägda resultat. Om forskningsfältet är nytt och den systematiska kunskapsöversikten inkluderar relativt få studier är risken däremot större att en studie byggd på oredlig forskning påverkar utfallet.
Något som bidrar till fejkresistensen är att artiklar som återkallas på grund av oredlig forskning ofta har andra kvalitetsbrister som gör att de inte uppfyller strikta inklusionskriterier för metaanalyser och andra systematiska översikter. Dessutom kan, som fallet Boldt visar, en metaanalys avslöja en forskargrupp som manipulerat data så mycket att resultaten tydligt skiljer sig från vad andra forskargrupper funnit.
Skyddssystemet är dock långt ifrån tillräckligt, och som fallet Sato visar behöver det stärkas ytterligare. Många av de som tagit upp problemet med fortsatt okritisk citering av tillbakadragna artiklar har funnit ett behov av mycket tydligare märkning av tillbakadragandet – i dag varierar praxis markant mellan olika tidskrifter och databaser [21-23].
Andra offer för oredlig forskning
Forskningsresultat byggda på oredlighet kan leda andra forskare in på felaktiga vägar och resultera i att tid och resurser ödslas på meningslösa forskningsprojekt. I den hårda konkurrensen om forskningsanslag skaffar sig fuskare orättfärdiga fördelar. De synnerligen stora anslag Paolo Macchiarini drog in från EU, Vetenskapsrådet och Stockholms läns landsting hade kunnat användas för annan angelägen forskning [24].
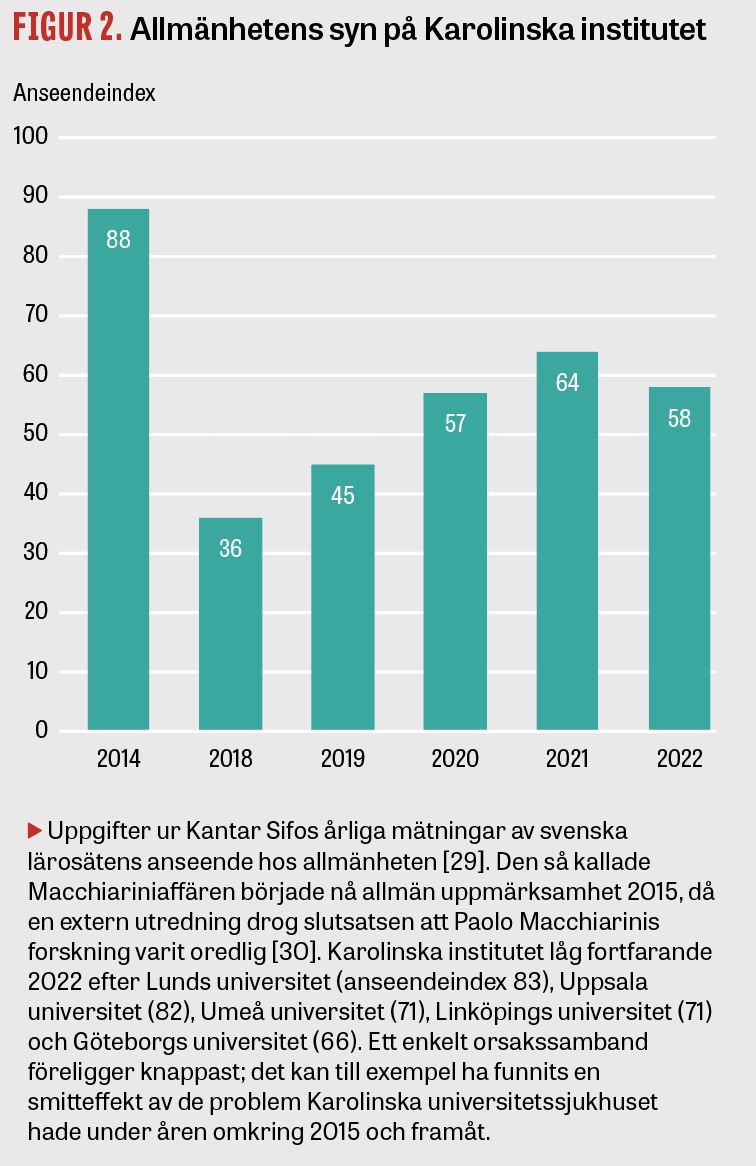
Förtroendet för ett universitet kan skadas av oredlig forskning. Innan »Macchiariniaffären« började avslöjas 2015 hade Karolinska institutet högst anseende av alla lärosäten hos den svenska allmänheten. Under affären sjönk anseendet drastiskt, och återhämtningen har gått långsamt (Figur 2).
Inte bara det drabbade universitetet utan också forskningen i stort kan ta stryk genom att dess anseende i samhället skadas. Vetenskap och allmänhet är en ideell förening som funnits sedan 2002 vars ändamål är att främja öppenhet och dialog mellan forskare och det omgivande samhället. Efter Macchiariniaffären genomförde föreningen en enkät för att undersöka hur avslöjandet hade påverkat den svenska befolkningens syn på forskning [25]. Av dem som svarade på enkäten uppgav mer än en tredjedel (35 procent) att deras inställning till medicinsk forskning påverkats negativt. En viss smitteffekt kunde skönjas: fler än var tionde (11 procent) uppgav att de även blivit mer negativa till forskning på andra områden än medicin.
Vad kan göras?
Hur ska hälso- och sjukvården och akademin skydda sig mot den oredliga forskningens skadeverkningar? Mycket handlar om prevention och tidig upptäckt.
De viktigaste förebyggande insatserna görs inom forskargruppen genom att värna om en kultur där även mindre avsteg från god forskningssed inte tolereras. Det ska exempelvis vara oacceptabelt att avstå från att publicera resultat som inte bekräftar hypotesen, att eliminera obekväma datapunkter eller att mixtra med bilder så att de inte blir rättvisande. Det finns åtskilligt att lära sig från den lilla skriften »Den europeiska kodexen för forskningens integritet« [28]. Där listas, utöver sådan oredlighet som täcks in av den svenska lagstiftningen (fabrikation, förfalskning och plagiering), 14 oacceptabla beteenden i forskningen.
Universiteten har en viktig uppgift att utbilda om forskningsetik och förekomsten av oredlighet. Detta gäller inte bara doktorander och juniora forskare – erfarenheterna visar att seniora forskare också kan behöva utbildning. I flera av exemplen i denna artikel har det definitiva avslöjandet dröjt för att man negligerat tidiga varningssignaler. Slutsatsen är att personer i ledningsfunktioner, vare sig det gäller institutioner, universitet, kliniker eller sjukhus, måste ta tidiga signaler på oredlighet och visselblåsare på största allvar.
På den nationella nivån har vi i Sverige, som ett av få länder, sedan ett par år en lag om oredlighet i forskning och en särskild myndighet, Nämnden för prövning av oredlighet i forskning, som är ansvarig för tillsynen av lagen [26, 27].
Inte sällan har det varit kritiska läsare av vetenskapliga publikationer som avslöjat oredlighet. Är inte resultaten för bra för att vara sanna? Varför är konfidensintervallen onaturligt snäva? Varför dyker samma bild upp i två publikationer för att illustrera helt olika resultat? De experter som arbetar med kliniska riktlinjer behöver vara särskilt observanta, i synnerhet när resultaten från olika studier spretar mycket. När riktlinjer uppdateras behöver de dessutom granska att äldre artiklar som dragits tillbaka inte finns med.
Också tidskriftsredaktionerna engagerar sig i kampen mot oredlighet. Sedan länge har det funnit dataprogram som avslöjar plagiering, en variant av forskningsfusk som är på nedgång. Redaktionernas process för att dra tillbaka artiklar som bygger på oredlig forskning kan bli snabbare, och en del tidskrifter kan behöva markera tydligare i alla relevanta databaser att artikeln är tillbakadragen. När en artikel dragits tillbaka bör det också finnas ett krav på att de systematiska översikter som citerat den felaktiga artikeln revideras.
Den tekniska utvecklingen kan komma till stor hjälp. Bildmanipulation håller på att bli den dominerande formen av forskningsfusk [3]. Med alltmer sofistikerade bildbearbetningsprogram blir det svårare att med blotta ögat upptäcka manipulationer av exempelvis elektrofores-, mikroskop-, MR- och PET-bilder. Många hoppas att artificiell intelligens kommer att bli ett kraftfullt verktyg för att avslöja denna typ av fusk. Likaså kan avancerade statistikprogram vara till hjälp för att skilja »naturliga« biologiska, psykologiska eller beteendevetenskapliga data från sådana som fabricerats.
Den kritiska ansatsen är central när hälso- och sjukvårdens vetenskapliga underlag ska bedömas. Att ta del av historierna om fuskare som Boldt, Wakefield och Macchiarini kan hjälpa oss att skärpa vår kritiska blick. Vi tvingas fundera på hur klinisk praxis och folkhälsoarbete kan skyddas mot oredlig forskning och vad som kan göras så att patienter inte kommer till skada eller förtroendet för vetenskapen urholkas
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.