Diagnostik och uppföljning av majoriteten av patienter med astma sker i primärvården.
Den varierande luftvägsobstruktionen gör att astmadiagnostik kan vara svår. Anamnes och lungfunktionsmätningar är grundstenen.
Även de med enbart sporadiska symtom ska ges behandling med inhalationssteroider (steg 1).
Patientutbildning är avgörande för god astmakontroll.
Optimal astmakontroll innebär normal lungfunktion, symtomfrihet och avsaknad av exacerbationer. Detta ska alltid bedömas.
Vid okontrollerad astma bör behandlingsbarriärer såsom bristande inhalationsteknik, otillräcklig följsamhet till behandling, exponering för utlösande faktorer och eventuell påverkan av samsjuklighet bedömas.
Primärvården har ett stort ansvar för diagnostik och uppföljning av majoriteten av patienter med astma. Kontinuitet i patient–läkarrelationen, interprofessionell samverkan och regelbunden fortbildning är viktiga hörnstenar för ett lyckat omhändertagande. Det är ofta en utmaning att få astmavården, med både noggrann utredning och adekvat uppföljning, att fungera optimalt i den tids- och resursbristdrabbade primärvården.
Folksjukdomen astma
Astma är en sjukdom som har varit känd så länge som det funnits skrifter om sjukdomar och läkekonst. Fram till 1990-talets början var akuta, svåra astmaanfall (exacerbationer) vanligt förekommande. De var också bland de mest fruktade tillstånden jourhavande läkare kunde möta. Akut astma var ofta svårbehandlad, oberäknelig och potentiellt livshotande. I dag känner de yngre läkarna – och merparten av patienterna – knappast igen denna bild. Den moderna antiinflammatoriska behandlingen med inhalationssteroider har bidragit till radikalt förbättrade symtom och prognos, trots att prevalensen av astma har ökat under den andra halvan av 1900-talet [1]. I dag har de flesta personer med astma en kronisk, men oftast lindrig, sjukdom med intermittenta besvär. Dödsfall i astma är i dag mycket sällsynta. Oavsett svårighetsgrad ger astma dock fortfarande en betydande negativ påverkan på livskvaliteten [2].
Astma är en folksjukdom som drabbar alla åldersgrupper. Den uppskattade prevalensen i Sverige är cirka 10 procent [3]. Det finns dock en betydande underdiagnostik: nästan hälften av personerna med astma är odiagnostiserade [4]. I vårt land omhändertas de allra flesta personer med astma i primärvården. I Region Stockholm sker till exempel 98 procent av astmarelaterade besök av vuxna i primärvården, inklusive närakutmottagningar, och den typiska primärvårdspatienten med astma är en pojke (bland barn) eller en kvinna (bland vuxna) och tillhör socioekonomiskt en låg- eller medelinkomstfamilj med låg eller medelhög utbildningsnivå (Gap-analys, internt arbetsmaterial, Hälso- och sjukvårdsförvaltningen, Region Stockholm; 2020). En stor andel av patienter med astma har också samtidig allergisk rinit, och upp mot 10 procent har både astma och KOL-diagnos i journalen [5].
Diagnostik i primärvården
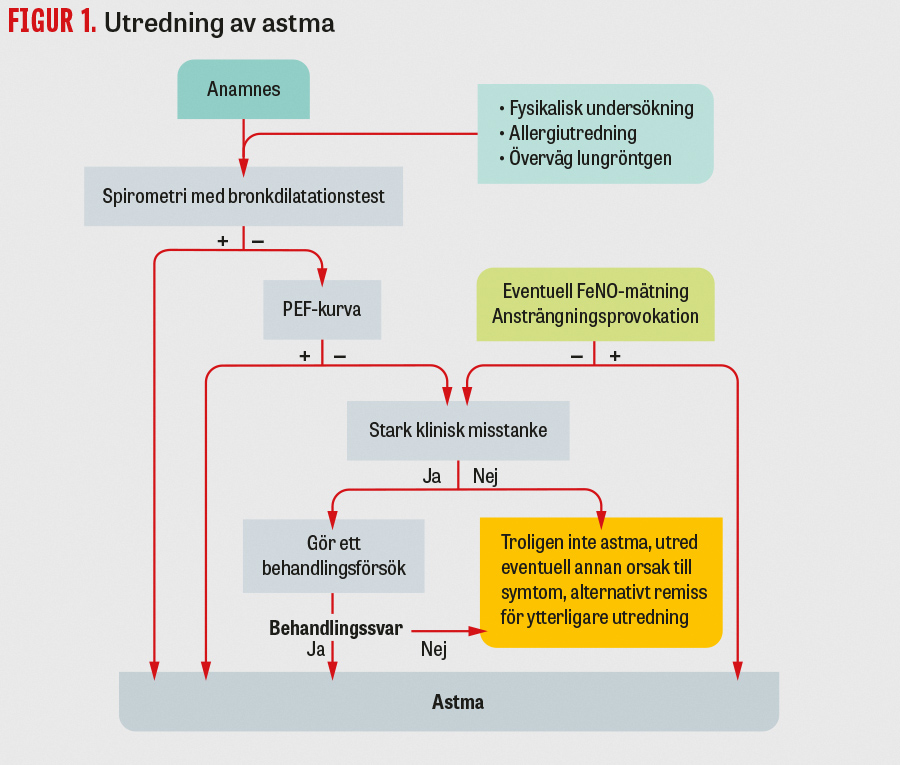
Eftersom astma kännetecknas av varierande symtom och grad av luftvägsinflammation kan diagnostiken vara svår och tidskrävande. En strukturell utredning enligt Läkemedelsverkets senaste behandlingsrekommendationer (2023) kan vara till god hjälp [6] (Figur 1).
En noggrann anamnes utgör grunden i all astmautredning. Spirometri tillhör basutredningen av obstruktiva lungsjukdomar, men på grund av variabiliteten utesluter ett normalt spirometriresultat inte astma. Ett positivt bronkdilatationstest (reversibilitetstest) med 12 procents ökning av FEV1 (forcerad exspiratorisk ensekundsvolym) och minst 200 ml samtidigt som kvoten FEV1/FVC (forcerad vitalkapacitet) är normal efter bronkdilatation talar för astma. Notera att många med KOL vid spirometri uppvisar en reversibilitet som är mer än 12 procent, men kvoten FEV1/FVC förblir alltid under 0,7. Vid klinisk misstanke om astma och normal spirometri kan utredningen med fördel fortsätta med mätningar av topputandningsflöde (peak expiratory flow, PEF), som kan fånga in dygnsvariabilitet och/eller situationsrelaterad variabilitet (det vill säga skillnaden mellan bästa PEF och när symtomen uppträder, till exempel vid ansträngning eller vid allergi), som i så fall bekräftar astmadiagnosen [7]. Vid typisk anamnes och normala lungfunktionsmätningar kan den mest praktiska handläggningen vara att provbehandla med medelhög eller hög dos av inhalationssteroider i 8–12 veckor och därefter genomföra en ny symtomkontroll och lungfunktionsmätning för att se om förbättring har skett. I enstaka fall, om luftvägsobstruktionen är svår att visa, kan patienten behöva remitteras till provokationstest (metakolin-, mannitol-, torr luft- eller ansträngningstest).
Vid astmautredning är det viktigt med en utförlig allergianamnes. Allergitest bör erbjudas vid klinisk misstanke om allergi och alltid frikostigt hos barn. Pricktest och riktade IgE-test är likvärdiga, men för att allergi ska anses föreligga ska positiva testresultat alltid åtföljas av anamnestiska uppgifter om allergisymtom vid exponering.
Gradering av luftvägsinflammation är svår, men mätning av eosinofila celler i blodet kan vara av värde. Mätning av kväveoxid i utandningsluft (FeNO) som markör för typ 2-inflammation är i dag tillgänglig på enstaka vårdcentraler, men tillhör inte basutredningen i primärvården. Användning av FeNO-mätaren i primärvården har dock i studier visat sig kunna bidra till bättre astmakontroll och livskvalitet hos primärvårdspatienter med astma [8].
Lungröntgen bör göras hos rökande patienter och om differentialdiagnostiken motiverar det. Differentialdiagnoser som är viktiga att utesluta vid astmautredning är till exempel KOL, hjärtsjukdom, bronkiektasier, sensorisk hyperreaktivitet, ansträngningsutlöst laryngeal obstruktion och dysfunktionell andning.
Uppföljning i primärvården
Målet med den moderna astmabehandlingen är att patienten ska uppnå »optimal astmakontroll« med normal lungfunktion, symtomfrihet i vardagen samt avsaknad av akuta exacerbationer under 12 månader (Fakta 1). Lungfunktionen bör vid uppföljning kontrolleras med spirometri.
Symtomkontroll kan bedömas med hjälp av astmakontrolltest (ACT eller AKT) [9]. ACT är ett frågeformulär med 5 frågor där en totalsumma av 20–25 poäng (av maximalt 25 poäng) tyder på god symtomkontroll. Frågorna speglar endast de senaste 4 veckorna och måste kompletteras med uppgifter om symtom och exacerbationer under övriga delar av året. I stället för att bara notera totalpoängen på ACT kan man få mer nytta av testet genom att använda de enskilda frågorna som underlag för en diskussion under patientkonsultationen.
Regelbunden uppföljning 1 gång per år, antingen hos läkaren eller astma/KOL-sjuksköterska, rekommenderas för dem med regelbunden underhållsbehandling, och oftare vid otillräcklig astmakontroll [10]. Att detta ofta inte kan genomföras trots riktlinjerna beror till stor del på brist på både allmänläkare och astma/KOL-sjuksköterskor. Många patienter vet inte heller varför man bör gå på regelbunden kontroll.
Patientutbildning
Primärvårdens uppgift är också att med lämplig patientutbildning få patienten att förstå målet med astmabehandlingen, varför en god astmakontroll är viktig och hur man kan nå den med egenvård. Resursbristen i primärvården bidrar till att endast ett fåtal astma/KOL-mottagningar har den tid som rekommenderas [11]. Då samtidig rökning minskar effekten av inhalationssteroider [12] och dessutom ökar risken för KOL är det viktigt att rökslutarstöd kan erbjudas på vårdcentralen.
Behandlingsplan
En skriftlig behandlingsplan underlättar för patienten att hantera och ta eget ansvar för sin sjukdom. Behandlingsplanen bör innehålla konkret och individualiserad information om behandlingen (Fakta 2).
Det är välkänt att en behandlingsplan tillsammans med patientutbildning förbättrar förutsättningarna för en välkontrollerad astma [13]. Ett tips för att åstadkomma en skriftlig behandlingsplan i den tidspressade primärvården är att läkaren och sjuksköterskan fyller i sina respektive delar i den och att den finns i digital form i journalen, så att den kan ändras vid behov och också vara lätt tillgänglig för patienten.
Om astman inte är under kontroll
Flera studier under de senaste två decennierna har visat att endast cirka 40–45 procent av patienterna i primärvården uppnår fullgod astmakontroll [14-16]. Akutbesök är fortfarande relativt vanliga: i Region Stockholm står de till exempel för 14 procent av alla astmabesök (Gap-analys, se ovan).
Om astman inte är under kontroll är det viktigt att identifiera eventuella behandlingsbarriärer, såsom att patienten har ordinerats inkorrekt behandling enligt riktlinjerna [6], att följsamheten till medicinering brister eller att patienten har en icke-fungerande inhalator eller felaktig inhalationsteknik. Studier har visat att uppåt 50 procent av patienterna har en felaktig inhalationsteknik, vilket också påverkar deras astmakontroll [17]. Det är därför viktigt att inhalationstekniken kontrolleras både vid nyinsättning av inhalationsläkemedel och vid återbesök, och särskilt vid byte av inhalator. Digitala verktyg, till exempel www.medicininstruktioner.se, kan med fördel användas både av förskrivande läkare och astma/KOL-sjuksköterskan som stöd i patientutbildningen.
Det är alltid viktigt att undersöka om patienten exponeras för luftvägsirritanter, i synnerhet allergener. Även otillräckligt behandlad samsjuklighet bidrar till sämre astmakontroll. Patienter med samtidig hjärtsjukdom, KOL eller allergisk rinit har en ökad risk för exacerbationer [5]. Övervikt kan också bidra till ökade symtom [18].
Om patienten inte uppnår symtomkontroll är det ibland viktigt att ifrågasätta om diagnosen astma är korrekt och överväga en alternativ diagnos, till exempel alfa-1-antitrypsinbrist eller annan lungsjukdom, som kan förklara patientens symtom.
Astma och läkemedelsbehandling
En orsak till icke-optimal astmakontroll är underbehandling. Både bristande kunskap inom sjukvården om Läkemedelsverkets behandlingsrekommendationer och bristande följsamhet till behandling hos patienten kan bidra till underbehandling. De senaste behandlingsrekommendationerna (2023) presenterar betydande förändringar av läkemedelsbehandlingen [6], illustrerade med en behandlingstrappa (Figur 2) där läkemedelsbehandlingen kan justeras både uppåt och nedåt. Inhalationssteroider (ICS) är basen för all läkemedelsbehandling vid astma, då de behandlar den underliggande inflammationen i luftvägarna. I de senaste rekommendationerna introduceras också ett nytt begrepp, FABA (fast acting beta-2 receptor agonist), för beta-2-receptoragonister med snabbt insättande effekt. FABA kan antingen ha lång (formoterol) eller kort verkan (salbutamol och terbutalin).
Framför allt har behandling på steg 1 förändrats. Redan vid mycket lindrig astma (symtom högst 2 gånger per månad), som tidigare behandlats med enbart kortverkande beta-2-receptoragonister (SABA) vid behov, rekommenderas nu behandling med inhalationssteroider i fast kombination med luftrörsvidgande läkemedel (ICS/FABA) vid behov. I praktiken kan enbart en fast kombination med ICS/formoterol användas som vidbehovsbehandling på steg 1. Vid mer frekventa symtom än 2 gånger per månad börjar behandlingen direkt på steg 2 med lågdos ICS dagligen med tillägg av ICS/formoterol vid behov.
Vid okontrollerad astma på steg 2 rekommenderas regelbunden behandling på steg 3 med ICS/långverkande beta-2-receptoragonister (LABA) i fast kombination, och som vidbehovsmedicinering antingen ICS/formoterol eller SABA. Om patienten redan före påbörjande av behandling har symtom 4–5 dagar i veckan eller mer eller vaknar nattetid på grund av astma är det lämpligt att börja behandlingen direkt på steg 3 [13]. Vid otillräcklig effekt av inhalationsmedicinering på steg 3 kan leukotrienreceptorantagonist (LTRA) provas som tillägg.
Vid otillräcklig astmakontroll är det alltid viktigt att systematiskt bedöma vad den bristande kontrollen kan bero på, innan man går upp till nästa steg på behandlingstrappan (se avsnittet ovan, »Om astman inte är under kontroll«).
Följsamheten till behandling med ICS är generellt låg [19]. Orsakerna till detta kan vara till exempel rädsla för biverkningar, okunskap och kostnader. Många slutar också med regelbunden behandling när man blivit symtomfri. Här är det viktigt med patientutbildning och patientens delaktighet i behandlingen.
Receptförnyelse
Vid begäran om receptförnyelse av astmaläkemedel via telefon, e-post eller »Mina vårdkontakter« (1177) är det viktigt att också bedöma patientens sjukdomskontroll (Fakta 1), och med ledning av detta bedöma behovet av läkarkontakt eller uppföljning.
Uppföljning efter astmaexacerbationer
Det är ytterst viktigt att följa upp patienter som sökt med akuta astmaexacerbationer för att bedöma astmakontroll, optimera behandlingen av både astman och eventuella komorbiditeter och stärka patientens egenvårdsfärdigheter. Socialstyrelsen rekommenderar uppföljning inom 6 veckor efter en akut exacerbation. Enligt en registerbaserad studie med patientdata från primärvården i Region Stockholm och Region Uppsala hade cirka 7 procent av patienter som behandlats för en akut exacerbation följts upp inom 6 veckor och 39 procent inom 15 månader. De allra flesta hade följts upp inom primärvården. Patienter som inte fick en uppföljning använde generellt mera SABA och perorala steroider än de som hade följts upp [20].
För bättre astmavård är det centralt att åstadkomma bättre fungerande remitteringsrutiner mellan akutsjukvården och patientens vårdcentral. På vårdcentralen bör patienter med akuta exacerbationer prioriteras och rutiner för uppföljning finnas.
Svårbehandlad eller svår astma?
När patientens astma fortsätter att vara okontrollerad trots systematisk bedömning uppstår frågan om patienten kan ha en svår astma eller om astman i stället är svårbehandlad. Av patienter med astma i Sverige har cirka 3-4 procent en svår astma [21]. Dessa patienter bör remitteras till den specialiserade vården för bedömning av fortsatt behandling. En remiss bör innehålla en noggrann beskrivning av den systematiska bedömning som primärvården har gjort (Fakta 3) [22].
Primärvårdens utmaningar, möjligheter och ansvar
Att identifiera patienter med okontrollerad astma som behöver intensifierad behandling och uppföljning är inte alltid enkelt. Interprofessionellt samarbete är en viktig del av en god astmavård, men att genomföra detta i praktiken kan ofta vara svårt [23]. Med god tillgänglighet och läkar–patientkontinuitet kan astma diagnostiseras tidigt, både kort- och långsiktiga behandlingsmål sättas och planer göras för att nå optimal kontroll av sjukdomen. Detta görs efter en individualiserad helhetsbedömning, som även tar hänsyn exempelvis till patientens hemmiljö, skola, arbetsplats och fritidsaktiviteter. Primärvården behöver kunna erbjuda lämplig patientutbildning och tydligt kommunicera behandlingsplanen till patienten, så att hen kan lära sig att hantera och ta eget ansvar för sin sjukdom.
Potentiella bindningar eller jävsförhållanden: Hanna Sandelowsky har under de senaste 5 åren erhållit arvoden för deltagande i rådgivande grupper och/eller föreläsningar vid utbildningsaktiviteter arrangerade av ALK, Astra Zeneca, Chiesi, Glaxo Smith Kline, Orion Pharma och Sanofi. Björn Ställberg har under de senaste 5 åren erhållit arvoden för föreläsningar och utbildningsaktiviteter arrangerade av Astra Zeneca, Boehringer Ingelheim, Novartis och Glaxo Smith Kline samt för deltagande i rådgivande grupper arrangerade av Astra Zeneca, Boehringer Ingelheim, Novartis och Glaxo Smith Kline.
Fakta 1. Tecken på okontrollerad astma [6]
- Hosta
- Slem
- Pip och väs i bröstet
- Luftvägssymtom kopplade till utlösande faktorer såsom rök, avgaser, starka dofter, kall eller fuktig luft och fysisk ansträngning
- Nattliga uppvaknanden på grund av astma
- Ökad användning av vidbehovsmedicinering
- PEF-variabilitet
- Exacerbation senaste året
- Frånvaro från skola eller arbete på grund av astmasymtom
- Trötthet
Fakta 2. Innehållet i behandlingsplan för astma
Läkemedel för underhållsbehandling
- Namn, styrka och dosering
- Tillfällen för dosjustering
Läkemedel som kan tas vid behov
- Namn, styrka och dosering
- Situationer då vidbehovsmedicinering är aktuell för att minska astmasymtomen, till exempel före fysisk ansträngning, vid allergiexponering, under luftvägsinfektioner
- Dosering vid akuta besvär
Uppgifter om patientens vårdkontakter
- Vad som bör föranleda akut kontakt med vården
- Kontaktuppgifter/telefonnummer för akut samt icke-akut vård
Råd om icke-farmakologisk behandling efter patientens behov
- Rökavvänjning
- Undvika/minska exponering för allergener och luftvägsirritanter
- Strukturerad uppvärmning före fysisk aktivitet
Fakta 3. Svår astma? Remissinnehåll till den specialiserade vården [22]
- Huvudsymtom/astmakontroll
- Exacerbationer senaste 12 månaderna, antal
- Aktuell och tidigare prövad läkemedelsbehandling
- Inhalationsteknik och läkemedelsföljsamhet
- Genomförd allergiutredning och exponering (yrke, allergener och annan relevant exponering)
- Annan sjukdom (samsjuklighet)
- Information om den senaste kliniska undersökningen
– Spirometri
– PEF
– Eventuellt provokationstest
– Laboratoriedata (blodeosinofiler, blodneutrofiler)
– Genomförd lungröntgen/DT