Prostatacancercentrum vid Capio S:t Görans sjukhus använder sedan 2017 en modell för strukturerad och sammanhållen prostatacancerdiagnostik.
Modellen använder undersköterskeledd diagnostik, Stockholm 3-testet och magnetresonanstomografi (MR) med riktad perineal vävnadsprovtagning.
Modellen medför korta ledtider, hög precision i diagnostiken och god hälsoekonomi.
Varje år drabbas cirka 10 000 män i Sverige av prostatacancer, varav cirka 2 000 dör av sjukdomen. Tidigt upptäckt prostatacancer går ofta att bota, medan sen upptäckt är förknippad med dålig prognos. Uppskattningsvis genomförs årligen nästan en halv miljon PSA-provtagningar i Sverige för att hitta prostatacancer tidigt [1].
2018 redovisade vi i Läkartidningen preliminära resultat från vår modell för tidig diagnostik på Capio S:t Görans sjukhus. Mycket har hänt sedan dess. Två välgjorda svenska studier har visat att MR och riktade vävnadsprov bör vara en del av en modern vårdkedja för prostatacancer [2, 3]. Transperineal vävnadsprovtagning rekommenderas nu i internationella riktlinjer för att minimera infektionsrisk [4], och sedan 2022 rekommenderar EU medlemsländerna att utvärdera organiserad screening för prostatacancer [5]. Ett flertal av Sveriges regioner har också kommit igång med organiserad prostatacancertestning, vilket leder till att vårdens resurser kan användas på ett mer effektivt sätt.
Trots framsteg finns fortfarande stora problem i dagens diagnostik. Tillgängligheten och kvaliteten är ojämn, och organiserad prostatacancertestning täcker ännu endast en mycket liten del av diagnostiken. Vidare finns ett underskott på resurser inom urologi, radiologi och patologi, vilket leder till långa väntetider inom standardiserade vårdförlopp för prostatacancer.
Här beskriver vi våra erfarenheter av en strukturerad och sammanhållen modell för tidig upptäckt av prostatacancer som satts upp på Capio S:t Görans sjukhus. Vår förhoppning är att den kan vara en inspirationskälla för jämlik vård i Sverige och leda till att vi utnyttjar våra begränsade resurser på bästa sätt.
För att förbättra möjligheten till tidig upptäckt och samtidigt undvika onödiga MR-undersökningar och biopsier använder vår modell Stockholm 3-testet som reflextest efter PSA. Stockholm 3-testet är, precis som PSA-provet, ett vanligt blodprov. Till skillnad från PSA-provet, som mäter en proteinmarkör, kombinerar Stockholm 3-testet drygt 100 proteinmarkörer samt genetiska och kliniska markörer för att beräkna risken för kliniskt betydelsefull prostatacancer (Gleason-summa 7 eller högre). Stockholm 3-testet har provats i flera stora studier, som visar att det kan minska risken för onödiga MR-undersökningar, biopsier och behandlingar, samtidigt som fler behandlingskrävande cancerformer kan identifieras tidigt jämfört med PSA [3].
Capio S:t Göran-modellen
Capio S:t Görans sjukhus har fått i uppdrag från Region Stockholm att sköta ca 25 procent av prostatacancervården i Stockholm, vilket motsvarar cirka 500 nya prostatacancerfall per år. Under 2017 etablerades Prostatacancercentrum vid Capio S:t Görans sjukhus med syftet att tillhandahålla kostnadseffektiv prostatacancerdiagnostik med hjälp av nya diagnostiska metoder och effektiva och strukturerade processer. Projektet är granskat och godkänt av Etikprövningsmyndigheten.
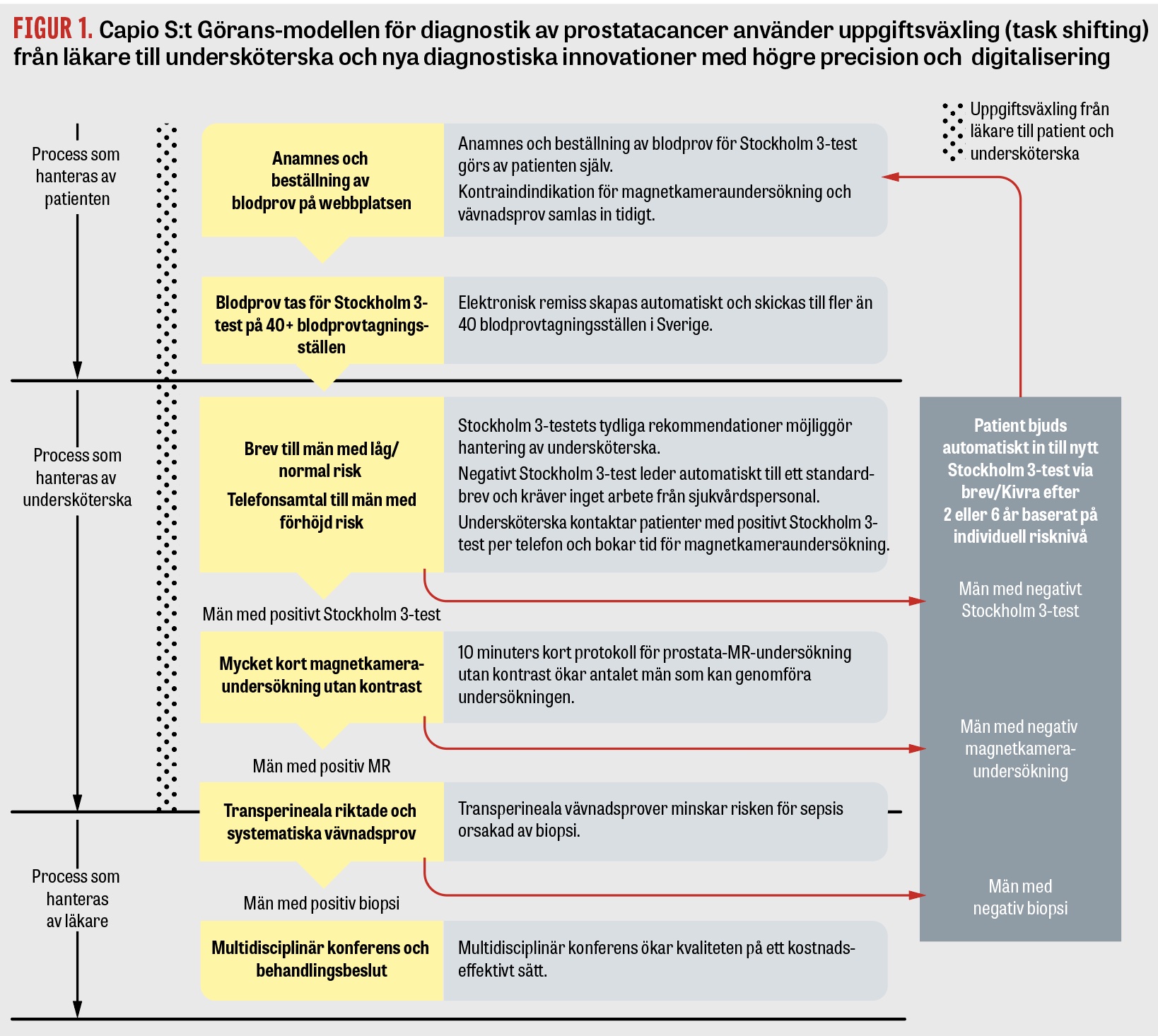
Baserat på tillgänglig kunskap har vi valt att bygga upp en diagnostisk kedja strukturerad enligt följande (Figur 1):
- Män mellan 45 och 75 år som inte tidigare diagnostiserats med prostatacancer och vill testa sig remitteras från vårdcentralen eller hänvisas till Prostatacancercentrums webbplats.
- Mannen loggar in på webbplatsen med mobilt bank-id och skapar sin remiss för provtagning. Han svarar på frågor om tidigare prostatacancerdiagnos (vilket leder till exklusion), läser information om för- och nackdelar med tidig diagnostik av prostatacancer och besvarar frågor om samsjuklighet och faktorer för analysen av Stockholm 3-testet.
- Mannen lämnar blodprov för analys med Stockholm 3-test på en av Unilabs blodcentraler. Blodprovet analyseras först för PSA. Om värdet är större än 1,5 ng/ml genomförs automatiskt en analys med Stockholm 3-test på samma blodprov. Denna reflexanalys sparar tid för patienten samtidigt som sjukvårdens kostnader minimeras. Vid kraftigt stegrat PSA (>40 ng/ml) tas patienten direkt vidare i ett snabbspår för diagnostik inom en vecka.
- Män med normalt resultat på Stockholm 3-testet får information om när uppföljande blodprov bör ske skickad hem i ett brev. Brevet genereras automatiskt och kräver inget arbete av vårdpersonal. Beroende på resultatet från PSA-prov och Stockholm 3-test rekommenderas uppföljning efter 2 eller 6 år. Journalsystemet aktiverar automatiskt en påminnelse till mannen att ta kontakt efter rekommenderat tidsintervall.
- Män med förhöjt resultat på Stockholm 3-test kontaktas av en undersköterska per telefon som bokar in dem för en 10-minuters MR-undersökning. Denna innehåller T2-viktade axiala och sagittala samt funktionella diffusionsviktade serier utan tillägg med kontrast. MR-bilderna klassificeras i enlighet med PI-RADS (Prostate imaging reporting and data system) version 2.1, och eventuella avvikelser med PI-RADS (≥3) segmenteras av radiologen i mjukvaran MIM, som används i BK Medicals ultraljudsmaskiner för MR-ledda fusionsbiopsier.
- Män med negativ MR (PI-RADS ≤2) får ett brev som informerar om resultatet och att uppföljande blodprov med Stockholm 3-test bör göras om 2 år. De får även en automatisk påminnelse om provtagning.
- Män med misstänkta förändringar på MR (PI-RADS ≥3) kontaktas av undersköterska per telefon som bokar in mannen för transperineal vävnadsprovtagning med MR-/fusionsteknik (BK Medical). Män med tumörmisstänkta fynd (PI-RADS 4‒5) genomför både riktade och systematiska vävnadsprovtagningar, medan män med mer osäkra fynd (PI-RADS 3) endast genomför riktade vävnadsprovtagningar för att minimera risken för överdiagnostik.
- Alla män som lämnat vävnadsprov diskuteras på multidisciplinär videokonferens, där beslut fattas om behandlingsrekommendation.
- Män som lämnat vävnadsprov får återkoppling av ansvarig urolog. Om vävnadsprovet är negativt ges återkoppling per telefon, men om det finns tecken på cancer eller om särskilda omständigheter föreligger ordnas ett fysiskt möte.
Medicinska resultat
Vi har sammanställt resultat från 16 maj 2018 till 31 december 2021. Av 5 439 män som testats genomgick 29 procent (n = 1 592) MR-undersökning. Som jämförelse hade 35 procent (n = 1 903) av männen ett PSA ≥3 ng/ml, vilket illustrerar att användandet av Stockholm 3-test i tillägg till PSA-prov minskar antalet MR-undersökningar.
47 procent (n = 744) av männen som genomgick MR rekommenderades vävnadsprovtagning.
Hos 56 procent (n = 414) av män med misstänkt fynd på MR identifierades kliniskt betydelsefull prostatacancer, medan endast 12 procent (n = 88) hade låggradig prostatacancer (Gleason-summa 6). Detta innebär att drygt 8 procent av männen som genomgick testning på Prostatacancercentrum fick en diagnos med kliniskt betydelsefull prostatacancer. Det finns tyvärr inga svenska studier att jämföra med.
155 män med förhöjt resultat i Stockholm 3-test hade ett negativt PSA-prov (1,5‒3 ng/ml). Av dessa hade 75 män (48 procent) en kliniskt betydelsefull prostatacancer i biopsi.
Löpande förbättringar baserade på ny forskning
Det är välkänt att transrektal vävnadsprovtagning av prostata är förknippad med en risk för urosepsis [7]. Vi har därför sedan 2019 helt övergått till transperineala vävnadsprov med lokalbedövning, vilket nu rekommenderas internationellt, och vi väntar oss att svenska riktlinjer snart gör detsamma. Vi har nu även exkluderat rutinmässig antibiotikaanvändning vid prostatabiopsi och trots detta endast registrerat 3 fall av associerad urosepsis (<0,5 procent).
I augusti 2021 presenterades resultaten från STHLM3 MR-studien med 12 750 deltagare i Lancet Oncology [3]. Baserat på dessa nya forskningsrön använder Prostatacancercentrum sedan januari 2022 Stockholm 3-test ≥15 procent som brytpunkt för vidare hantering med MR.
Kortare ledtider och bättre utnyttjande av resurser
Vi har genomfört en journalgranskning av alla män som diagnostiserats och behandlats på Capio S:t Görans sjukhus under perioden 1 januari till 31 mars 2022. Totalt har vi granskat 218 patienter, varav cirka hälften har kommit via remiss med konstaterad prostatacancer för behandling. Baserat på denna granskning kan vi jämföra ledtider, resursutnyttjande och hälsoekonomi i Capio S:t Göran-modellen med traditionell diagnostik som initierats i primärvården.
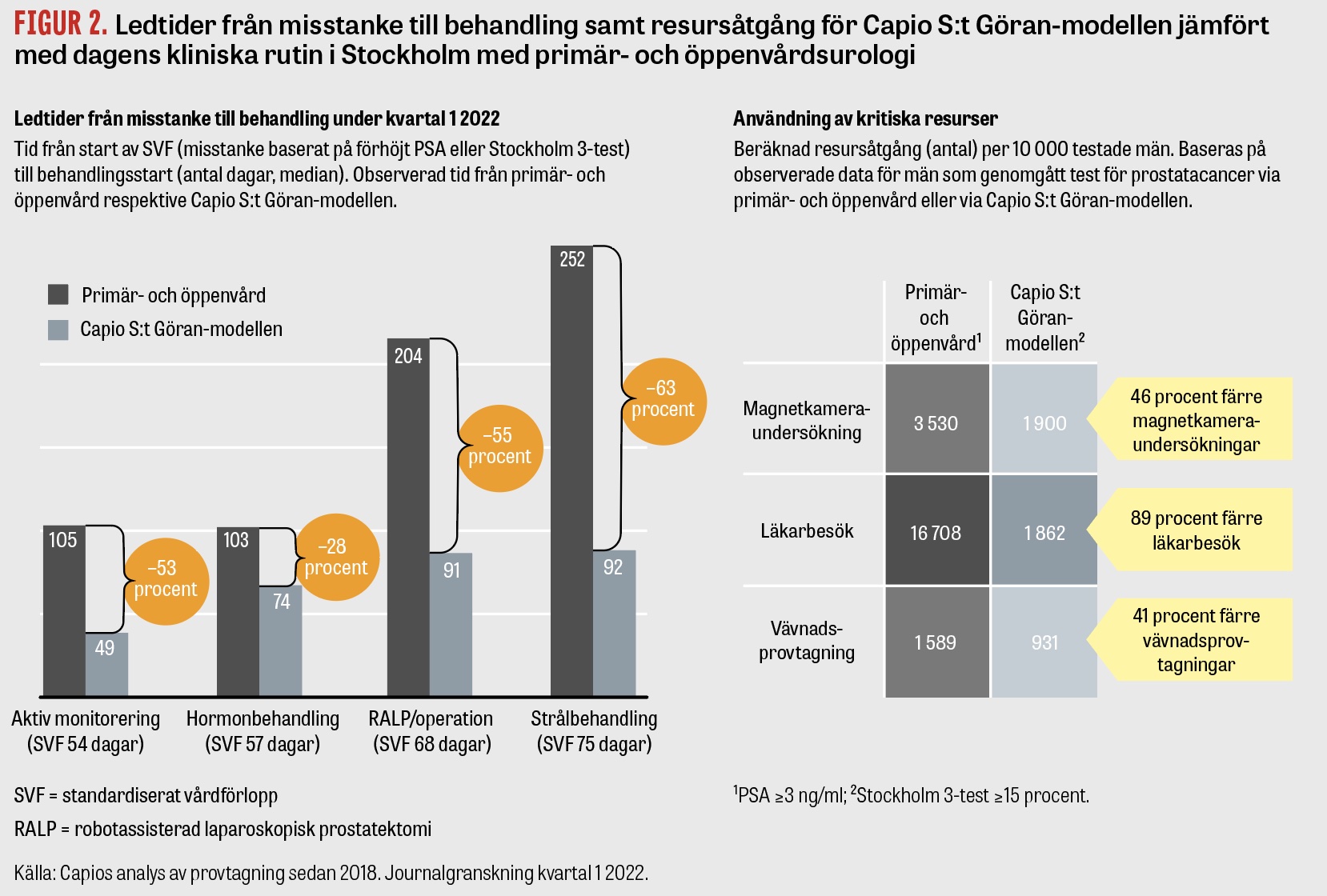
Jämfört med dagens kliniska rutin, med besök hos primärvården, urologen och sjukhus, leder Capio S:t Göran-modellen till att de genomsnittliga tiderna för standardiserade vårdförlopp, från misstanke (förhöjt PSA eller Stockholm 3-test) till behandling, minskar med 53 procent för aktiv monitorering, 28 procent för hormonbehandling, 55 procent för operation och 63 procent för strålbehandling (Figur 2). Detta återspeglar sig också i en rapport från Nationella prostatacancerregistret som jämför andelen patienter som får PAD-besked inom 11 dagar från vävnadsprovtagning. Riksgenomsnittet är 11 procent och genomsnittet för alla sjukhus i Stockholm är 17 procent, medan Capio S:t Görans sjukhus toppar listan med 57 procent [8].
Samtidigt minskade resursutnyttjandet. I en analys där vi beräknar resursbehov baserat på 10 000 testade patienter minskade resursutnyttjandet med 46 procent för MR, 89 procent för läkarbesök och 41 procent för vävnadsprovtagning i Capio S:t Göran-modellen jämfört med dagens kliniska rutin i Stockholm (Figur 2).
Capio S:t Göran-modellen sparar pengar
Det är viktigt att nya vårdprocesser förs in på̊ ett hälsoekonomiskt rimligt sätt. Vi har gjort en översiktlig hälsoekonomisk utvärdering av sjukvårdens direkta kostnader för diagnostik fram till behandlingsbeslut. Vi har utvärderat 2 olika strategier:
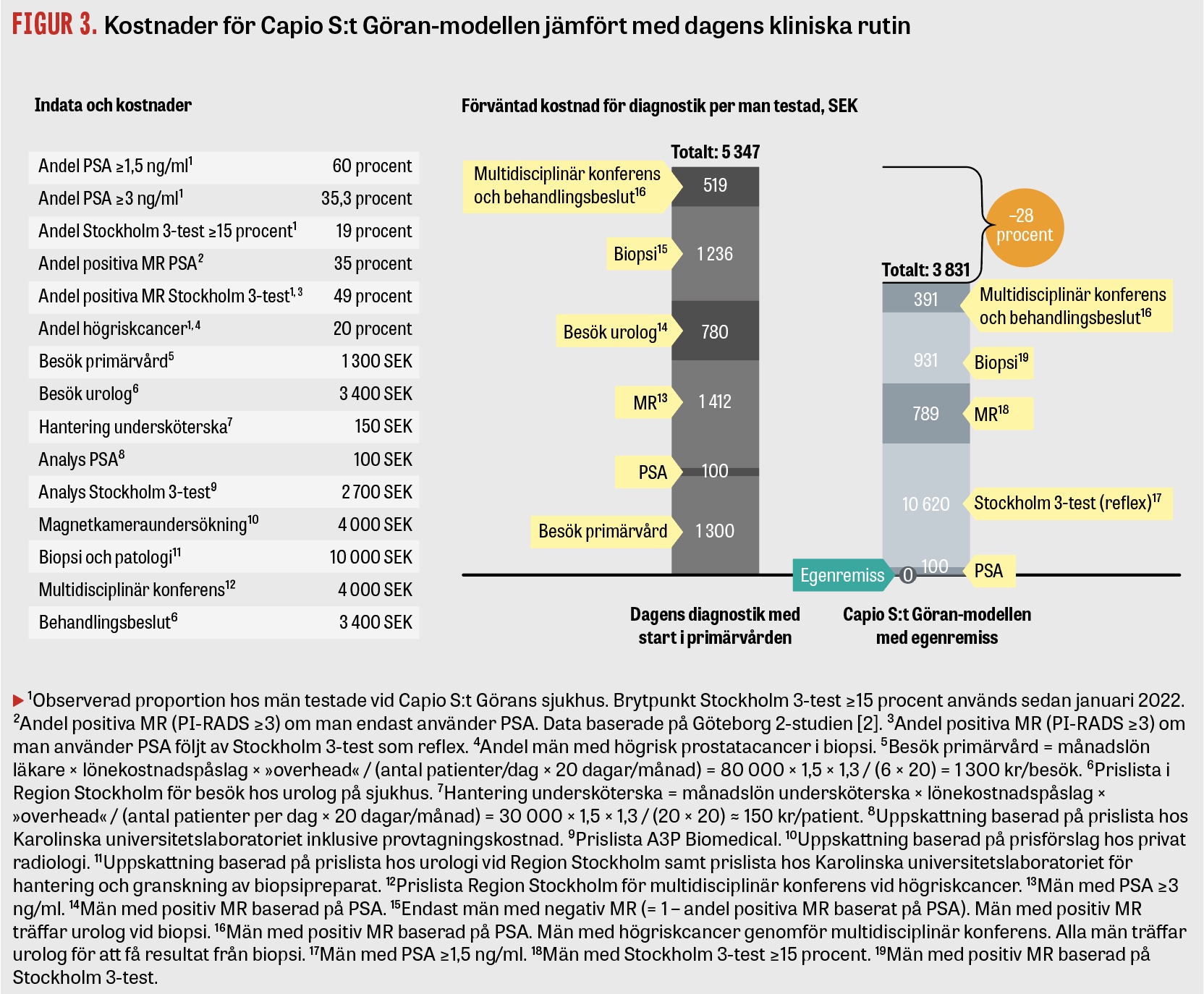
- Strategi 1 efterliknar klinisk rutin i Sverige. Vi har antagit att män med positivt PSA (≥3 ng/ml) genomgår MR. Processmässigt börjar denna strategi med att patienten träffar en allmänläkare på en vårdcentral då ett första PSA-prov tas. Patienter med förhöjt PSA (≥3 ng/ml) remitteras till MR och urolog på sjukhus följt av riktade och systematiska vävnadsprov vid positivt resultat.
- Strategi 2 är Capio S:t Göran-modellen och innebär att man tar ett Stockholm 3-test som reflex vid PSA ≥1,5 ng/ml. Män med positivt Stockholm 3-test (≥15 procent) genomgår MR. Processmässigt börjar denna strategi med att mannen själv skapar en remiss till Stockholm 3-provtagning. Logistik och administration hanteras här av undersköterskor fram till vävnadsprovtagningen.
Den hälsoekonomiska analysen indikerar att kostnaden blir lägre med Capio S:t Göran-modellen och att de diagnostiska kostnaderna kan minska med 28 procent för varje testad man jämfört med dagens kliniska rutin som utgår från primärvårdsläkaren. Skälet till att kostnaden blir lägre är att man undviker onödiga besök hos primärvårdsläkaren och urologen, onödiga MR-undersökningar och onödiga vävnadsprov (Figur 3).
Diskussion
Det finns konsensus om att tidig diagnostik i ett organiserat screeningprogram minskar dödligheten i prostatacancer, men också̊ att tidig diagnostik är förknippad med utbredd diagnostisering av ofarliga tumörer (överdiagnostik) och komplikationer orsakade av utredning och behandling (infektioner, behandlingsorsakad inkontinens och impotens). Det är därför viktigt att diagnostiken förbättras.
Vi illustrerar här en modell där mer än hälften av männen som biopseras har Gleason-summa 7, det vill säga en kliniskt betydelsefull prostatacancer, samtidigt som antalet män med liten icke-behandlingskrävande cancer är låg.
Capio S:t Göran-modellen är en av flera möjliga strategier för att förbättra diagnostiken för prostatacancer. Ett exempel är att använda PSA och MR utan tillägg av andra blodtest [2]. Ett annat exempel är den modell som införts i Region Värmlands program för organiserad prostatacancertestning, där Stockholm 3-test används som reflex för män med PSA >3 ng/ml. Ytterligare alternativ inkluderar att kombinera PSA med volymmätning av prostata (PSA-densitet) eller att använda alternativa blodprov som 4K-score, som studeras i den finska screeningstudien Proscreen. Om man överväger att införa nya verktyg i klinisk rutin menar vi att det är viktigt att det vetenskapliga stödet är tillräckligt, att resursutnyttjandet är undersökt och att en hälsoekonomisk utvärdering genomförts. Flera av de föreslagna alternativen brister fortfarande i detta.
Vården är i ständig utveckling. Vi har här visat att det i en strukturerad och sammanhållen vårdkedja är möjligt att införa viktiga förbättringar fortlöpande och på kort tid. Vi har till exempel infört digitaliserade processer med inslag av automatisering, vilket är resurssparande. Andra exempel är uppgiftsväxling (task shifting) från läkare till undersköterska, införandet av ett nytt blodprov, MR samt övergången till perineala biopsier. Våra erfarenheter visar att ett strukturerat omhändertagande av män som önskar prostatacancertestning i en sammanhållen vårdkedja, där PSA kombineras med Stockholm 3-test och MR följt av riktad perineal vävnadsprovtagning, är
- genomförbart
- förknippat med hög känslighet för att hitta prostatacancer
- leder till ett kostnadseffektivt nyttjande av sjukvårdens resurser.
Återkopplingen från patienter har spontant varit god, och de kommentarer som vi fått rör god tillgänglighet, tydliga rekommendationer och korta ledtider. Vi är också väldigt glada över efterfrågan på våra erfarenheter hos våra kollegor. Vi har sedan 2017 tagit emot över 40 svenska och utländska studiebesök, som varit mycket uppskattade.
Sammanfattningsvis har vi på Capio S:t Görans sjukhus genom uppgiftsväxling, nyttjande av nya diagnostiska innovationer med högre precision och smart digitalisering skapat ett enklare, bättre och effektivare flöde för diagnostiken, vilket har lett till lägre kostnader för huvudmannen, bättre nyttjande av kritiska resurser, tidigare upptäckt av prostatacancer, kortare vårdtid och färre biverkningar.
Läs även: Evidensbaserad screening för prostatacancer börjar ta form
Potentiella bindningar eller jävsförhållanden: Henrik Grönberg och Tobias Nordström har aktier i A3P Biomedical AB, som säljer Stockholm 3-testet.