Rapportering av misstänkta biverkningar bidrar till tidig upptäckt av nya säkerhetsrisker med läkemedel.
Spontanrapporteringssystemet har fyllt sitt syfte under pandemin, dock med stora tidsvariationer i rapporteringsgrad. Variationerna drivs av olika faktorer som nationella informationsinsatser, mediauppmärksamhet och yttre omvärldshändelser.
Underrapportering kan göra att det tar längre tid att upptäcka säkerhetsproblem och att patienter utsätts för större säkerhetsrisker än nödvändigt.
Läkemedelverket har en viktig roll i att bidra till ökad rapporteringsgrad genom regelbunden dialog med hälso- och sjukvården, riktade utbildningsinsatser och förenklade rapporteringssystem.
Syftet med spontanrapportering av misstänkta biverkningar är att tidigt upptäcka nya säkerhetsrisker med läkemedel och att minimera riskerna i klinisk läkemedelsanvändning. För att spontanrapporteringssystemet ska fungera ändamålsenligt krävs det att misstänkta biverkningar rapporteras till Läkemedelsverket. Av yttersta vikt är därför att berörda myndigheter, i nära samverkan med bland annat regionerna, arbetar för att hitta effektiva och hållbara rapporteringssystem som ytterst syftar till att läkemedel som används ska vara säkra och effektiva.
Erfarenheter från covid-19-vaccinationen
Det är välkänt att det finns en stor underrapportering av misstänkta biverkningar [1, 2]. Åren före covid-19-pandemin fick Läkemedelsverket in cirka 8 000 spontanrapporter per år. År 2021 var motsvarande siffra 100 000. Den absoluta majoriteten av rapporterna handlade om misstänkta biverkningar av vaccin mot covid-19. När rapportinflödet var som störst, det vill säga i mars 2021, tog Läkemedelsverket emot drygt 20 rapporter per 1 000 givna vaccindoser och vecka. Från kliniska studier av vaccinerna mot covid-19 är det känt att 80–90 procent av de vaccinerade drabbas av lindriga biverkningar. Författarna förutsätter därmed att det föreligger en stor underrapportering även för dessa vacciner. Några av anledningarna bakom underrapporteringen kan vara tidsbrist, glömska samt okunskap kring vad som ska rapporteras och hur rapporteringen genomförs. Här har Läkemedelsverket en viktig roll i att utbilda rapportörer om syftet och nyttan med spontanrapportering samt att underlätta själva rapporteringen.
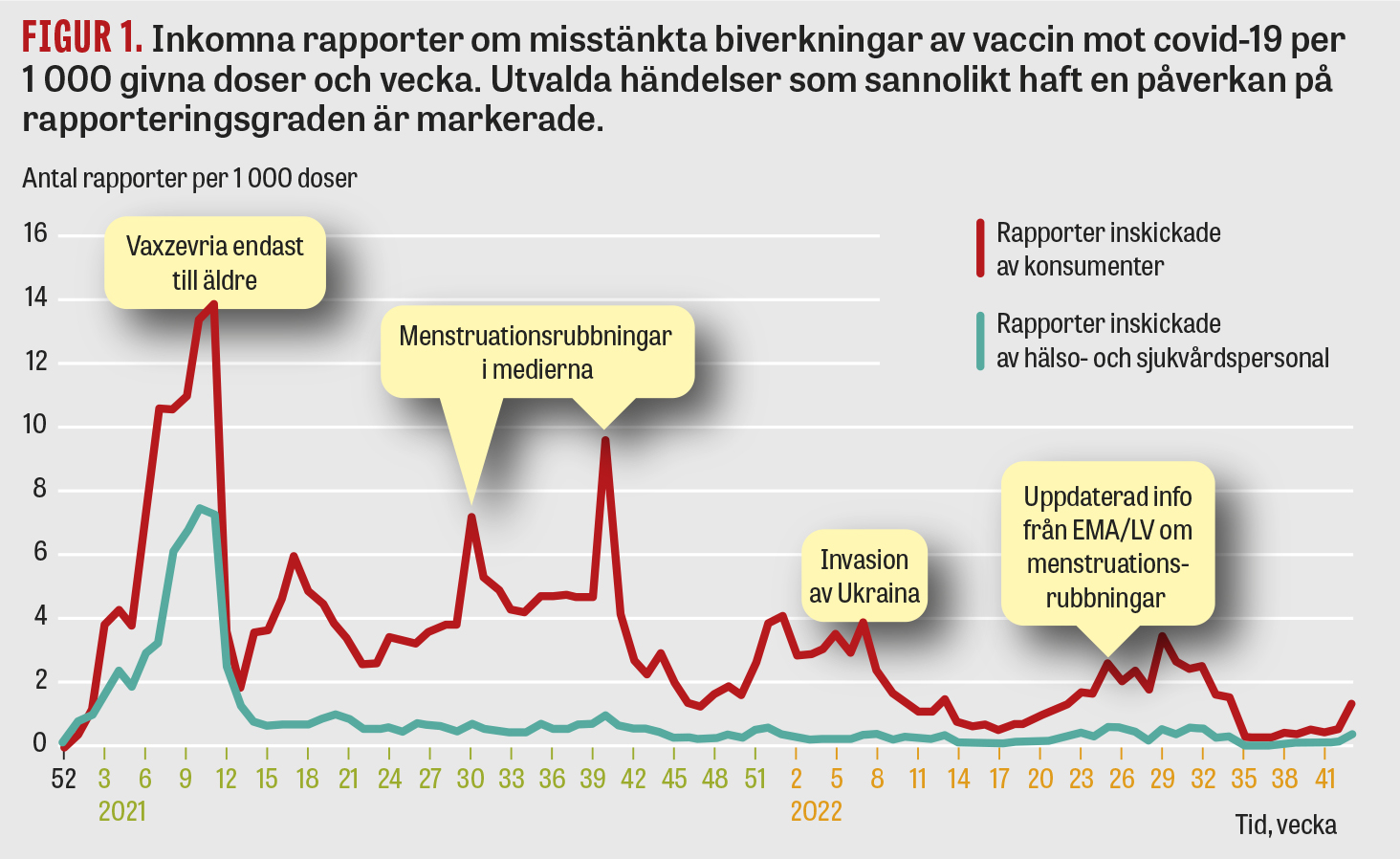
Läkemedelsverket identifierade tydliga tidsvariationer i rapportinflöde kopplade till exponeringsgrad, inte minst från konsumenter (Figur 1). Rapporteringstoppar ses bland annat i samband med de regulatoriska utredningarna av trombotiskt trombocytopent syndrom (TTS) för Vaxzevria [3] och menstruationsrubbningar efter vaccination mot covid-19 [4]. Benägenheten att rapportera kan sannolikt ha påverkats positivt av att den europeiska läkemedelsmyndigheten (EMA) och Läkemedelsverket (LV) i ett tidigt skede, gick ut och uppmuntrade till rapportering av samtliga misstänkta biverkningar med en koppling till covid-19. Det stora medieintresset för vaccinbiverkningar och säkerhetsuppföljning samt historiken kring narkolepsi och Pandemrix har sannolikt ytterligare bidragit till en högre rapporteringsgrad.
På motsvarande sätt sjönk i stället rapporteringsgraden i samband med att Ryssland invaderade Ukraina i februari 2022, då medierapporteringen ögonblickligen skiftade fokus. Man kan spekulera om huruvida invasionen utgör ett bakgrundsbrus som stör rapportering eller om medborgare prioriterat ned sina symtom i kontexten av oro för omvärldsläget. Oavsett vilket är det viktigt att komma ihåg att spontanrapportering bygger på egna initiativ och att dessa i sin tur påverkas av olika faktorer som är svåra att förutse. Databaser över misstänkta biverkningar har med andra ord, sitt viktiga syfte till trots, även sina inneboende begränsningar, till exempel att de inte utgör en källa för frekvensuppskattningar. Här har Läkemedelsverket ett viktigt utbildningsuppdrag, det vill säga att visa vilka slutsatser som kan dras från olika datakällor.
Konsumenter har haft möjlighet att rapportera misstänkta biverkningar till Läkemedelsverket sedan år 2008. Konsumentrapporter utgör ett viktigt komplement till rapporter från hälso- och sjukvården. Dels ses många lindriga händelser aldrig av professionen, dels kan konsumenter bidra med detaljeringsgrad och ett annat perspektiv, det vill säga den egna upplevelsen av det inträffade [5].
Drygt 10 procent av rapporterna om misstänkta biverkningar av vaccin mot covid-19 har bedömts som allvarliga av rapportören. Dessa har löpande prioriterats för hantering av Läkemedelsverket, då sannolikheten där är som störst för att hitta nya säkerhetsrisker som bör leda till förändrade rekommendationer på gruppnivå. Att allvarliga rapporter skyndsamt har kunnat hanteras och tillgängliggöras för signalspaning har bedömts som nödvändigt för upprätthållande av en god kvalitet på den regulatoriska säkerhetsuppföljningen.
Säkerhetsuppföljning efter godkännande är helt avgörande för att ytterligare förstå ett läkemedels säkerhetsprofil. Läkemedel följs genom hela sin livscykel, och kliniska studier pågår långt efter marknadsgodkännande. Exempel på mycket sällsynta biverkningar av vaccin mot covid-19 som upptäckts i spontanrapporteringen är TTS och myokardit. Spontanrapportering är med andra ord en viktig källa för signaldetektion, men behöver kompletteras med andra datakällor, såsom kliniska och epidemiologiska studieresultat, för vidare analys av orsakssamband och riskfaktorer.
Med lärdom från Pandemrix-vaccinationerna, där vikten av att kunna genomföra epidemiologiska studier blev tydlig [6], har Läkemedelsverket inom sitt forskningsuppdrag upprättat en ny databas över landets vuxna befolkning med uppgifter om bland annat vaccinationer mot covid-19 och hälsoutfall. Databasen består av information på individnivå med personnummer och uppdateras regelbundet med uppgifter från olika hälsodataregister [7]. Genom att koppla exponeringsdata från Nationella vaccinationsregistret till information från andra register skapas utökade möjligheter till detektion och epidemiologisk utvärdering av misstänkta biverkningar efter vaccination mot covid-19. Forskare som vill göra liknande studier behöver, utöver godkännande från Etikprövningsmyndigheten, också få tillstånd från den registerhållare från vilken data har hämtats. Läkemedelsverket har genom detta arbete kunnat bidra med underlag både till andra nationella myndigheter och till det EU-gemensamma säkerhetsarbetet, vilket i sin tur hjälpt oss att ytterligare karaktärisera covid-19-vaccinernas säkerhetsprofiler [8]. Samhällsnyttan av frekvent uppdaterade hälsodataregister är med andra ord tydlig och svår att ifrågasätta.
Slutsats
Läkemedelsverket ser en regelbunden och öppen dialog med hälso- och sjukvården och allmänheten som avgörande för en välfungerande spontanrapportering och en patientsäker läkemedelsanvändning. Under pandemin har Läkemedelsverkets mål varit att ge saklig information för att underlätta ställningstagande till vaccination för individen. Läkemedelsverket har också, redan i ett tidigt utredningsskede, velat uppmärksamma hälso- och sjukvården på symtom som kan vara tecken på vaccinbiverkningar där det är viktigt att uppmana till skyndsam vårdkontakt. För att uppnå en god följsamhet till myndigheternas råd och rekommendationer krävs etablerade och tillförlitliga kanaler för informationsöverföring och dialog. Samordning och vidareutveckling av nationella producentobundna kunskapsstöd är avgörande för en effektiv och trovärdig kunskapsöverföring, och det arbetet behöver prioriteras, vilket bland annat lyfts fram i Läkartidningen [9]. Att genom tidig informationsöverföring bidra till ett bättre kunskapsläge hos behandlande kliniker ökar sannolikt också benägenheten och motivationen att rapportera misstänkta biverkningar.
Läkemedelsverket har ett önskemål om att kunna ge tydligare återkoppling från säkerhetsarbetet med läkemedel till våra rapportörer. Eftersom Läkemedelsverket inte rutinmässigt genomför sambandsbedömningar på fallnivå är det inte möjligt att ge återkoppling på varje individuell rapport, annat än en bekräftelse på att den mottagits. Däremot planerar myndigheten för en öppen databas med aggregerade sökbara data om misstänkta biverkningar för samtliga läkemedel. Läkemedelsverket har också ett starkt önskemål om en utökad dialog med regionerna för att bättre förstå behoven och hur vi tillsammans kan arbeta för säkra och effektiva läkemedel för våra patienter.
Avslutningsvis kan vi konstatera att spontanrapporteringssystemet har fyllt sitt syfte under vaccinationsinsatsen mot covid-19, det vill säga att nya säkerhetsrisker med vaccinerna har kunnat upptäckas tidigt och åtgärder vidtas. För att spontanrapporteringen ska fortsätta vara ett värdefullt verktyg i jakten på nya signaler behöver myndigheter, regioner och övriga aktörer, i nära samverkan, utarbeta hållbara rapporteringssystem och kommunikationsvägar som möter våra olika behov. Till exempel borde strukturerad information som dokumenteras i journalsystemet kunna användas för automatisk generering av biverkningsrapporter. Författarna utgår från att automatiserad överföring av rapporterna från den hårt belastade hälso- och sjukvården till Läkemedelsverket är en förutsättning för en hög rapporteringsgrad. Den största framgångsfaktorn här är samverkan, det vill säga att skapa aktörsgemensamma nätverk och att inom dessa identifiera incitament och behov för rapporteringssystem och kanaler för återkoppling samt att driva utveckling utifrån behoven. Till syvende och sist värnar vi tillsammans en god folkhälsa och säkra och effektiva läkemedelsbehandlingar.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.