Vaskulära lesioner är vanliga och drabbar upp till 10 procent av alla spädbarn [1, 2]. Lesionerna indelas i tumörer, som är vanliga, och missbildningar, som är relativt ovanliga. Att förstå, och kunna tillämpa, den moderna klassificeringen av vaskulära lesioner är grundläggande för att man ska kunna ställa rätt diagnos och ge patienten rätt behandling. Grunden i diagnostiken av vaskulära lesioner är anamnes och status. En studie från ett kärlteam i USA visade att ungefär hälften av de inremitterade barnen hade fått fel diagnos av den inremitterande läkaren och att de i många fall därför också hade fått fel behandling [3].
I denna ABC-artikel får läsaren vägledning för att kunna skilja banala tillstånd från potentiellt komplicerade och kunskaper för att kunna bedöma när vidare utredning eller bedömning hos kärlteam är indicerad och för att översiktligt kunna informera om prognos och förväntat förlopp. Fokus ligger på infantila hemangiom, eftersom de är den vanligaste lesionen man träffar på om man inte arbetar i ett kärlteam.
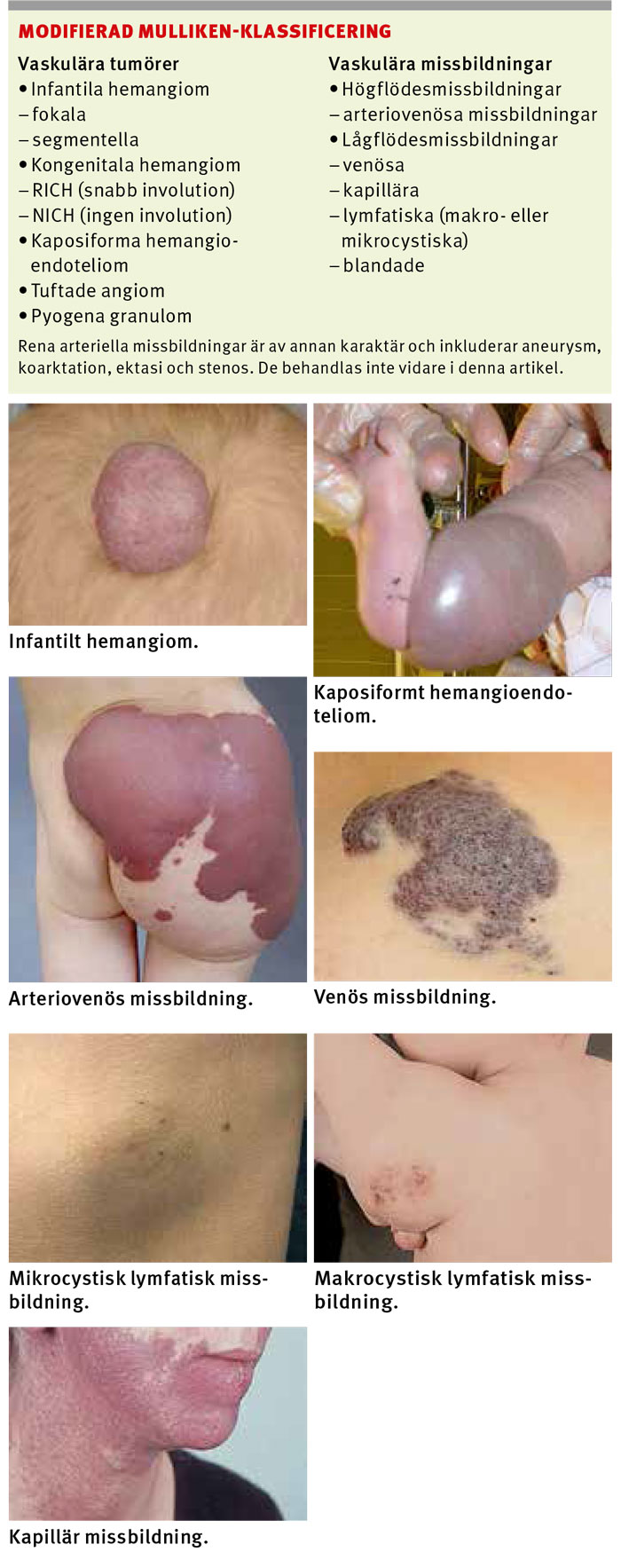
Klassificering av vaskulära lesioner
Lesionerna indelas i tumörer, med endotelproliferation, och missbildningar, utan endotelproliferation [4]. Missbildningarna indelas vidare i undergrupper beroende på flödeskarakteristika och kärltyp i missbildningen [5].
Den vanligaste tumörformen är infantilt hemangiom, en godartad barntumör som ofta växer snabbt postnatalt och går i långsam regress under barndomen. Vaskulära missbildningar består av onormalt bildade kanaler klädda med kärlendotel. Även om de alltid är kongenitala, är de inte alltid uppenbara vid födseln. Missbildningarna går i regel inte i regress.
Trots att klassificeringen antogs av International Society for the Study of Vascular Anomalies (ISSVA) 1996 används fortfarande ofta äldre terminologi för kärllesioner [3, 6]. Det kan leda till att barnen får felaktig behandling och föräldrarna felaktig information om vad de kan förvänta sig [3].
Kärltumörer
Infantila hemangiom
Infantila hemangiom drabbar upp till 10 procent av spädbarn [2]. Tumören är vanligare hos flickor än hos pojkar (3–9:1), vid prematuritet och låg födelsevikt (<1 500 gram), vid flerbörd och vid hög maternell ålder [7]. Cirka 20 procent av de drabbade barnen har mer än en lesion [2]. Då det finns mer än fem kutana hemangiom benämns tillståndet hemangiomatos, vilket föranleder palpation av buk och utredning med ultraljud för att utreda förekomst av intrahepatiska/intraabdominella hemangiom. Etiologin och patofysiologin är okända, men teorier om hypoxisk stress, placentaanomalier och hudtrauma i födslokanalen har framkastats [2, 8]. Infantila hemangiom anses inte vara ärftliga [9].
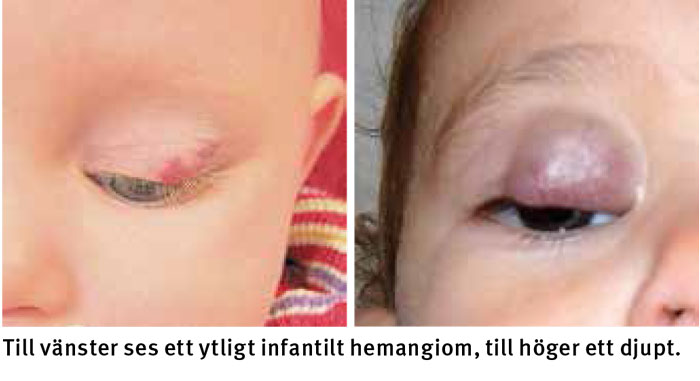
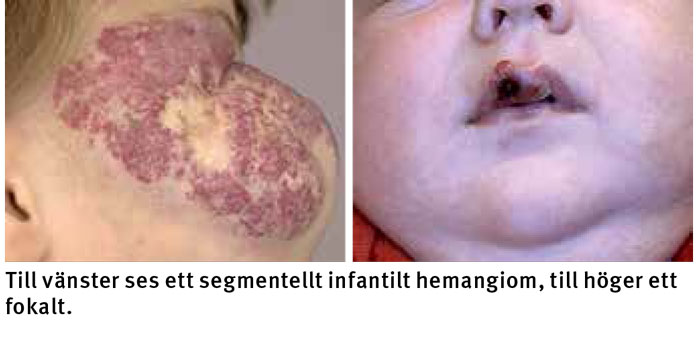
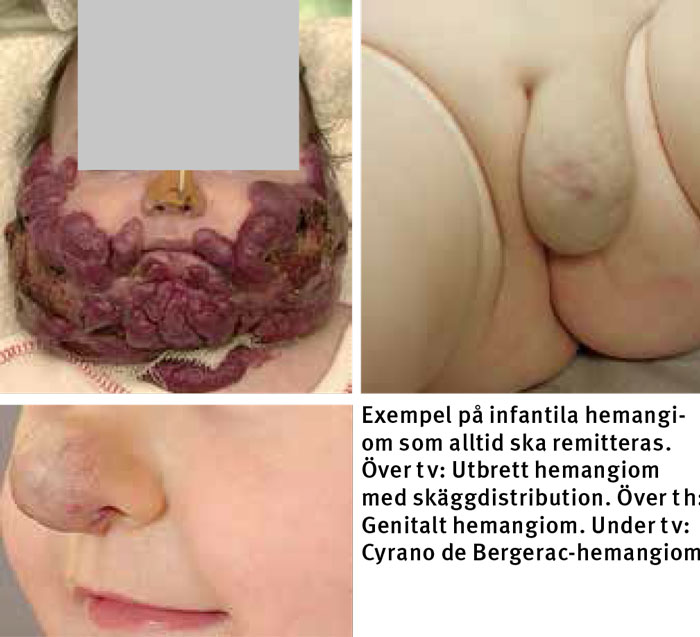
Infantila hemangiom kan vara djupa (subkutana) eller ytliga (kutana) eller både och, och de indelas i två subtyper: fokala och segmentella. Fokala hemangiom har ett begränsat, samlat fokus, medan de segmentella är utbredda och följer Blaschkos linjer [10]. Utbredningen kan ge information om prognos och inge misstanke om association till syndrom.
De flesta infantila hemangiom utvecklas under de första veckorna efter födseln, och alla under det första levnadsåret [11]. Lesioner som uppstår senare är aldrig infantila hemangiom, utan annan lesion måste misstänkas. Typiskt växer hemangiomen snabbt de första 3–6 månaderna och når sedan en platåfas och blir stationära. Den maximala storleken är i de allra flesta fall uppnådd senast vid 9 månaders ålder, dock med relativt stor variation.
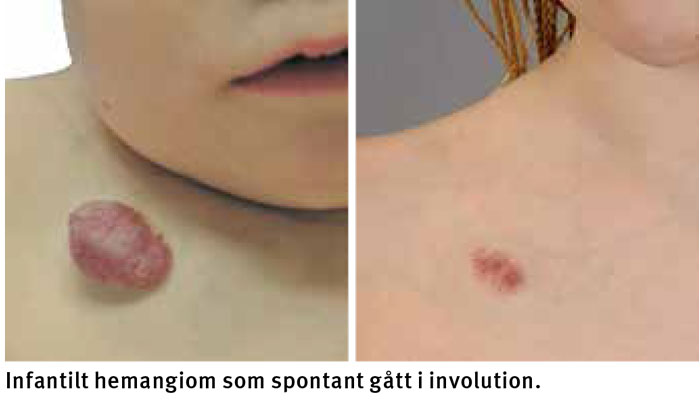
Involutionen börjar sedan typiskt omkring 1 års ålder [11]. Involutionshastigheten är relativt konstant, och ungefär 50 procent av storleken har gått i involution vid 5 års ålder och ca 70 procent vid 7 års ålder [10]. De tidigaste tecknen på involution är färgförändring; färgen bleknar från klarröd till en mer dov färg, och en gråvit hätta kan utvecklas i mitten av lesionen. Denna sprids sedan mot periferin. Lesionens spänning minskar först och därefter börjar volymen bli uppenbart mindre [12].
Medfödda hemangiom
Medfödda hemangiom är ovanliga, och de är biologiskt sett inte släkt med infantila hemangiom [13]. Det diskuteras om medfödda hemangiom är en variant av infantila hemangiom eller ett helt separat tillstånd. Medfödda hemangiom har ett annat naturalförlopp än de infantila. Deras tillväxtfas är intrauterin, och de är färdigutvecklade vid födseln. Därefter uppvisar de antingen en accelererad involution (RICH [rapid involuting congenital hemangioma]), som ofta är komplett före 1 års ålder, eller ingen involution alls (NICH [non-involuting congenital hemangioma]).
Pyogena granulom (telangiektatiska granulom)
Pyogent granulom är ett inflammatoriskt, hyperplastiskt tillstånd, med proliferativ vaskulär vävnad, som kan uppstå under hela livet. Kliniskt ser förändringen ut som en papel eller polyp, med glansig yta, som blöder mycket lätt. Den uppstår oftast på ett ställe där det finns en preexisterande skada. Vanliga lokaler är tandköttet, läpparna, näsmukosan, ansiktet och fingrarna. Pyogena granulom utvecklas snabbt under några veckor till maximal storlek, och på grund av den snabba utvecklingen misstas de ibland för maligniteter. Vid osäkerhet bör alltid histopatologisk undersökning göras.
I enstaka fall kan pyogena granulom tillbakabildas, men oftast krävs aktiv behandling [14]. De är vanliga vid kapillära missbildningar [15].
Ovanliga kärltumörer
Kaposiforma hemangioendoteliom
Kaposiforma hemangioendoteliom är ovanliga, lokalt aggressiva kärltumörer med potential till invasiv växt. Tumören kan växa in i ben, muskler och lymfkörtlar samt lokal viscera, men distansmetastaser har aldrig rapporterats [16]. Den uppstår oftast före 2 års ålder som en röd eller violett fläck, som raskt växer och infiltrerar. Tumören är dessutom vanlig hos personer som insjuknat i aids [7]. Tumörinväxt kan leda till akut andningssvikt, hemotorax, ikterus, gastrointestinalt hinder, retroperitoneal tumörväxt och svår trombocytopen koagulopati (Kasabach–Merritt-fenomen). Dödligheten i Kasabach–Merritt-fenomen är ca 30 procent.
Diagnosen ställs med hjälp av biopsi (positivt för CD31, CD34, podoplanin och PROX1, negativt för GLUT-1) och MR. Kaposiforma hemangioendoteliom går aldrig spontant i involution och behandlas vanligen med excision och/eller cytostatika [16].
Tuftade angiom
Tuftade angiom är ovanliga benigna tumörer av okänd patogenes. Cirka 25 procent är medfödda, och 50 procent uppstår under barndomen, oftast de första levnadsåren. I de återstående 25 procenten av fallen uppstår tumören i vuxen ålder, ofta i samband med graviditet. För att ställa diagnosen krävs biopsi, där man ser diagnostiska »kanonkulor« (cannon-balls). Tuftade angiom har en långsammare tillväxtfas än infantila hemangiom, och den kan fortgå under flera år.
Av medfödda tuftade angiom går ca 95 procent i involution innan barnet fyllt 2 år. Bland de övriga går ca 15 procent så småningom i involution. Tumören kan kompliceras av Kasabach–Merritt-fenomen. Behandlingen är densamma som för kaposiforma hemangioendoteliom [17].
Maligna differentialdiagnoser
Maligna differentialdiagnoser till kärltumörer inkluderar hemangiopericytom, Wilms tumör, rabdomyosarkom, fibrosarkom, nasala gliom, retinoblastom och leiomyosarkom. Vissa av dem kan kliniskt se ut precis som infantila hemangiom, särskilt då de sitter subkutant [18]. Malign diagnos bör misstänkas när förändringen inte följer den anamnes och det förlopp som är typiskt för infantila hemangiom eller kärlmissbildning.
Kärlmissbildningar
Kärlmissbildningar är kongenitala, och naturalförloppet är att de växer med individen och finns kvar hela livet. Tonårens hormonella förändringar kan orsaka tillväxt. Ibland uppstår smärtsamma tromboflebiter med efterföljande fleboliter (förkalkade tromber) i missbildningarna. Kärlmissbildningar är lika vanliga hos flickor som pojkar. Patogenesen är oklar, men missbildningarna uppstår troligen under kärlutvecklingen, dvs under antingen vaskulogenesen eller angiogenesen [8]. De flesta kärlmissbildningar anses inte vara ärftliga, men några ovanliga nedärvda former har observerats [9].
Venösa kärlmissbildningar
Venösa missbildningar är ofta mjuka, komprimerbara, blåa förändringar. Den blåa färgen är patognomon och orsakas av missbildade små och mellanstora vener, oftast i dermis eller subkutis men ibland även i muskler och skelett. Typiskt ändrar förändringen volym vid tryckändring, t ex då patienten lutar sig framåt, vid skrik/affekt eller fysisk aktivitet.
Venösa missbildningar är oftast mer voluminösa och utbredda än de först synes vara och engagerar ofta såväl hud och subkutis som muskler; ibland finns också viscerala lesioner. Genom lesionernas svullnad kan underliggande skelett bli deformerat [19]. Histopatologiskt består venösa missbildningar av oregelbundna, endotelbeklädda kärlkanaler. Kanalernas väggar är tunna och saknar glattmuskelceller. Missbildningarna kan tillväxa vid trauma och under puberteten då de stimuleras av hormoner. I analogi med detta kan de även tillväxa vid t ex p-pillerbruk, graviditet och klimakterium [20].
Glomovenösa kärlmissbildningar skiljer sig till viss del kliniskt och histopatologiskt från venösa missbildningar. De är fastare och mindre komprimerbara, har en mer blåviolett färg och kiselstensaktig yta. De är ofta mer smärtsamma än vanliga venösa missbildningar. De behandlas på samma sätt som venösa, men svarar på ett lite annorlunda sätt. Skleroterapi är ofta mindre effektiv, och kompressionsbehandling kan ge mycket obehag. Histopatologiskt har förändringen odifferentierade muskelceller, glomusceller [21].
Kapillära kärlmissbildningar
Kapillära missbildningar kallas även portvinsfläckar, naevus flammeus, eldsmärke, »angel’s kiss« eller storkbett, beroende på vilken undergrupp de tillhör, och drabbar ca 3 av 1 000 födda barn. Ibland misstas dessa initialt för blåmärken eller födslotrauma. Hos barn är de ofta ljusröda makulor som i många fall mörknar, blir mer violetta, tjockare och ibland hyperkeratotiska med åren. Då förändringen sitter i ansiktet följer den ofta nervus trigeminus utbredningsområde [19]. Kapillära kärlmissbildningar är bristfälligt innerverade och kan växa hela livet.
Ibland är de associerade med andra missbildningar, såsom andra kärlmissbildningar (ofta lymfatiska), ben- eller mjukdelshyperplasi eller -atrofi, neurologiska defekter och spinal dysrafism. Riktlinjer för när vidare utredning med t ex MR, slätröntgen och lymfskintigrafi (med tanke på andra missbildningar) är indicerad saknas och får avgöras från fall till fall [19].
Lymfatiska kärlmissbildningar
Lymfatiska kärlmissbildningar sitter oftast (i 90 procent av fallen) i huvud-, hals- eller axillregionen och indelas i makrocystiska och mikrocystiska förändringar. Lymfatiska missbildningar kan vara lokaliserade eller diffusa och uppstår vid fel i lymfangiogenesen [8].
De vanligaste är cervikala makrocystiska lymfatiska kärlmissbildningar, tidigare kallade cystiska hygrom, som klassiskt uppstår i halsens posteriora triangel. Dessa ses typiskt redan vid födseln. Histologiskt och radiologiskt ses stora cystiska hålrum klädda med bristfälligt glattmuskelcellslager i ett tunt endotel.
Mikrocystiska förändringar upptäcks ofta inte förrän en komplikation, t ex infektion eller blödning, gör dem uppenbara genom påtaglig svullnad. Mikrocystiska förändringar ser ofta ut som en samling tunnväggiga vesiklar eller hyperkeratotiska papler som är organiserade i oregelbundna grupper [19].
Lokala lymfatiska missbildningar exacerberar och blir större på grund av hormonella faktorer, lokal eller generell inflammation/infektion och trauma [19]. Sekundära fenomen till lymfatiska missbildningar inkluderar angiokeratom, som ses som små mörklila makulor, med keratotiskt lättblödande epitel i huden, eller som vätskande lymfatiska vesikler i hud och slemhinna. Dessutom finns diffusa lymfatiska missbildningar som orsakas av hypoplasi av lymfsystemet och då kallas primära lymfödem. Kliniskt är gränsdragningen däremellan inte alltid helt självklar. Primära lymfödem handläggs inte av kärlteam och behandlas därför inte vidare i denna artikel.
Arteriovenösa kärlmissbildningar
Arteriovenösa missbildningar består av dysmorfiska arteriella och venösa kärl där mellanliggande kapillärbädd saknas, vilket medför kontinuerlig shuntning, AV-fistel, på grund av bristfällig kontroll i den prekapillära sfinktern eller avsaknad av sfinkter. Det första segmentet av dilaterad ven efter sammankopplingen kallas nidus. Det sker en konsekutiv hypertrofi av nidus, venös dilatation och arteriell hypertrofi, och arteriovenösa kärlmissbildningar kan därför leda till hjärtsvikt [19].
Schobinger-klassifikationen för arteriovenösa kärlmissbildningar utgår från den kliniska allvarlighetsgraden och beskriver stadium I som en stillsam röd makula som så småningom övergår i stadium II med karakteristiskt bultande smärta. I stadium III tillkommer ulceration, nekros och spontana blödningar med mycket kraftig stråle och i stadium IV dessutom kardiell inkompensation.
Arteriovenösa missbildningar är vanligast i huvud–halsregionen, vilket kan förklaras av att de förmodligen bildas tidigt under embryogenesen då embryot består av främst cefala strukturer [19].
Blandade (kombinerade) kärlmissbildningar
Förutom de arteriovenösa högflödesmissbildningarna finns olika blandade lågflödesmissbildningar och blandade låg- och högflödesförändringar.
Omhändertagande
Ibland är diagnossättning komplicerad när anamnes och klinisk bild inte följer de typiska, ovan beskrivna mönstren. Vanligast är att djupa infantila hemangiom utan kutan komponent förväxlas med venösa eller lymfatiska kärlmissbildningar och på så vis kan leda till felaktig diagnos, prognos och behandling. I tveksamma fall eller vid behandlingssvikt kan förutom utredning med ultraljud och/eller MR även biopsi vara vägledande. Remiss till kärlteam för diagnos och behandlingsförslag kan bli aktuell.
För korrekt diagnos och omhändertagande av patienterna krävs teamarbete och kombination av flera olika behandlingsmodaliteter och specialiteter. I de flesta länder handläggs i dag kärllesioner i multidisciplinära team, och många av teamen träffas vartannat år och diskuterar forskning och utveckling inom fältet under det internationella mötet International Workshop for the Study of Vascular Anomalies (http://www.issva.org) [22].
I Malmö bildades det multidisciplinära kärlteamet i början på 1990-talet och består av dermatolog, plastikkirurg, barnläkare och interventionell radiolog. Som konsulter finns även ögonläkare, öron-, näs- och halsläkare, kärlkirurger, handkirurg, barnortoped, barnkirurg, kurator, sjukgymnast och arbetsterapeut. Teamet träffas regelbundet varannan vecka, och möjlighet till konsultation via videokonferens finns.
De olika kärlteamen i Sverige och övriga Norden samarbetar tätt kring dessa patienter, och svårare fall diskuteras regelbundet på nordiska möten med Nordic Society for Vascular Anomalies (NSVA) (http://www.nsva.no) och vartannat år på de internationella mötena med ISSVA.
Övriga kärlteam i Sverige finns vid Akademiska sjukhuset i Uppsala, Karolinska universitetssjukhuset i Stockholm och Sahlgrenska universitetssjukhuset i Göteborg.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.