De flesta är ense om att
- Cushings syndrom är en allvarlig åkomma med kraftigt ökad morbiditet och mortalitet samt nedsatt livskvalitet
- vid klinisk misstanke om Cushings syndrom bör biokemisk utredning göras med antingen kortisol i dygnsurin, dexametasonhämningstest eller salivkortisol vid sänggåendet
- ökad risk för kardiovaskulär sjukdom, hjärtinfarkt, stroke och venös tromboembolism samt neuropsykiatriska besvär kvarstår efter behandling av Cushings syndrom
Åsikterna går isär vad gäller
- hur patienter med Cushings syndrom ska följas upp efter behandling på ett optimalt sätt.
Endogent Cushings syndrom orsakas av kronisk överproduktion av kortisol. De vanligaste orsakerna till Cushings syndrom är ACTH-producerande hypofysadenom (Cushings sjukdom), kortisolproducerande binjureadenom och ektopiskt ACTH-producerande tumörer (ektopiskt Cushings syndrom). Betydligt vanligare än endogent Cushings syndrom är exogent Cushings syndrom, det vill säga patienter som utvecklar samma kliniska bild på grund av långvarig suprafysiologisk kortisonbehandling. Andra vanliga orsaker till ökade kortisolhalter som inte beror på endogent Cushings syndrom är alkoholism, svår fetma, ångest och depression, vilka går under samlingsbegreppet pseudocushingssyndrom [1]. Vidare är lindrig autonom hyperkortisolism (tidigare kallat subkliniskt Cushings syndrom) relativt vanlig bland patienter med binjureincidentalom [1]. Denna artikel kommer dock endast att avhandla den endogena formen av syndromet.
Cushings syndrom åtföljs av en hög förekomst av allvarliga följdsjukdomar och hög dödlighet. Det är därför viktigt att skyndsamt utreda patienter med misstänkt Cushings syndrom och när diagnosen är bekräftad snabbt erbjuda effektiv behandling.
Epidemiologi
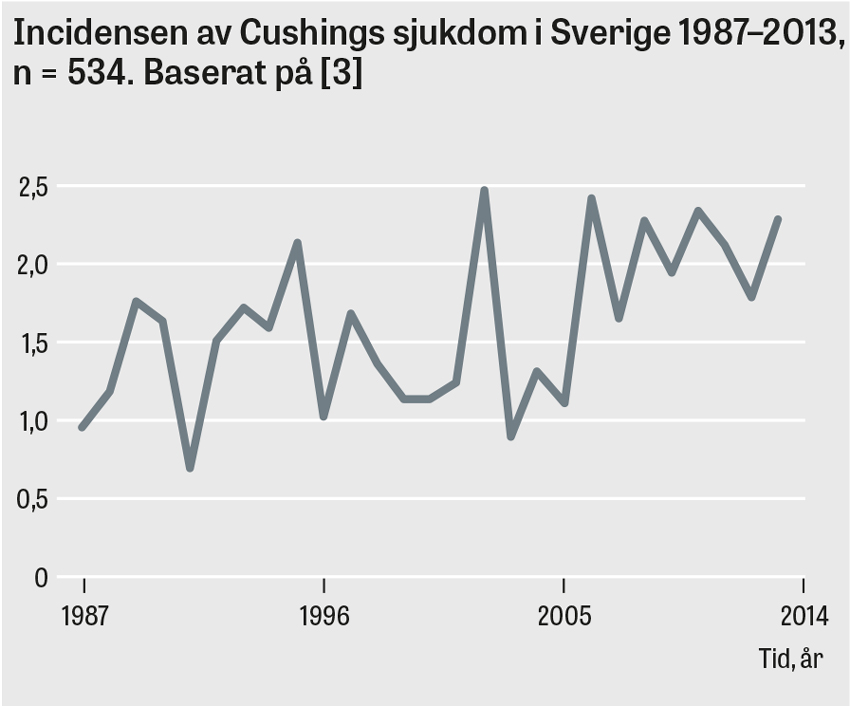
I en nyligen publicerad studie från västra Sverige var den totala incidensen av Cushings syndrom 3,2 patienter per miljon och år [2]. Detta innebär att det i Sverige diagnostiseras drygt 30 patienter med endogent Cushings syndrom årligen, varav hälften har Cushings sjukdom, en fjärdedel har binjureorsakat Cushings syndrom och en fjärdedel har ektopiskt ACTH-producerande tumörer; vanligast av de senare är maligna lungtumörer och neuroendokrina pankreastumörer. En aktuell svensk studie visade högre incidens av Cushings sjukdom i Sverige under åren 2005–2013 jämfört med 1987–2004 [3]. Om detta återspeglar en sann ökning av sjukdomen eller ökad medvetenhet är oklart.
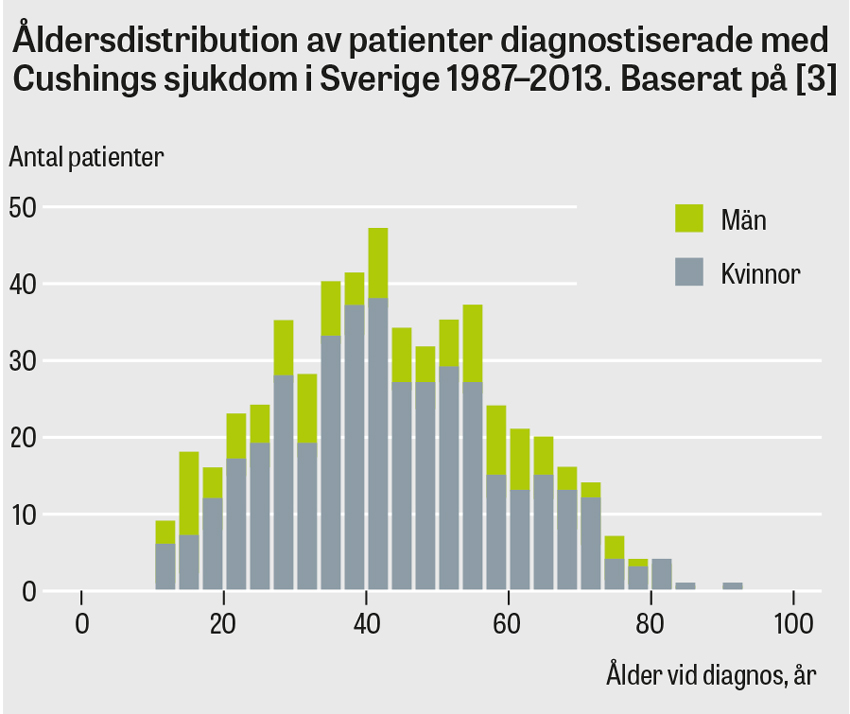
Majoriteten av alla som drabbas av Cushings sjukdom och kortisolproducerande binjureadenom är kvinnor. Sjukdomarna diagnostiseras oftast i 25–50-årsåldern, även om individer i alla åldrar kan drabbas. Patienter med ektopiskt ACTH-producerande tumörer är i regel något äldre, och lika många män som kvinnor drabbas.
Symtom och tecken
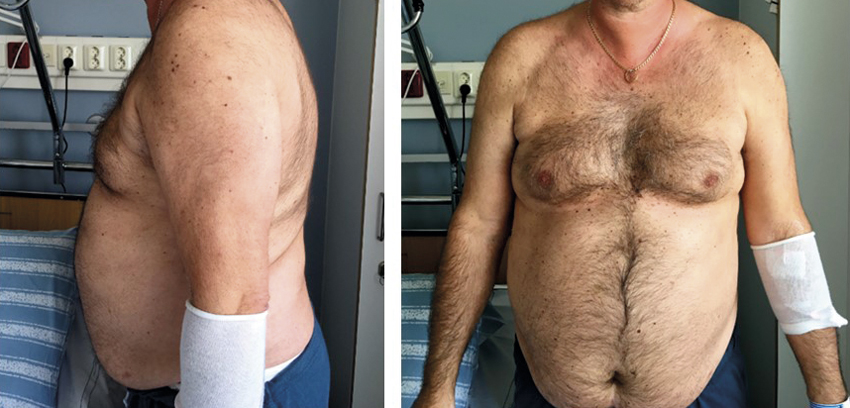
Den klassiska kliniska bilden vid uttalat Cushings syndrom är inte svår att känna igen. Syndromets svårighetgrad varierar dock betydligt mellan olika individer när diagnosen ställs. De vanligaste symtomen som patienter med Cushings syndrom söker för är viktuppgång och trötthet [1, 4, 5]. Typiskt är central fettansamling tillsammans med oproportionerligt smala armar och ben. Majoriteten av patienterna har hypertoni, som inte sällan är svårbehandlad, och en tredjedel har diabetes mellitus. Vidare är symtom från hud vanliga, inklusive hudatrofi, striae, blåmärken, ansiktsrodnad och akne. Andra vanliga symtom är nedstämdhet, kognitiv dysfunktion, sömnsvårigheter, menstruationsrubbningar och osteoporotiska frakturer. Således är många av symtomen ospecifika och vanliga i den allmänna befolkningen, vilket gör att diagnosen lätt kan missas. Vissa symtom, som blålila striae, ansiktsrodnad, proximal muskelsvaghet, blåmärken och oförklarlig benskörhet, är dock mer typiska än andra [6].
De senaste åren har det blivit allt vanligare att patienter med Cushings syndrom upptäcks i ett tidigt skede av sjukdomsutvecklingen, inte sällan i samband med utredning av ett binjureincidentalom [7]. I dessa fall kan trötthet, nedstämdhet och/eller viktuppgång vara de enda symtomen som patienterna har.
Den kliniska bilden är ofta snarlik oavsett etiologi. Patienter med ektopiskt Cushings syndrom har dock ofta ett snabbare sjukdomsförlopp med mer uttalad hyperkortisolism än patienter med Cushings sjukdom och kortisolproducerande binjureadenom. Den uttalade hyperkortisolismen orsakar ofta en kraftig katabolism med svår muskelsvaghet, hyperglykemi, svårbehandlad hypertoni och ibland hypokalemi. På grund av det uttalade katabola tillståndet är det mindre vanligt med viktuppgång och den annars karakteristiska centrala fettansamlingen hos patienter med grav hyperkortisolism.
Fördröjd diagnos
Då Cushings syndrom är ovanligt, och många av de symtom och kliniska tecken som patienter med Cushings syndrom söker för är ospecifika och vanliga i befolkningen, är lång fördröjning av diagnosen tyvärr vanlig. En aktuell tysk studie visade i genomsnitt 3 års fördröjning från patienternas första läkarkontakt på grund av symtom orsakade av Cushings syndrom tills rätt diagnos ställdes [8]. I genomsnitt träffade patienterna fem olika specialistläkare innan diagnos ställdes; vanligast var allmänläkare, gynekologer, hudläkare, internmedicinare och/eller ortopeder [8]. Fördröjd diagnos är också ett faktum i Sverige, där patienter med Cushings syndrom väntar i genomsnitt 2 år från första symtom till diagnos [2]. Denna fördröjning är beklaglig. Livskvaliteten är kraftigt nedsatt hos patienter med Cushings syndrom och förbättras inte förrän efter behandling [9]. Allvarliga följdsjukdomar som kardiovaskulär sjukdom, frakturer, djup ventrombos och lungemboli är vanliga åren före diagnos och behandling av Cushings syndrom [10]. Vidare är lång duration av hyperkortisolism före diagnos förknippad med ökad mortalitet, vilket betonar vikten av tidig diagnos och behandling för att förbättra livskvalitet samt minska morbiditet och mortalitet [11].
Diagnostik
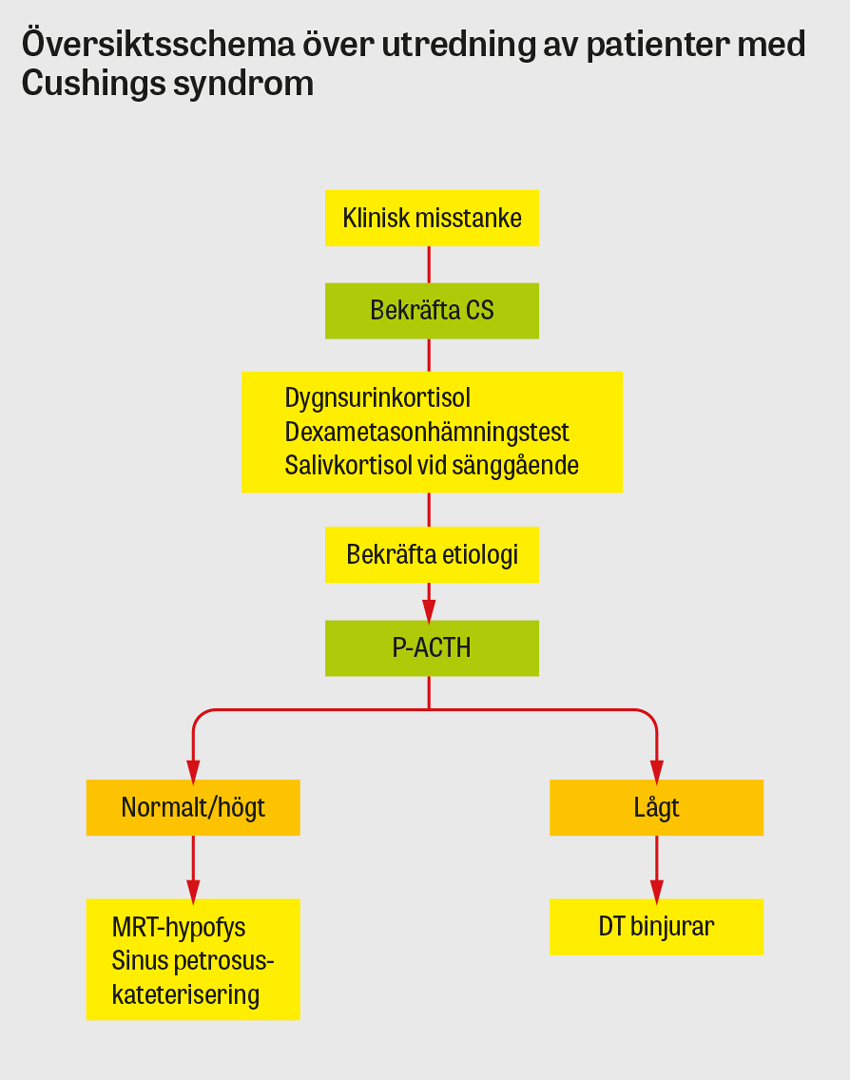
Vid klinisk misstanke om Cushings syndrom är det första steget i utredningen en noggrann läkemedelsanamnes avseende kortisonpreparat, inklusive högre doser av inhalationssteroider, starka kortisonkrämer etc, då biverkningar av exogent tillförda glukokortikoider ger samma kliniska bild som endogent Cushings syndrom. Om biverkningar av exogena glukokortikoider kan uteslutas bör biokemisk screening för endogen hyperkortisolism genomföras utan dröjsmål.
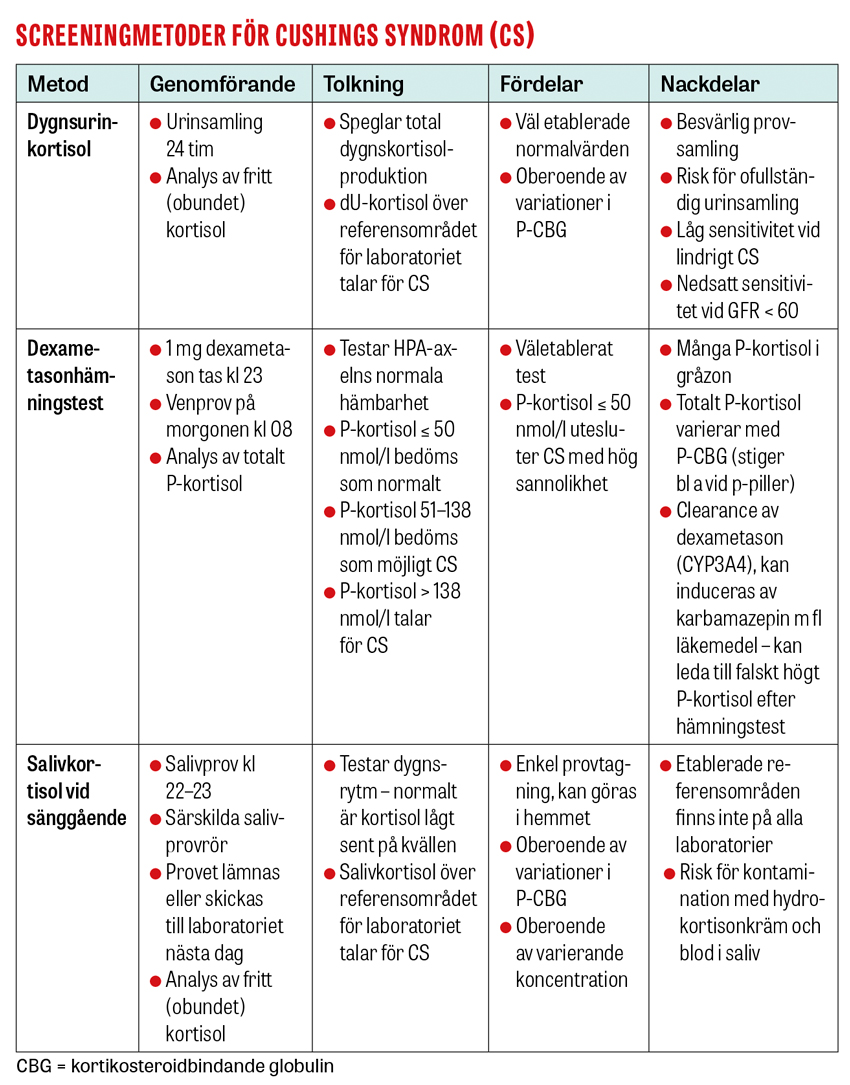
Rekommenderade screeningmetoder är dygnsurin-kortisol, dexametasonhämningstest och salivkortisol före sänggående [6]. Om ett av screeningstesten utfaller patologiskt, det vill säga talande för förhöjd kortisolproduktion, bör minst ytterligare ett av de övriga diagnostiska testen genomföras för att bekräfta autonom kortisolproduktion [6]. Det mest använda screeningtestet för Cushings syndrom inom primärvården är urinkortisol, där kortisolkoncentrationerna mäts i en, eller helst två dygnsmängder urin. Testet är enkelt och kan göras på alla vårdenheter, men har låg sensitivitet och kan vara normalt vid lindrigare Cushings syndrom och vid nedsatt njurfunktion. Dexametasonhämningstest är ett betydligt känsligare screeningstest, men många patienter (30 procent) utan Cushings syndrom har ett falskt positivt test. Salivprovtagning på kvällen före sänggåendet har också hög sensitivitet, även hos patienter med lindrig hyperkortisolism, och är ett enkelt test som kan göras i hemmet.
Samtliga patienter med biokemiskt bekräftad Cushings syndrom bör remitteras till en endokrinolog för vidare utredning. Även patienter med negativa screeningsprov bör remitteras om det fortfarande finns klinisk misstanke om endogent Cushings syndrom.
Efter bekräftad hyperkortisolism mäts ACTH i plasma. Lågt plasma-ACTH tyder på en kortisolproducerande tumör i en av binjurarna, och datortomografi av dessa ger oftast diagnosen. Vid högt eller normalt plasma-ACTH är orsaken antingen Cushings sjukdom eller ektopisk ACTH-produktion. Eftersom hälften av patienterna med Cushings sjukdom har ett mycket litet ACTH-producerande hypofysadenom, som inte syns vid magnetkameraundersökning, krävs i princip alltid invasiv provtagning av ACTH direkt från hypofysens venösa avflöde (sinus petrosus). Om ACTH i sinus petrosus är högre än i perifert blod ställs diagnosen Cushings sjukdom. Om ACTH är lika högt i hypofysärt som perifert blod måste ektopisk ACTH-producerande tumör misstänkas.
Behandling
Alla patienter med Cushings syndrom, oavsett bakomliggande orsak, ska erbjudas behandling för att minska morbiditet och mortalitet samt få en förbättrad livskvalitet.
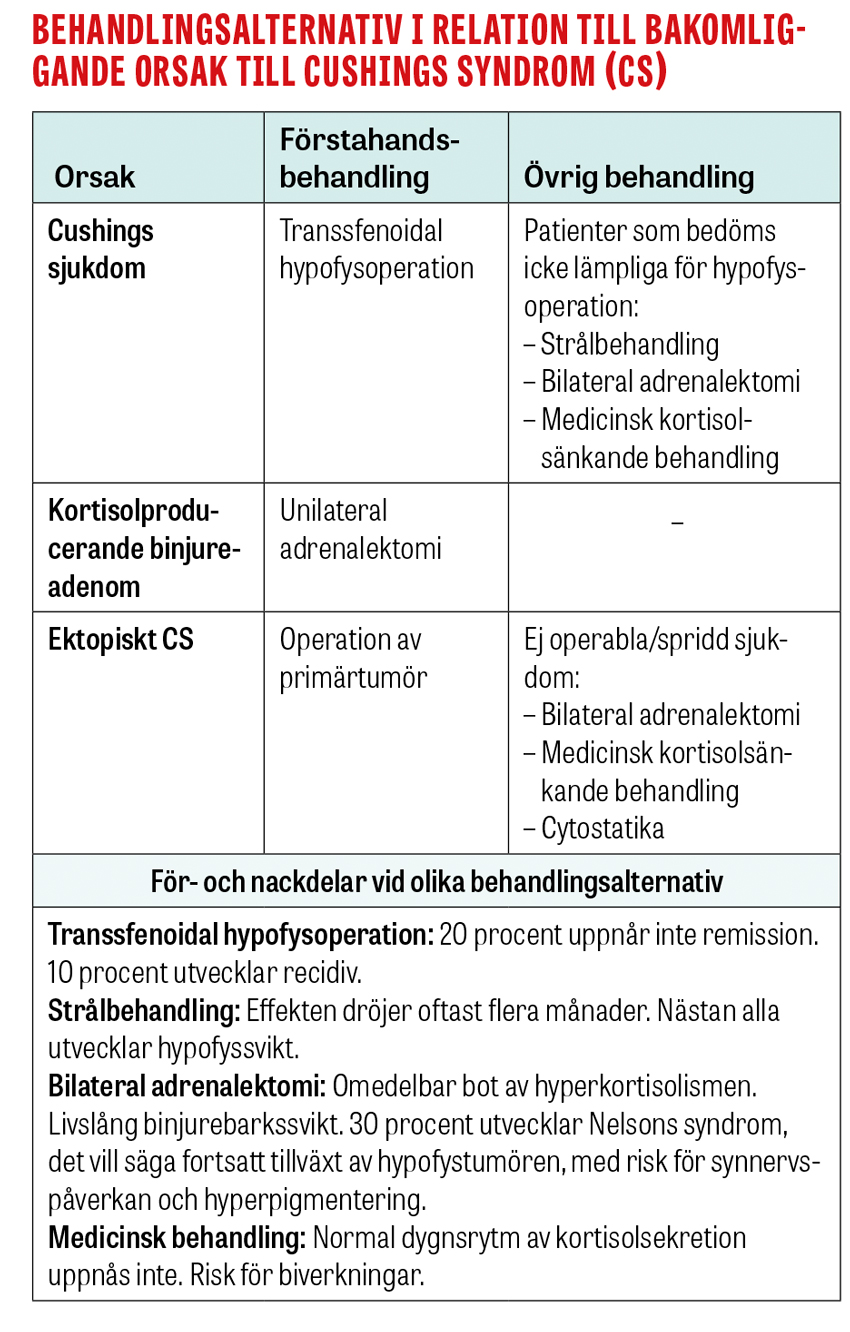
Förstahandsbehandling för patienter med Cushings sjukdom är transsfenoidal hypofysoperation där det ACTH-producerande adenomet avlägsnas. Andra behandlingsalternativ är strålbehandling av hypofystumören, bilateral adrenalektomi samt medicinsk kortisolsänkande behandling.
Vid en kortisolproducerande binjuretumör är det primära behandlingsalternativet unilateral adrenalektomi och vid ektopiskt Cushings syndrom operation av den ACTH-producerande tumören. Många patienter med ektopiskt Cushings syndrom har dock spridd sjukdom vid diagnos, vilket omöjliggör kurativ behandling.
Även om kortisolsänkande läkemedel i undantagsfall kan ges under lång tid till patienter med Cushings syndrom, oavsett etiologi, används dessa huvudsakligen preoperativt för att minska komplikationsrisker samt sänka blodtrycks- och blodsockernivåerna. De mest använda läkemedlen är ketokonazol och metyrapon. Vidare ska trombosprofylax ges till alla patienter med medelsvår eller svår hyperkortisolism för att minska den kraftigt ökade perioperativa risken för trombossjukdom. Hur länge behandling med trombosprofylax bör pågå är oklart, men minst en månad postoperativt har föreslagits [12].
Vid behov av akut sänkning av kortisolnivåerna, till exempel hos patienter med uttalad muskelsvaghet, svårbehandlad hypokalemi, snabbt progredierande osteoporos med frakturer och/eller allvarliga psykiska störningar på grund av grav hyperkortisolism, kan behandling med etomidat övervägas. Etomidat har en kraftigt hämmande effekt på kortisolproduktionen som leder till sänkning av kortisolnivåerna inom några få timmar.
Följdsjukdomar
Patienter med Cushings syndrom har ökad mortalitet, främst på grund av kardiovaskulära sjukdomar, men även på grund av infektioner och självmord [13]. Således har patienter med otillräckligt behandlad Cushings sjukdom upp till 5–7 gånger högre mortalitet än normalbefolkningen [13, 14]. Mortaliteten är lägre hos patienter som uppnår remission efter behandling men risken är fortfarande dubbelt så hög som i normalbefolkningen [13, 15]. Vidare har patienter i remission efter Cushings syndrom fortsatt ökad risk för kardiovaskulär sjukdom, hjärtinfarkt, stroke och venös tromboembolism [10, 16]. Risken för frakturer, som är kraftigt ökad hos patienter med aktiv hyperkortisolism, normaliseras däremot efter behandling. Livskvalitet och kognitiv funktion, inklusive minne, koncentrationsförmåga och uppmärksamhet, förbättras också efter behandling men normaliseras inte [9].
Uppföljning
Livslång uppföljning är nödvändig för alla patienter som har behandlats för Cushings syndrom. Alla patienter med Cushings syndrom som är framgångsrikt behandlade med operation utvecklar binjurebarkssvikt postoperativt och behöver ersättningsbehandling med hydrokortison. De flesta patienter, förutom de som opereras med bilateral adrenalektomi, återfår normal kortisolproduktion inom 6–18 månader postoperativt [17]. Av stor vikt är att informera patienterna noggrant om vad det innebär att ha binjurebarkssvikt och förhållningssätt vid eventuella akuta åkommor, samt att utrusta dem med ett varningskort för patienter med kortisolbrist [18].
Minst 10 procent av patienter med Cushings sjukdom som behandlas med transsfenoidal hypofysoperation, och 20 procent av patienter som får strålbehandling mot hypofysen, recidiverar i hyperkortisolism. Kliniska och biokemiska tecken tydande på recidiv ska därför kontrolleras minst en gång om året. Salivkortisol vid sänggåendet tycks vara den känsligaste diagnostiska metoden för att upptäcka recidiverande sjukdom.
Läs även författarintervjun med Sofie Wengander.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Orsaker till endogent Cushings syndrom1
ACTH-beroende Cushings syndrom:
- ACTH-producerande hypofysadenom, 50–70 procent
- Ektopiskt ACTH-producerande tumörer, 5–25 procent
- ACTH-producerande hypofyscancer, < 1 procent
ACTH-oberoende Cushings syndrom:
- Kortisolproducerande binjureadenom, 15–25 procent
- Kortisolproducerande binjurebarkscancer, 5 procent
- Makronodulär binjurebarkshyperplasi, < 1 procent
- Mikronodulär binjurebarkshyperplasi, < 1 procent
1 Incidens- och prevalenssiffror för de olika formerna av Cushings syndrom är något osäkra på grund av avsaknad av stora epidemiologiska studier. Detta gäller speciellt andelen patienter med ektopiskt ACTH-producerande tumörer, där mellan 5 [4] och 25 procent [2] har rapporteras.
Cushings syndrom – Symtom och tecken
- Trötthet, 90 procent
- Viktuppgång med central fettansamling, ökat bukomfång, runt ansikte, supraklavikulära fettkuddar och fettkudde på nacken, 80–90 procent
- Hypertoni, 75–85 procent
- Hudförändringar, inklusive hudatrofi, blålila striae
(endast patienter < 40–45 år), blåmärken, ökad rodnad i ansikte och på bröst, akne, 70–80 procent - Proximal muskelatrofi och muskelsvaghet, 60–70 procent
- Kognitiv dysfunktion inklusive minnes- och koncentrationssvårigheter och nedsatt uppmärksamhet, 60–80 procent
- Hirsutism, 50–60 procent
- Oligomenorré/amenorré, 50–60 procent
- Sömnsvårigheter, 50 procent
- Nedsatt sexlust och potens, 50 procent
- Depression, 40–60 procent
- Diabetes mellitus, 30 procent
- Frakturer, 20 procent
(uppdaterad 2021-03-03)




![Kortisonkort. Baserat på [18].](https://lakartidningen.se/wp-content/uploads/2020/09/Fig6_webb.jpg)