Egenreferat. Glukagonlik peptid-1 (GLP-1) är ett hormon som produceras av enteroendokrina celler i tarmslemhinnan. GLP-1 bidrar till mättnad och att kontrollera sockernivåerna i blodet i samband med måltid. Frisättningen är av oklara skäl hämmad vid fetma med typ 2-diabetes, vilket misstänks bidra till dessa sjukdomstillstånd. Roux-en-Y är en metod för gastrisk bypass som effektivt sänker kroppsvikten. Redan någon dag postoperativt, innan någon väsentlig viktminskning hunnit ske, förbättras sockerläget avsevärt och samtidigt ökar GLP-1-frisättningen vid födointag [1].
För att utreda mekanismerna bakom den gastriska bypasskirurgins snabba viktoberoende effekter på typ 2-diabetes initierade vi denna studie. Med global proteomikanalys på prov från tunntarmsslemhinnan från patienter före och efter gastrisk bypass eftersträvade vi att identifiera nya mekanismer som operationen verkar igenom. Vi gjorde även studier på möss och i cellkulturer med enteroendokrina celler från jejunum.
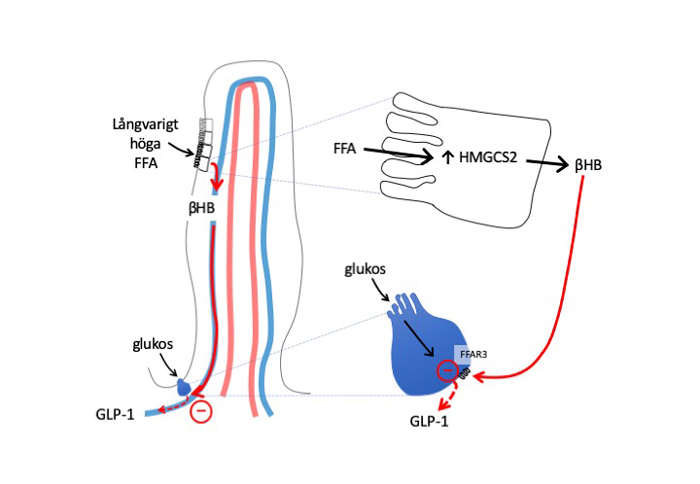
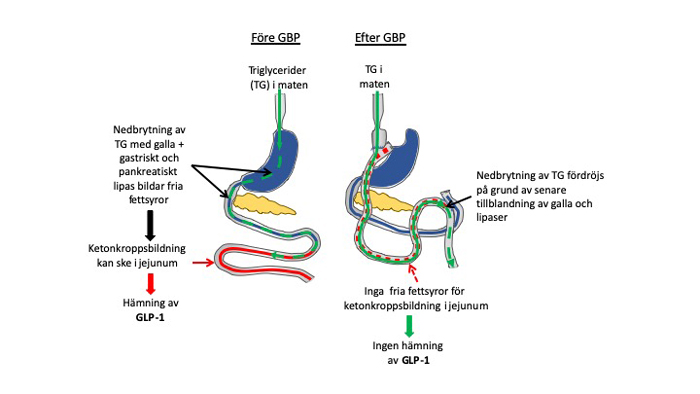
Det har visat sig att tunntarmsslemhinnan kan börja producera ketonkroppar (t ex β-hydroxibutyrat) vid långvarigt intag av fet mat. Såväl det ketonkroppsbildande enzymet, mitokondriellt HMG-CoA-syntas (mHMGCS), som ketonkroppar finns i höga nivåer i slemhinnan hos obesa patienter före en gastrisk bypass. Ketonerna fungerar lokalt i tarmen som signalsubstanser, som hämmar de enteroendokrina cellernas GLP-1-frisättning (Figur 1). Efter gastrisk bypass hämmas mHMGCS-uttrycket med mer än 70 procent och ketonkroppsproduktionen minskar. Troligen sker detta som en följd av omkopplingen av mag–tarmkanalen (Figur 2). Härmed försvinner »bromsen« på GLP-1. Detta kan bidra till att förklara den snabbt ökade GLP-1-frisättningen och den förbättrade blodsockerregleringen efter operationen [2].
Normalt produceras ketonkroppar i levern vid svält och är livsviktiga för överlevnad, till exempel för hjärnan, som är beroende av ketonkroppar vid långvarig svält. Bildningen av ketonkroppar i tarmen, så kallad intestinal ketogenes, är ett nyupptäckt fenomen som inträffar vid intag av kost med hög fetthalt under längre tid och alltså verkar ha en annan funktion: att hämma mättnadssignaleringen. Kanske har syftet varit att öka förmågan att äta när födotillgången har varit god. I dagens samhälle bidrar mekanismen i stället till övervikt och diabetes. Förhoppningen är nu att denna upptäckt ska möjliggöra en ny typ av framtida läkemedel som kan efterlikna effekterna av gastrisk bypass på diabetes och övervikt.