Egenreferat. Neuroblastom är en heterogen barncancerform som drabbar yngre barn. Trots ofta biverkningstung multimodal behandling med cytostatika, kirurgi, strålning, autolog stamcellstransplantation och immunterapi är överlevnaden för barn med högriskneuroblastom endast drygt 50 procent. Effektiv målinriktad behandling är därför efterlängtad. Mutationer i tyrosinkinasreceptorn ALK har identifierats som sjukdomsdrivande och påvisas i ca 10 procent av neuroblastom, men kliniska erfarenheter av ALK-hämning är ännu begränsade.
En unik fallstudie där en gränsöverskridande kombination av kliniska, genetiska, proteomiska och funktionella studier ledde till individanpassad behandling har nyligen rapporterats av oss [1]. En 6 månader gammal pojke diagnostiserades med neuroblastom i ena binjuren och omfattande metastasering i benmärg, lever och lungor. Han uppvisade extrema nivåer av katekolaminmarkörer och led av svårkontrollerat högt blodtryck. Trots fem olika kombinationer av konventionell cytostatikabehandling och operation av primärtumören kvarstod behandlingsrefraktära metastaser.
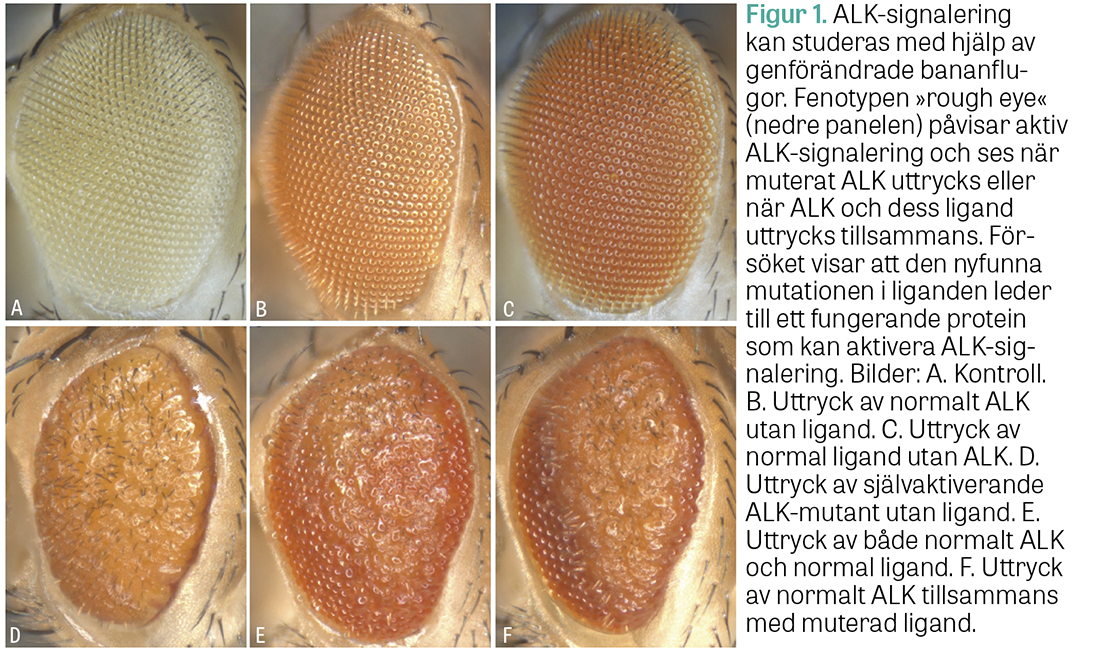
Analys av tumörresektat visade tillskott av kromosomarm 2p, där ALK, dess ligand ALKAL2 och onkgenen MYCN är lokaliserade. Proteinanalyser påvisade aktivering av ALK men även av TRKA, också med betydelse inom neuroblastom. Helgenomsekvensering fann dock inga korresponderande genetiska förändringar. I stället upptäcktes en inte tidigare beskriven konstitutionell DNA-variant i ALKAL2. Studier på bananflugor visade att ALKAL2-varianten är funktionell (Figur 1) och kan aktivera ALK, medan immunblottning visade att ALKAL2 var uttryckt i tumören. Därmed kan ALKAL2-varianten ha bidragit till sjukdomen.
Då både ALK och TRKA var aktiverade startades experimentell behandling med ALK-TRK-ROS-inhibitorn entrektinib (nu Rozlytrek, då endast i fas 1-studie för äldre barn) genom ett så kallat »compassionate use«-program och licens från Läkemedelsverket. Entrektinib tolererades väl och barnets allmäntillstånd förbättrades snabbt, medan lung- och levermetastaser samt katekolaminmarkörer minskade mycket gradvis och normaliserades först efter flera år. Gossen behandlas fortfarande med entrektinib men är välmående med normal tillväxt och utveckling 6,5 år efter diagnos.
I dag är storskaliga genetiska analyser en viktig grund för precisionsmedicin, men vår studie påvisar att proteinanalyser också har stor klinisk potential. Barn med neuroblastom och ALK-aktivering på proteinnivå, även utan ALK-mutation, bör beaktas för behandling med ALK-hämmare.