Sammanfattat
Migrän är en ärftlig huvudvärkssjukdom inom det centrala nervsystemet med sekundära effekter på såväl de extra- som de intrakraniella blodkärlen. Migränanfall kan ge kraftig funktionsnedsättning och utgör en stor börda för både individ och samhälle.
Modern migränbehandling är i mångt och mycket baserad på de nu rådande patofysiologiska teorierna kring migränsjukdomen; dessa involverar första grenen av trigeminusnerven och trigeminuskärnan och vidare upp i CNS.
Flera behandlingsalternativ ökar sannolikt möjligheten att hitta en för individen rätt anpassad terapi, men ökar samtidigt kraven på den förskrivande läkaren att känna till de enskilda preparatens för- och nackdelar.
Behandling med migränspecifika läkemedel lindrar inte enbart smärtan utan även de associerade symtomen. Framgångsrik behandling kräver adekvat dosering och val av optimal beredningsform.
Överanvändning av symtomlindrande läkemedel bör undvikas, eftersom den i sig kan leda till mer huvudvärk. Användning av dessa läkemedel bör begränsas till högst två eller tre dagar i veckan.
Användning av huvudvärkskalender kan hjälpa läkaren och patienten både att förstå sjukdomen och att använda läkemedel på ett bra sätt.
Migrän är en kronisk, delvis ärftlig, neurologisk sjukdom som karakteriseras av återkommande episoder med svår pulserande huvudvärk kombinerad med illamående, ljus- och ljudkänslighet men med symtomfrihet mellan attackerna [1, 2]. Enligt internationell klassifikation varar ett migränanfall hos en vuxen individ 4–72 timmar [3].
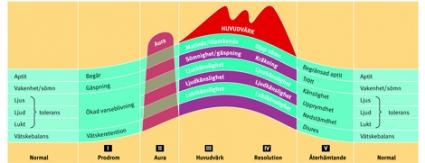
Man tycker sig kunna identifiera fem faser under migränattacken: försymtom (prodromal fas), aura med neurologiska retnings- och bortfallssymtom, huvudvärksfas, upplösning (resolution) och återhämtning (postdromal fas) [3, 4] (Figur 1). Av dessa är det bara den klassiska neurologiska auran som har en distinkt början och avslutning [5].
Prevalens
Ettårsprevalensen för migränsjukdomen varierar mellan 10 och 13 procent (6–9 procent för män och 15–18 procent för kvinnor) [6-11]. En fördubblad till trefaldigad risk för migrän har rapporterats bland förstagradssläktingar (föräldrar, syskon och barn) till individer med migrän [12-16]. Vart fjärde hushåll har minst en individ med migrän, och var femte kvinna i fertil ålder har migrän [9].
Följaktligen är migrän en mycket vanlig sjukdom, som drabbar omkring 1 miljon svenskar [7]. En medelfrekvens på 1,3 migränanfall per månad innebär att den svenska befolkningen har omkring 13 miljoner migränanfall per år. Av den miljon svenskar som har migrän är omkring 400000 extra hårt utsatta genom att migränattackerna kommer ofta, vilket innebär fyra attacker eller fler per månad [7].
Efter 40-årsåldern minskar förekomsten av migrän med stigande ålder. Minskningshastigheten kan uttryckas på så sätt att förekomsten halveras på cirka 15 år [7]. Detta betyder i ett svenskt perspektiv att cirka 20 procent av svenskar i 40-årsåldern och cirka 5 procent av svenskar i 70-årsåldern har migrän.
Belastning för individ och samhälle
Migrän är ett stort funktionshinder och en stor ekonomisk börda för både individen och samhället [17-24]. Förutom den invaliditet och det omedelbara lidande som den drabbade upplever under attackerna, verkar oförutsägbarheten hos migrän och den förväntansoro som skapas inför framtida attacker även producera negativa effekter mellan attacker [17-25].
Migrän drabbar framför allt kvinnor i arbetsför ålder [9]. I en rapport utgiven av Världshälsoorganisationen (WHO) rankas migränsjukdomen på 12:e plats bland kvinnor när det gäller olika sjukdomars grad av funktionshinder [26-28].
Migrän står tillsammans med andra huvudvärksåkommor för en tredjedel av de totala direkta och indirekta kostnaderna för alla neurologiska sjukdomar i Europa [29]. Varje dag besväras 2 miljoner individer i Europa av migränanfall, och sjukdomen belastar den europeiska ekonomin med minst 27 miljarder euro årligen [29].
Anamnestagning
Ett optimerat omhändertagande av individer med besvärande huvudvärk är en svår, men samtidigt intressant och utmanande uppgift. Dagens patienter med huvudvärk är medvetna och välinformerade, inte minst inom sitt eget sjukdomsområde, och de ställer höga krav på sin läkare när det gäller kunskap och bemötande.
Fortfarande saknas objektiva test i form av specifika laboratorieundersökningar, röntgenologiska, neurofysiologiska eller andra metoder för att påvisa primära huvudvärkssjukdomar. Patientens sjukdomshistoria är därför den viktigaste källan till den information som leder till diagnos.
Många patienter tycker det är svårt att svara i detalj på frågorna och har ingen exakt överblick över sina anfall och symtom. Därför ska man be patienten föra en sk huvudvärksdagbok i hemmet. Den kan i praktiken bestå av en almanacka, där patienten skriver upp varje anfall och dess karakteristika. Det är viktigt att patienten skriver varje dag i huvudvärksdagboken, eftersom erfarenheten visar att det blir mindre korrekt om uppgifterna fylls i ur minnet i efterhand.
Klassifikationskriterier
I den nya internationella huvudvärksklassifikationen (International Classification of Headache Disorders, ICHD-II) ingår migrän som den första av de fyra primära huvudvärksformerna [3].
Majoriteten av individer med migrän kan diagnostiseras till att ha migrän utan aura, migrän med aura eller båda formerna. I de allra flesta fall räcker denna diagnostisering för kliniskt omhändertagande, men ibland kan det vara av värde att subdiagnostisera enligt ovanstående klassifikation.
Migrän utan aura.
Detta är den vanligaste formen av migrän, och diagnosen är uppenbar enbart på basis av noggrann anamnesgenomgång. Tidigare använda beteckningar är vanlig migrän och hemicrania simplex [3]. Migrän utan aura beskrivs som en idiopatisk, återkommande huvudvärkssjukdom som manifesteras i attacker med 4–72 timmars duration. Huvudvärken kännetecknas av ensidig lokalisation, pulserande karaktär, måttlig till svår intensitet, försämring av normal fysisk aktivitet samt tillhörande symtom såsom illamående och/eller ljus- och ljudöverkänslighet (Fakta 1).
Migrän med aura.
Tidigare använda beteckningar är klassisk migrän, oftalmisk, hemiparetisk, hemiplegisk eller afatisk migrän, migrän accompagnée och komplicerad migrän [3]. Migrän med aura beskrivs som en idiopatisk, återkommande migränsjukdom manifesterad i attacker av reversibla, fokala neurologiska symtom, som vanligtvis utvecklas gradvis över 5–20 minuter och varar mindre än 60 minuter [3]. Omkring 30 procent av individer med migrän upplever aurasymtom. Huvudvärk med egenskaper av migrän utan aura följer vanligtvis aurasymtomen. Mindre vanligt är att huvudvärken saknar migränegenskaper eller är helt frånvarande.
Migrän med typisk aura består av visuella och/eller sensoriska symtom och/eller talstörningar (Fakta 2). Migränauran karakteriseras av gradvis utveckling, duration kortare än 1 timme och en blandning av positiva (retning) och negativa (bortfall) egenskaper med fullständig reversibilitet, och den är förbunden med en huvudvärk som uppfyller kriterierna för migrän utan aura.
Det mest vanliga är att huvudvärken är kontralateral till aurasymtomen, tex att känselstörningar i höger sida följs av huvudvärk på vänster sida. Visuell aura är vanligast och har mestadels formen av en utåtkonvex figur med sågtandsliknande, flimrande kant (positivt retningssymtom), vilken under minuter successivt sprids och vidgas åt höger eller vänster i synfältet [3, 5].
Patofysiologi
Migränsjukdomens etiologi är ofullständigt känd men förefaller minst sagt komplicerad. Det har varit känt i decennier att migränsjukdomen är ärftlig. Senare undersökningar av familjär hemiplegisk migrän har visat på mutationer i kromosom 19 och CACNA1A-genen, med påverkan på hjärncellernas kalciumkanaler som följd [30]. Särskilt de spänningsberoende kalciumkanalerna av P/Q-typ har utpekats, och dessa är speciellt vanliga i cerebellum, cerebrala kortex, talamus, hypotalamus och i övre hjärnstammen. Vi måste emellertid påpeka att än idag har detta inte påvisats för »de vanliga formerna av migrän«, trots många studier. Patienter med familjär hemiplegisk migrän tycks dessutom inte vara en enhetlig grupp, eftersom 3 olika gener nu påvisats som möjlig orsak till denna sjukdom [31].
Hjärnans aktivering under ett migränanfall
Ett tänkbart scenario som sammanlänkar de tidigt observerade förändringarna i intrakraniell cirkulation till en hereditär faktor är att nervceller med genetiskt reducerat antal/förändrad funktion av kalciumkanaler sannolikt är lättare att aktivera (beroende på förändrad membranpotential). Idag anser man att de eventuellt kan resultera i en våg av spridande depression, vilket aktiverar den sk trigeminovaskulära reflexen och som sedan resulterar i excitation av specifika områden, tex den periakveduktala grå substansen (PAG, periaqueductal grey), nucleus raphe- och locus coeruleus-neuron [32].
Bevis för att hjärnstamskärnor är involverade vid migrän kom först från Weiller och medarbetare, vilka studerade akuta unilaterala migränattacker med positronemissionstomografi (PET). Detta har konfirmerats i senare studier [33, 34]. Under attackerna observerades ökat blodflöde i de cerebrala hemisfärerna, i cingulum-, hörsel- och synassociationskortex samt i vissa hjärnstamsregioner. Endast hjärnstamsaktiveringen kvarstod emellertid efter injektion med sumatriptan, vilken totalt lindrade såväl huvudvärk som fono- och fotofobi.
Dessa fynd stödjer hypotesen att patogenesen vid migrän är relaterad till obalans i aktivering av de hjärnstamskärnor som reglerar nociception och vaskulär kontroll; fynden visar till och med ett samband med associerade symtom som emesis.
Aktivering av trigeminusnerven
Studier av den funktionella rollen av trigeminovaskulära systemet avslöjade tidigt att denervation (avskärning av trigeminusnerven) inte förändrade regionalt cerebralt blodflöde eller glukosomsättning i hjärnan, cerebrovaskulära svar på koldioxid eller autoregulation. I stället observerades att lokalt inducerad vasokonstriktion, som utlöstes med ett flertal agens, snabbt motreglerades av de sensoriska nerverna som genom frisättning av CGRP (kalcitoningenrelaterad peptid) kunde normalisera cerebrovaskulär tonus [35].
Nuvarande hypotes är att en spridande våg av kärlkontraktion sker över hjärnan, och denna kärlkonstriktion motregleras genom antidrom frisättning av CGRP från de sensoriska nerverna. Kliniskt observerar vi detta som ökad frisättning av CGRP i kraniellt venöst blod [32].
När väl den trigeminala vaskulära reflexen initierats, aktiveras troligen den centrala delen av denna nervbana, som sträcker sig till nucleus trigeminalis caudalis och dess reciproka delar vid C1- och C3-nivåerna.
Introduktionen av triptaner har inneburit ett stort genombrott vid behandling av migrän och fokuserat på vilken roll 5-HT1B/1D-agonister (serotonin 1B/1D-agonister) spelar vid akut behandling av migrän. Dessa läkemedel utövar troligen sin effekt genom vasokonstriktion (för att begränsa för hög distension i circulus arteriosus cerebri) via 5-HT1B-receptorer samt blockad av aktiviteten i sensoriska nerver genom frisättning av CGRP via 5-HT1D-receptorer [2, 35]. 5-HT1B/1D-agonister utövar sin effekt på presynaptiska receptorer vid trigeminala afferenter och inhiberar frisättningen av CGRP.
Autoradiologiska studier med radioaktivt märkta triptaner har bekräftat existensen av 5-HT1B/1D-receptorer i avgränsade hjärnstamskärnor som är involverade i nociceptiv bearbetning [36]. Experimentella studier har gett övertygande bevis för att 5-HT1B/1D-receptorer är lokaliserade i avgränsade kärnor centralt i det trigeminala systemet, som troligen aktiveras under migränanfallet, och att dessa receptorer verkligen är åtkomliga för triptaner vid systemisk administration [37]. Det är av stort intresse att nya studier visat att en lika god antimigrän effekt kan erhållas genom CGRP-receptorhämning som med triptaner [38].
Patienter med migrän blir vanligtvis lugnade när de får veta att det faktiskt sker en rad fysiologiska förändringar i hjärnan under ett migränanfall. Man kan exempelvis förklara för dem att individer med migrän har en hjärna som är mer känslig för inkommande intryck (tex beröring, ljus och ljud). Detta beror på att en rad olika neuropeptider frisätts inom centrala nervsystemet, vilka gör att normala känselintryck upplevs som smärtsamma/obehagliga. Man kan också förklara att auran beror på att en urladdning sker på hjärnans yta, och beroende av vilket område som drabbas får man motsvarande aurasymtom (tex flimmerskotom, stickningar/domningar i huden och påverkan på talet) [39].
Principer för migränbehandling
Framgångsrik behandling av migränsjukdomen underlättas om läkaren känner till de patofysiologiska teorierna och baserat på dessa kan informera patienten om hur man bäst använder såväl icke-farmakologisk som farmakologisk behandling [2, 40, 41].
Icke-farmakologiska behandlingar inkluderar utbildning av patienten om sjukdomen och om nödvändiga livsstilsförändringar, med målsättningen att undvika utlösande faktorer för huvudvärken. Till icke-farmakologisk behandling hör också akupunktur, avslappningsträning och biofeedback. Tillsammans kan dessa alternativ utgöra ett komplement till farmakologisk profylax, och de är förstahandsvalen för vuxna individer som inte kan eller vill använda akuta eller förebyggande läkemedel mot migrän [40].
Den farmakologiska behandlingen av primär huvudvärk kan vara akut (anfallskuperande, symtomatisk) eller förebyggande (profylaktisk). Någon dokumenterat effektiv akutbehandling mot aurasymtom saknas fortfarande. Även om man idag saknar möjlighet att bota migrän, kan adekvat kontroll uppnås i de flesta fall.
Anfallsbehandling
Akut anfallsbehandling uppfattas som det bästa alternativet av de flesta individer med migrän. Anfallsbehandling kan indelas i icke-specifika och migränspecifika preparat. Icke-specifika alternativ, såsom acetylsalicylsyra (ASA), paracetamol, icke-steroida antiinflammatoriska läkemedel (NSAID), opiater och kombinationsanalgetika, används för att behandla ett flertal olika smärttillstånd [2, 40-42]. Om ASA eller NSAID-preparat inte tolereras på grund av tex gastrointestinala biverkningar bör paracetamol användas i form av brustabletter eller som suppositorier. Vid illamående kan antiemetika ges i form av metoklopramid som tablett, kombinerat dospulver eller stolpiller.
Migränspecifika läkemedel
Till migränspecifik behandling hör mer eller mindre selektiva 5-HT1B/1D-agonister (tex triptaner). Den första triptanen (sumatriptan) innebar en revolution inom migränbehandlingen och har betytt ett nytt liv för många svårt migrändrabbade. Detta stimulerade forskarna att utveckla en andra generation triptaner med ambitionen att förbättra de farmakologiska egenskaperna. Under de senaste åren har fem nya triptaner lanserats på den svenska marknaden: naratriptan, zolmitriptan, rizatriptan, eletriptan och almotriptan [43]. Nyligen har ytterligare en triptan, frovatriptan, blivit tillgänglig i vissa länder.
Under utvecklingen av andra generationens triptaner har ambitionen varit att, jämfört med sumatriptan, förbättra såväl farmakodynamik som farmakokinetik. Emellertid finner man, om man jämför resultaten från olika kliniska prövningar, att de flesta triptanerna är anmärkningsvärt likvärdiga från både effekt- och biverkningssynpunkt [43].
Triptanerna är registrerade för användning inom åldersintervallet 18–65 år. För individer äldre än 65 finns ingen dokumentation från kontrollerade kliniska prövningar, men i klinisk praxis (under förutsättning att kontraindikationer beaktas) har triptan visat sig vara effektivt och tolereras väl även av dessa personer [40]. Vad gäller yngre individer får sumatriptan nässpray 10 mg användas från och med 12 års ålder.
De vanligaste biverkningarna vid triptanbehandling är trötthet och dåsighet, och symtom på obehaglig tyngd- eller tryckkänsla i bröstet, nacken och/eller halsen är typiska för denna läkemedelsgrupp [40]. Det finns ett flertal argument som stödjer påståendet att triptaninducerade symtom som åtstramning, tyngd-/tryckkänsla över bröstkorg/hals inte är av kardiovaskulärt ursprung och att triptanerna är att betrakta som säkra om de används enligt givna rekommendationer.
Val av beredningsform
Graden av illamående och gastrointestinal påverkan med risk för kräkning blir avgörande för val av beredningsform [44]. Injektionsbehandling erbjuder utan tvekan den mest konsekventa och snabbast insättande effekten med god lindring av migränattackens symtom. Injektion av sumatriptan med autoinjektor/injektionspenna lämpar sig speciellt för de individer som behöver snabb effekt (tex vid »morgonmigrän«), dem som besväras av kraftigt illamående/kräkningar och dem som inte fått önskvärd effekt av konventionell peroral behandling med triptaner. Emellertid ogillas denna beredningsform av flera individer med migrän, eftersom dess goda terapeutiska effekter kan ackompanjeras av uttalade biverkningar eller på grund av att individen har mer eller mindre uttalad sprutfobi.
Nässpray är ett alternativ när snabbt insättande effekt är önskvärd hos en individ som ogärna vill behandla sig med injektion. En betydande del av det som sprayas in i näskaviteten transporteras vidare mot svalget och sväljs med saliven [44]. Med undantag av obehaglig smak eller lokal slemhinneirritation tolereras denna formulering vanligtvis väl.
Tablettbehandling föredras av de flesta individer med migrän, trots att effekten av den kan störas av själva migränattackens inverkan på gastrointestinala funktioner. Vid migränattacken är magsäckens motorik hämmad redan tidigt under attacken, och det finns alltid en risk att illamåendet under attacken kulminerar i uppkastningar. Troligen är detta orsaken till att effekten av tablettbehandling kan variera högst påtagligt mellan migränattackerna. En alternativ peroral beredningsform är smälttabletten, som på några få sekunder löser sig på tungan och kan sväljas med munnens saliv utan att man behöver tillföra vätska. Denna beredningsform förefaller speciellt lämplig för individer vars illamående kan förstärkas av att de dricker eller i situationer då man inte har tillgång till vätska. Effektmässigt förefaller denna beredningsform vara likvärdig med motsvarande tablettberedning.
Suppositorium (tex sumatriptan och metoklopramid) är naturligtvis ett alternativ för individer med migrän vars attacker karakteriseras av uttalat illamående och kräkningar.
Oavsett vilken behandlingsstrategi man använder sig av bör respektive preparat prövas under optimala betingelser. Det är tex klart visat att en migränattack av hög intensitet är svårare att behandla än en lindrig sådan. Tills vidare bör rekommendation om tidigt insatt behandling gälla migränattackens huvudvärksfas. Om anfallsbehandlingen tas redan under aurafasen finns det risk för att den inte hjälper mot den efterföljande migränhuvudvärken. Utöver tidigt insatt behandling förefaller terapiresultatet bli bättre om individen tillåter sig att vila cirka 1 timme efter det att behandlingen påbörjats.
Cirka varannan individ upplever att migränanfallets symtom återkommer efter 6–12 timmar, vilket motsvarar ungefär den tid det finns terapeutiska koncentrationer av triptanen i blodet. Förnyad dosering med triptan ger åter symtomlindring. Antalet upprepade doseringstillfällen är avhängigt migränanfallets naturalförlopp.
Förebyggande läkemedelsbehandling
Förebyggande migränbehandling bör skräddarsys efter den enskilda patienten, vilket bla innebär att vederbörande förstår planeringen och aktivt deltar i beslut om behandlingen. Valet av förebyggande läkemedel måste individualiseras och styrs av kontraindikationer, potentiella biverkningar och behov av att behandla komorbida tillstånd, såsom astma, hypertoni, depression och sömnsvårigheter [2, 40-42]. Huvudsyftet med profylaktisk behandling är att optimera patientens förmåga att fungera normalt genom att reducera migränanfallens frekvens, duration och intensitet.
De åtta huvudgrupperna av profylaktiska preparat inkluderar betablockerare utan egenstimulerande sympatomimetisk effekt (som atenolol, metoprolol och propranolol), kalciumkanalblockerare (som licenspreparatet flunarizin), 5-HT2-antagonister (som pizotifen och cyproheptadin), 5-HT1/2-agonister (som licenspreparatet metysergid), icke-steroida antiinflammatoriska läkemedel (NSAID, tex naproxen), antiepileptiska läkemedel (som valproat, gabapentin och topiramat), angiotensinII-receptorantagonister (som kandesartan) och antidepressiva (som amitriptylin) [40, 42]. För prioritetsordning, se Fakta 3.
Migränpatienter som har ett uttalat behov av profylax bör tilllåtas att pröva olika förebyggande behandlingsalternativ enligt rekommendationer i Fakta 4. Dessutom bör patienten instrueras och uppmuntras att föra huvudvärksdagbok för att utvärdera effektiviteten vid uppföljande besök. Det är en vanlig erfarenhet att en patient kan behöva pröva två eller fler klasser av migränförebyggande läkemedel innan ett lämpligt preparat hittas [40].
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.