Sammanfattat
Diagnostik av autoantikroppar är viktigt vid utredning av oklar leverpåverkan.
Utöver antikropparna ANA, SMA, anti-LKM-1 och AMA finns ett flertal andra viktiga diagnostiska markörer för autoimmuna leversjukdomar.
Alla relevanta autoantikroppar kan inte detekteras med immunfluorescensmikroskopi, varför denna bör kompletteras med antigenspecifika test.
Titrar som mått på autoantikroppskoncentration är inte jämförbara mellan olika laboratorier.
Ett flertal autoantikroppar är viktiga diagnostiska markörer för autoimmun hepatit och primär biliär cirros. För primär skleroserande kolangit har däremot ingen stark serologisk markör identifierats. Sedan många år är immunfluorescens(IF)-mikroskopi på råttvävnad den etablerade metoden för att påvisa autoantikroppar. Metoden kräver dock erfarenhet vid avläsning och påvisar inte alla diagnostiskt betydelsefulla autoantikroppar. Med kunskap om autoantikropparnas molekylära specificitet har relevanta antigener framställts, och ett flertal antigenspecifika test finns numera tillgängliga. Dessa utgör värdefulla komplement till IF-mikroskopi, som fortfarande är basen för den serologiska diagnostiken.
Det som i dag benämns autoimmun hepatit typ 1 kallades i slutet på 1950-talet för »lupoid hepatit« på grund av förekomst av »LE-celler«, som är ett uttryck för antinukleära antikroppar riktade mot kromatin. Snart kom rapporter om att också antikroppar mot glattmuskelceller var vanligt förekommande vid denna sjukdom.
Sedan dess har ett flertal andra viktiga autoantikroppar identifierats för såväl autoimmun hepatit som primär biliär cirros.
I denna översikt beskrivs aktuella serologiska markörer.
Autoimmun hepatit typ 1
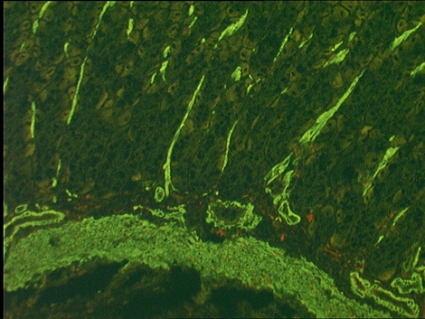
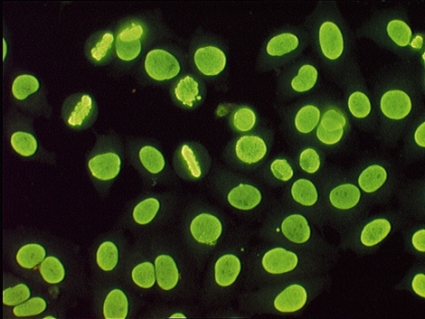
Antinukleära antikroppar (ANA). Förekomst av antinukleära antikroppar har rapporterats hos ca 60–80 procent av patienter med autoimmun hepatit. Ofta påvisas också antikroppar mot glattmuskelceller (SMA, smooth muscle antibodies), men isolerad förekomst av ANA ses hos ca 15 procent [1]. Vid autoimmun hepatit är ANA ofta riktade mot kromatin och ger ett »homogent« mönster vid IF-mikroskopi (Figur 1). I en del fall påvisas autoantikroppar mot dubbelsträngat DNA (anti-dsDNA), som annars är en stark markör för systemisk lupus erythematosus (SLE). I mindre utsträckning förekommer »kornigt« ANA-mönster, som är uttryck för antikroppar mot extrakromosomala antigener.
Utöver anti-dsDNA finns det ingen specifik ANA-subtyp som är kopplad till autoimmun hepatit och inte heller något sjukdomsspecifikt ANA-mönster. Förekomst av ANA ses vid IF-mikroskopi på råttvävnad, men numera används humana epitelceller (HEp-2) som antigenkälla vid rutinmässig ANA-diagnostik, eftersom deras stora cellkärnor gör det lättare att identifiera olika ANA-mönster.
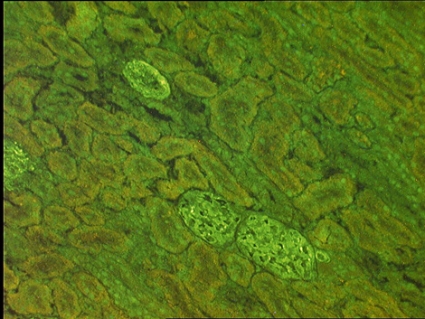
Antikroppar mot glattmuskelceller (SMA). SMA har rapporterats förekomma hos ca 70–80 procent av patienter med autoimmun hepatit, ofta ihop med ANA, men ses isolerat hos ca 35 procent [1]. SMA riktade mot filamentöst (F) aktin har hög specificitet för autoimmun hepatit och påvisas med IF-mikroskopi på råttvävnad [2]. Vanligtvis ses reaktion med glatt muskulatur i ventrikel och i kärlvägg, s k vessel(V)-mönster. Antikroppar mot andra mikrofilament kan dock ge liknande mönster och ses vid en rad andra tillstånd utan koppling till autoimmun hepatit.
Om reaktion mot aktin i glomeruli (G) och njurtubuli (T) också kan påvisas, s k VGT-mönster, är däremot specificiteten för autoimmun hepatit mycket hög [3].
Numera finns kommersiella test som mer specifikt påvisar autoantikroppar mot F-aktin, men de har ännu inte visat sig erbjuda några påtagliga fördelar i diagnostiken av autoimmun hepatit [4]. IF-mikroskopi på råttvävnad används därför fortfarande i första hand.
Antikroppar mot »soluble liver antigen« (anti-SLA). Anti-SLA är en stark markör för autoimmun hepatit typ 1 och har rapporterats förekomma i 10–50 procent. Dessa autoantikroppar anses vara kopplade till ett allvarligare sjukdomsförlopp och kan förekomma med eller utan samtidig förekomst av ANA och/eller SMA [5].
Anti-SLA påvisas inte med IF-mikroskopi på råttvävnad och missas därför om inte ett specifikt SLA-test också utförs. Det är ännu oklart i vilken omfattning de förekommer solitärt, men ett observandum är att anti-SLA rapporteras förekomma i upp till 20 procent av fall med akut leversvikt av oklar genes [6].
Antikroppar mot asialoglykoproteinreceptor (anti-
ASGPR). ASGPR är en receptor som uttrycks på hepatocyters yta och är viktig för eliminationen av galaktosuttryckande (de-sialylerade) proteiner. Anti-ASGPR har rapporterats förekomma i flertalet fall av autoimmun hepatit, och nivån anses avspegla sjukdomsaktiviteten [4].
Ett problem är dock låg sjukdomsspecificitet, eftersom dessa antikroppar också kan påvisas vid primär biliär cirros, virushepatit och andra leversjukdomar. En förklaring kan vara metodologiska svårigheter att ta fram rena receptorproteiner med bevarad antigenstruktur och utan kontamination av andra proteiner. Orent antigen i testen medför risk för att irrelevanta antikroppar också detekteras.
Den låga specificiteten för autoimmun hepatit har hittills inneburit att anti-ASGPR inte används rutinmässigt i diagnostiken.
I en studie av Hausdorf et al presenteras dock data med ett förbättrat ASGPR-test med 78 procents sensitivitet och nästan 100 procents specificitet för autoimmun hepatit [7]. Om dessa fynd bekräftas, kan analys av anti-ASGPR komma att utgöra en viktig diagnostisk markör.
Autoimmun hepatit typ 2
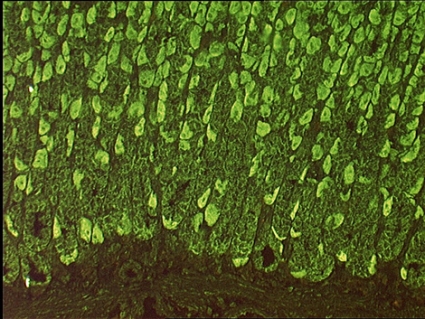
Antikroppar mot »liver kidney microsomes« (anti-LKM-1). Vid autoimmun hepatit typ 2 förekommer oftast inte ANA eller SMA; i stället är anti-LKM-1 typiskt [4]. Dessa autoantikroppar är riktade mot olika epitoper på cytokrom P450 2D6 (CYP2D6). Anti-LKM-1 kan påvisas vid hepatit C, men är då oftast riktade mot andra epitoper, vilket inte kan särskiljas vid IF-mikroskopi. Dessutom kan liknande IF-mönster, utan specificitet för CYP2D6, påvisas vid hepatit D och andra tillstånd. Subtypning med antigenspecifikt test bör därför göras.
Autoantikroppar mot »liver cytosol« typ 1 (anti-LC-1). Anti-LC-1 har påvisats hos ca 30 procent av patienter med autoimmun hepatit typ 2 och kopplar eventuellt till ett allvarligare sjukdomsförlopp [1]. Även om anti-LKM-1 oftast påvisas samtidigt, förekommer anti-LC-1 isolerat hos ca 10 procent. Anti-LC-1 påvisas med antigenspecifikt test, eftersom anti-LKM-1 stör IF-mikroskopibilden. I motsats till de flesta andra autoantikroppar tycks nivån av anti-LC-1 avspegla sjukdomsaktiviteten [4, 8, 9].
Autoantikroppar vid hepatit C. ANA och/eller SMA påvisas hos upp till 50 procent av hepatit C-fallen. Detta gör att samtidig autoimmun hepatit kan misstänkas, vilket försvårar ställningstagande till antiviral behandling med interferon-α, som kan förvärra autoimmun sjukdom. Anti-LKM-1 påvisas i ca 10 procent och kan till viss del förklaras av korsreagerande antikroppar på grund av molekylär likhet mellan CYP2D6 och hepatit C-virus [10]. Även anti-LC-1 har rapporterats i enstaka fall [11].
Primär biliär cirros
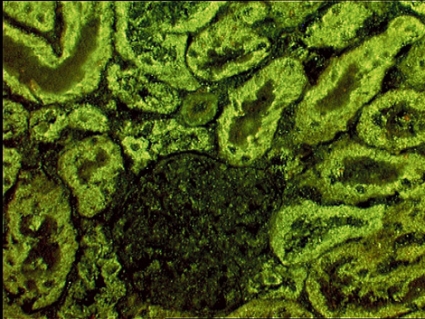
Antimitokondriella antikroppar (AMA) typ M2/M4. AMA typ M2 är en mycket stark diagnostisk markör för primär biliär cirros och påvisas i ca 95 procent av fallen. Autoantikropparna är framför allt riktade mot pyruvatdehydrogenaskomplexet (PDC-E2) i mitokondriernas inre membran, men andra epitoper är också av betydelse. Även i avsaknad av laboratoriemässiga tecken till kolestas förutsäger AMA typ M2 framtida utveckling av primär biliär cirros [12]. Vid IF-mikroskopi på råttvävnad kan AMA typ M2 inte särskiljas från autoantikroppar mot sulfitoxidas (AMA typ M4). Även dessa är en markör för primär biliär cirros, men har inte riktigt lika hög diagnostisk specificitet som AMA typ M2.
M2-specifika test har något högre sensitivitet än IF-mikroskopi och bör utföras vid negativt resultat av IF-mikroskopi om den kliniska misstanken om primär biliär cirros är stark. Ett nyligen utvärderat test med en blandning av PDC-E2 och ytterligare ett par relevanta antigener kunde påvisa primär biliär cirros hos 25 procent av patienterna där IF-mikroskopi och M2-ELISA visat negativa resultat. Om detta fynd bekräftas, kan det bli ett värdefullt diagnostiskt tillskott [13].
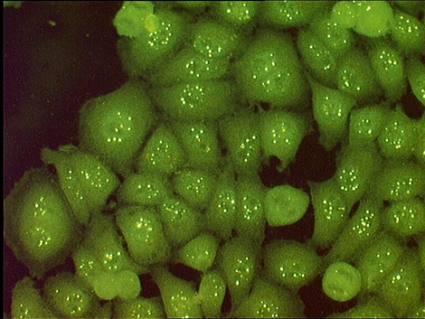
Antinukleära antikroppar (ANA). ANA förekommer i 30–50 procent av fallen med primär biliär cirros, ofta med homogent och/eller kornigt ANA-mönster utan stark sjukdomsassociation [5]. Antikroppar mot centromer ses vid övergångsformer av primär biliär cirros och systemisk skleros. Till skillnad från autoimmun hepatit finns det sjukdomsspecifika ANA-subtyper för primär biliär cirros. Det gäller antikroppar mot kärnmembran, »nuclear pore complex«, med specificitet för 210 kDa glykoprotein (gp210) och 62 kDa nukleoporin (NUP 62). Anti-gp210 predicerar dessutom ett aggressivt sjukdomsförlopp [14]. »Multiple nuclear dots« med specificitet för ett 100 kDa protein (sp100), som beskrivits vid reumatisk systemsjukdom, anses vara en stark diagnostisk markör för primär biliär cirros [15]. Ett observandum är att dessa ANA-specificiteter kan påvisas utan samtidig förekomst av anti-M2.
Primär skleroserande kolangit
Antineutrofila cytoplasmaantikroppar (ANCA). Vid IF-mikroskopi (med etanolfixerade granulocyter som antigenkälla) ger serumprov från patienter med primär skleroserande kolangit eller autoimmun hepatit ofta en perinukleär reaktion (P-ANCA). Ingen sjukdomsassocierad antikroppsspecificitet har påvisats, och tolkningen försvåras av positivt ANA-fynd som ofta inte kan särskiljas från P-ANCA. Fyndet har låg klinisk relevans.
Perifera neutrofilspecifika ANA (P-ANNA). P-ANNA är riktade mot hittills okänt antigen i granulocyternas kärnmembran och påvisas med IF-mikroskopi på formalinfixerade granulocyter. De förekommer ofta vid primär skleroserande kolangit och autoimmun hepatit, men kan även ses vid andra tillstånd, och det kliniska värdet är därför begränsat [16].
Metodologiska fallgropar
En utbredd missuppfattning är att SMA-, AMA- och ANA-titrar vid IF-mikroskopi är likvärdiga mellan olika laboratorier. Ett och samma serumprov kan dock ge helt olika »titrar« vid olika laboratorier på grund av metodologiska skillnader. Det är därför olyckligt att SMA- och/eller ANA-titer utgör en av hörnpelarna i de internationella diagnostiska kriterierna för autoimmun hepatit. Fynd av ANA och/eller SMA i låga nivåer är vanligt hos friska personer, och för att undvika falskt positiva resultat måste varje laboratorium utforma sin metod så att högst 5 procent av ett normalmaterial blir positivt.
Endast autoantikroppar av IgG-klass ska påvisas, eftersom autoantikroppar av IgA- och IgM-klass har låg klinisk relevans. Detektionsantikroppar som inte är strikt IgG-specifika ska därför undvikas.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.