Sammanfattat
Patienter med svårt skov av ulcerös kolit bör vårdas på sjukhus och handläggas av gastroenterolog och kolorektal kirurg i nära samarbete.
Skovets svårighetsgrad kan underskattas, varför noggrann bedömning av inflammationens utbredning och svårighetsgrad enligt validerade kriterier är viktigt.
Intravenös behandling med kortikosteroider är en av hörnstenarna i den akuta behandlingen.
Patienter som inte förbättras på denna behandling, bör erbjudas medicinsk »rescue-behandling« eller kolektomi.
Infliximab har visats vara en effektiv rescue-behandling och kan minska behovet av kolektomi inom de första 3 månaderna och upp till 3 år.
Ulcerös kolit har oftast ett kroniskt intermittent förlopp, där perioder av ökad sjukdomsaktivitet växlar med perioder av besvärsfrihet. Svårighetsgraden av ett skov indelas traditionellt i lindrigt, måttligt svårt och svårt skov [1, 2]. Omkring 15 procent av patienterna drabbas någon gång under sjukdomsförloppet av ett svårt skov, vilket ibland kan vara debutsymtomet.
Ett svårt skov hade under 1930- och 1940-talen mycket hög mortalitet, 30–40 procent. Med förbättrad medicinsk behandling, framför allt efter införandet av kortikosteroider under 1950-talet samt tidig kolektomi vid medicinsk terapisvikt, sjönk mortaliteten och understiger i dag 1 procent. Kolektomifrekvensen vid svårt skov har trots dessa framsteg förblivit oförändrad, omkring 30 procent [3].
Nya medicinska behandlingsalternativ har introducerats under de senaste åren, och avsikten med denna översikt är att belysa det kliniska omhändertagandet av patienter med svårt skov av ulcerös kolit.
Arbetet utgår från en arbetsgrupp inom Svensk gastroenterologisk förening (SGF) och Swedish Organisation for the Study of Inflammatory Bowel Disease (SOIBD).
Klinik
Blodtillblandad diarré är huvudsymtomet vid aktiv ulcerös kolit. Vanligtvis insjuknar patienterna med successivt förvärrade symtom under några veckors tid, men ibland kan en mera akut debut ses. Tenesmer, dvs smärtsamma trängningar till avföring, är ett vanligt symtom även vid ett lindrigt skov, medan mera uttalad buksmärta, feber och viktförlust tyder på ett svårt skov.
Patienter med svårt skov bör vårdas inneliggande på sjukhus [4]. Ett svårt skov kan snabbt övergå i ett allvarligt tillstånd med feber, anemi, vätske- och elektrolytförluster, och livshotande komplikationer kan tillstöta som toxisk dilatation och tarmperforation. Trots svår kolit kan patienterna te sig anmärkningsvärt opåverkade, och sjukdomens svårighetsgrad kan därför lätt underskattas. En noggrann kartläggning av inflammationens utbredning och svårighetsgrad enligt väl validerade kriterier samt fortlöpande monitorering av kliniskt förlopp och svar på insatt behandling utgör därför hörnstenar i optimal handläggning av patienterna.
Aktivitetsindex, prognostiska index, klinisk övervakning
Sjukdomens svårighetsgrad bedöms med enkla kliniska parametrar och laboratorieparametrar. Truelove och Witts [5] presenterade redan 1955 ett index för att klassificera svårighetsgraden av ulcerös kolit, vilket sedermera har modifierats något (Fakta) [2].
Andra mera komplexa index har utvecklats för att möjliggöra bedömning av sjukdomsaktiviteten över tid, speciellt i förhållande till inledd behandling [6]. Det mest använda av dessa är Seo-index [7], i vilket man bedömer sjukdomens svårighetsgrad med utgångspunkt i fem oberoende faktorer: blodtillblandad avföring, antalet tarmtömningar, SR, Hb och serumalbumin.
Övervakningen av en inneliggande patient med ett svårt skov bör omfatta daglig registrering av allmäntillstånd, temperatur, hjärtfrekvens, bukstatus, antal avföringar, förekomst av blod i avföringen, Hb, C-reaktivt protein (CRP), SR, albumin och trombocyter. Röntgen buköversikt görs initialt och upprepas vid behov (se nedan). För att skärpa det prognostiska värdet av registreringen av avföringsfrekvens rekommenderas fasta och parenteral vätske- och näringstillförsel under de första dygnen.
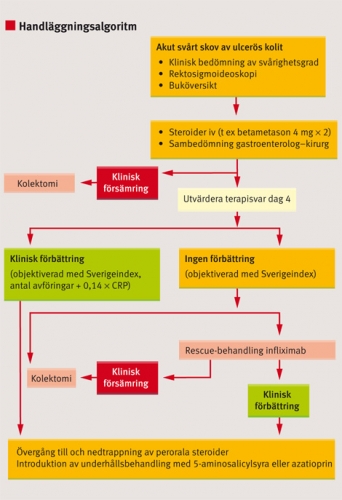
Det kliniska svaret efter de tre första dagarnas intravenösa steroidbehandling ger god prognostisk information om huruvida tarmsjukdomen kommer att gå i remission eller inte. Fortsatt lätt förhöjning av kroppstemperaturen, oförändrad avföringsfrekvens med blodtillblandning och kvarvarande CRP-stegring efter 3 dagar är prognostiskt ogynnsamt och indikerar ett dåligt svar på insatt behandling [8, 9]. Antalet tarmtömningar och CRP-värdet på det 3:e dygnet efter insatt behandling kan kombineras i ett index (»Sverigeindex« = antalet tarmtömningar + 0,14 × CRP [mg/l]). Vid ett indexvärde <8 är risken 16 procent för att en patient behöver genomgå kolektomi inom 30 dagar, medan risken för behov av kolektomi vid indexvärde >8 är 72 procent [8]. I dessa fall bör annan medicinsk behandling, s k rescue-behandling, eller kolektomi övervägas (Figur 1).
Diagnostik
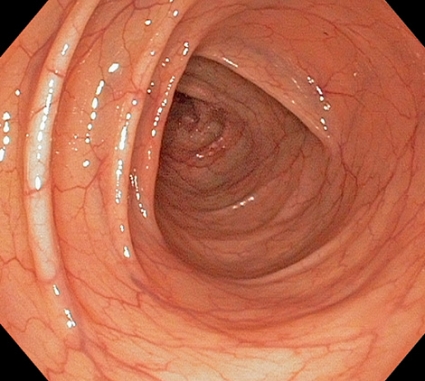
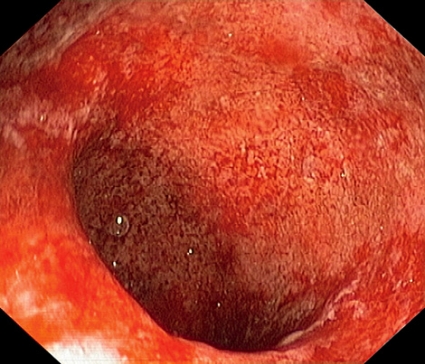
Endoskopi. Endoskopi är referensmetod för att värdera tarminflammationens intensitet och utbredning (Figur 2). Utbredningen indelas i proktit (makroskopisk inflammation omfattande de nedre 15 cm av rektum), distal kolit (inflammation upp till vänster kolonflexur) eller extensiv kolit (inflammation proximalt om vänster flexur) [1, 2]. Majoriteten av patienter med svårt skov har extensiv utbredning av inflammationen. Olika graderingar av de endoskopiska fynden har föreslagits [6]. Svårare förändringar som djupa ulcerationer eller avstött slemhinna indikerar en allvarlig tarminflammation (Figur 2).
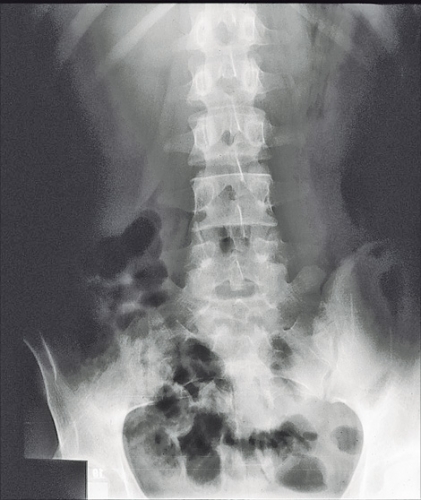
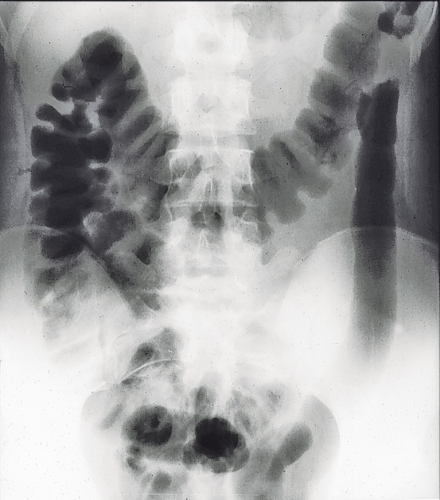
Radiologi. Röntgen buköversikt görs för att utesluta dilatation och perforation av tarmen men kan även ge en viss uppfattning om inflammationens utbredning och förekomst av djupa ulcerationer i slemhinnan (Figur 3). En mera noggrann bedömning av slemhinnan kan erhållas med s k luftkolonröntgen, som kan göras i direkt anslutning till röntgen buköversikt. Efter det att dilatation och perforation uteslutits blåses luft under genomlysning försiktigt upp i kolon genom en kateter inlagd i rektum. En normal luftkolonundersökning utesluter med stor sannolikhet svår och djup inflammation i kolon (prediktivt värde 0,86). Metoden underskattar utbredningen av lätt till måttlig inflammation jämfört med såväl endoskopi som leukocytscintigrafi, medan metoderna sinsemellan väl överensstämmer när det gäller att påvisa svårare grader av inflammation [10-12].
Kolonröntgen, såväl enkelkontrast som dubbelkontrast, har ingen plats i diagnostiken utan är snarast kontraindicerad vid ett svårt skov av ulcerös kolit.
Leukocytskintigrafi. Indikationen för leukocytskintigrafi är i första hand att bedöma utbredningen av tarminflammationen. Patienter som är svårundersökta med andra tekniker, t ex barn, lämpar sig väl för denna metod, som har fördelar genom att vara icke-invasiv och ge mindre strålbelastning än konventionell röntgenundersökning samt att både tunntarm och grovtarm kan undersökas vid samma undersökningstillfälle [13].
Praktisk användning av diagnostiska metoder
På varje patient som söker för akut ulcerös kolit ska rektoskopi, eller med fördel flexibel rektosigmoideoskopi, och buköversikt omedelbart utföras. Vid behov av ytterligare information om utbredningen kan kompletterande luftkolonundersökning utföras. Tillsammans med den kliniska bedömningen ger dessa metoder tillräckligt underlag för att bedöma sjukdomens utbredning och svårighetsgrad så att behandling kan påbörjas. Leukocytskintigrafi kan vara av värde vid svårbedömda fynd. Upprepade buköversikter, ibland dagligen, är nödvändigt om patienten inte visar tecken på förbättring eller försämras trots behandling.
Koloskopi av patienter med akut kolit är i vana händer inte belastad med ökad komplikationsrisk och kan med stor försiktighet utföras för att värdera läkningsförloppet hos patienter som inte svarar adekvat på den initiala behandlingen [14, 15]. Ambitionen är då inte att göra en totalkoloskopi, utan även en begränsad endoskopisk undersökning kan ge värdefull information.
Differentialdiagnoser
Andra orsaker till blodig diarré måste alltid övervägas. Infektiös kolit orsakad av Campylobacter, Salmonella, Shigella, Yersinia eller Clostridium difficile måste alltid uteslutas med fecesodlingar och analys av Clostridium difficile-cytotoxin. Symtomen vid infektiös kolit liknar dem vid akut ulcerös kolit, men insjuknandet är ofta mer abrupt, och feber förekommer tidigt i förloppet. Histologisk undersökning av biopsier från tjocktarmsslemhinnan kan ge ytterligare vägledning i differentialdiagnostiken [16]. En bakteriell infektion kan utlösa ett skov av ulcerös kolit, vilket bör övervägas om det kliniska förloppet vid infektiös diarré avviker från det förväntade. Provtagning avseende enterohemorragisk E coli (EHEC), Entamoeba histolytica eller cytomegalovirus bör göras i speciella kliniska situationer.
Hos äldre personer är ischemisk kolit, som oftast engagerar slemhinnan omkring vänster flexur och colon descendens, en viktig differentialdiagnos.
Vid det första skovet kan det vara svårt att skilja ulcerös kolit från Crohns sjukdom och obestämbar kolit. Eftersom behandlingen i det akuta skedet av dessa tillstånd är densamma, är denna differentialdiagnostik av underordnad betydelse initialt.
Medicinsk behandling
Kortikosteroider. Kortison är en av hörnstenarna i behandlingen av akut ulcerös kolit (evidensstyrka 1, rekommendationsgrad A). Det är viktigt att inledningen av adekvat kortisonbehandling inte försenas i avvaktan på mikrobiologiska analyssvar. De första jämförande studierna på 1960-talet visade att 20 mg prednisolon var underlägset både 40 mg och 60 mg, medan 60 mg gav mer biverkningar. I dag används betametason 8 mg/dag eller andra kortikosteroider i ekvipotenta doser, som ges intravenöst under minst 5 dagar. Högre steroiddos eller intravenös behandlingstid överstigande 10 dagar har inte visats ge bättre klinisk effekt [17]. Vid ett svårt skov kan man förvänta sig att omkring hälften av patienterna uppnår remission på steroidbehandling, ytterligare en andel förbättras långsamt, medan resterande 30 procent är steroidresistenta och blir aktuella för »rescue-behandling« eller kolektomi [3, 9, 17, 18].
Ciklosporin, takrolimus. Ciklosporin introducerades 1994 som intravenös rescue-behandling vid steroidresistent, svår ulcerös kolit och har internationellt fått genomslag men haft begränsad användning i Sverige. Bland allvarliga biverkningar, varav en del är letala, noteras opportunistiska infektioner, sepsis, njurpåverkan, hypertoni och grand mal-anfall. Kortsiktigt svarar 51–80 procent av patienterna på ciklosporin [4], men recidivfrekvensen är hög, och efter 5–6 år har majoriteten av patienterna genomgått kolektomi [19, 20]. En Cochrane-sammanfattning konkluderar att evidens saknas för att ciklosporin är mer effektivt än standardbehandling vid akut ulcerös kolit [21].
Takrolimus har samma biverkningsprofil som ciklosporin. Evidens saknas för behandling med takrolimus vid svårt skov av ulcerös kolit [4, 22].
Infliximab. Tumörnekrosfaktor-α (TNF) är ett proinflammatoriskt cytokin med central betydelse för inflammationen vid både Crohns sjukdom och ulcerös kolit. Infliximab, som är en anti-TNF-antikropp, är en etablerad behandling vid svår Crohns sjukdom. Under de senaste åren har studier visat att infliximab är effektivt även vid behandling av ulcerös kolit (evidensstyrka 2, rekommendationsgrad B). I dag finns sju kontrollerade studier av infliximab vid ulcerös kolit [23-28]. Studierna är heterogena avseende inklusionskriterier, dosering och effektmått och därmed inte inbördes jämförbara. I fyra av dessa studier sågs ingen eller endast marginell fördel för infliximabbehandling [23, 25, 26, 28].
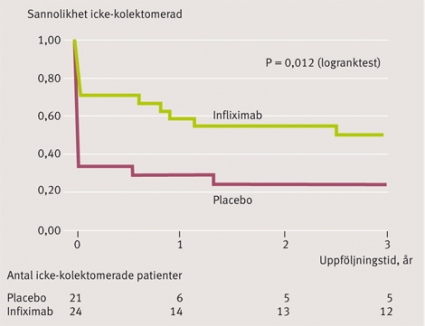
Resultaten från en svensk-dansk studie, där infliximab gavs som rescue-behandling vid svårt terapiresistent skov av ulcerös kolit, visade tydligt nyttan av denna tilläggsbehandling [24]. Efter tre dagars inledande behandling med betametason 8 mg/dag randomiserades 45 patienter, som uppfyllde kriterier på terapisvikt, till en engångsinfusion av infliximab 5 mg/kg eller placebo. Efter 3 månader var signifikant färre i infliximabgruppen (29 procent) opererade än i placebogruppen (67 procent) (Figur 4). En Cochrane-översikt konkluderar att vid svårt skov av ulcerös kolit halverar infliximab behovet av kolektomi under 90 dagar [29]. En uppföljningsstudie visar att en signifikant skillnad i operationsfrekvens kvarstår även efter 3 år till infliximabbehandlade patienters fördel (Figur 4) [30]. Ytterligare studier med större patientmaterial krävs dock för att definiera optimal dosering och visa den långsiktiga effekten av infliximab som rescue-behandling.
Infliximabs effekt vid ulcerös kolit har vidare visats i två stora studier, ACT 1 och ACT 2 (Active ulcerative colitis trials), som vardera inkluderade 364 patienter [27]. Dessa patienter skiljer sig från patienterna i den svensk-danska studien genom att ha en kronisk, steroidberoende sjukdom och inte ett svårt skov av ulcerös kolit. I studierna randomiserades de till kontinuerlig underhållsbehandling med infliximab 5 mg/kg kroppsvikt, infliximab 10 mg/kg kroppsvikt eller placebo. Signifikant fler infliximabbehandlade patienter än placebobehandlade var i klinisk remission efter 30 respektive 54 veckor.
Av de olika anti-TNF-preparaten är det endast infliximab som i dag är godkänt på indikationen ulcerös kolit.
Hos patienter som svarar på rescue-behandling ses oftast en snar klinisk förbättring. Vid försämring eller utebliven förbättring inom 4 till 5 dagar efter inledandet av rescue-behandling bör kolektomi övervägas (otillräckligt vetenskapligt underlag). Biverkningar som akuta infusionsreaktioner och serumsjukeliknande tillstånd ses på grund av infliximabs immunogenitet. Risk för opportunistiska infektioner och aktivering av latent tuberkulos föreligger på grund av medlets immunsupprimerande effekt.
Understödjande medicinsk behandling. Det är viktigt att korrigera anemi, vätske- och elektrolytrubbningar och att tillgodose en adekvat nutrition under sjukdomsförloppet. Med tarmvila och parenteral nutrition minskar patientens lösa avföringar jämfört med vid intag av vanlig kost. Tarminflammationen och utgången av ett svårt skov påverkas däremot inte av tarmvila [31, 32]. Parenteral nutrition kan med fördel ges i perifer ven i flertalet fall, och central venkateter bör om möjligt undvikas på grund av risk för komplikationer. Enteral nutrition har visats likvärdig med parenteral nutrition och har färre biverkningar och lägre risk för postoperativa infektioner [33].
Risken för tromboemboliska komplikationer är ökad vid aktiv ulcerös kolit [34, 35], varför sedvanlig trombosprofylax med lågmolekylärt heparin rekommenderas (otillräckligt vetenskapligt underlag) [4, 36]. Heparin har även föreslagits som behandling vid aktiv ulcerös kolit, men en metaanalys har inte påvisat någon effekt av vare sig ofraktionerat eller lågmolekylärt heparin [37].
Antibiotika ska inte ges rutinmässigt (evidensstyrka 1, rekommendationsgrad A). I randomiserade studier har varken ciprofloxacin, metronidazol, tobramycin, vankomycin eller rifamycin haft någon övertygande tilläggseffekt utöver standardbehandling [38]. Antibiotika har en given plats i speciella situationer som perforation eller dilatation av kolon eller vid insjuknande i nära anslutning till utlandsresa. Vid ett svårt skov som inte svarar på steroidbehandling kan reaktiverad cytomegalovirusinfektion övervägas, vilket beskrivits förekomma hos upp till 30 procent av »steroidrefraktära« patienter [39]. Det är dock oklart om cytomegalovirusinfektionen är enbart ett epifenomen eller om den har kausal betydelse för tarminflammationen. I dag saknas evidens för att antiviral behandling påverkar sjukdomsförloppet, och kontrollerade studier är nödvändiga [40, 41].
Antikolinergika, loperamid, opioider och NSAID bör inte ges under akut skov, eftersom de kan förvärra tillståndet och utlösa en toxisk kolondilatation (evidensstyrka 3, rekommendationsgrad C).
Leukocytaferes
Leukocytaferes har använts framför allt i Japan, och i små, okontrollerade studier har hög respons- och remissionsfrekvens rapporterats vid steroidberoende eller steroidrefraktär kronisk ulcerös kolit. I en kontrollerad studie randomiserades 215 patienter med måttligt svår eller svår kronisk ulcerös kolit till behandling med antingen leukocytaferes eller sham-behandling [42]. Efter 10 behandlingar givna under 9 veckors tid kunde ingen skillnad påvisas mellan de två grupperna avseende klinisk remission eller klinisk förbättring.
Kirurgisk behandling
Patienten måste tidigt informeras om att kolektomi kan bli nödvändig och är ett alternativ till den medicinska behandlingen. Ett nära samarbete mellan gastroenterolog och kolorektal kirurg är därför viktigt vid bedömning av den kliniska utvecklingen efter insatt behandling så att tidpunkten för en operation blir optimal. Målet är att rädda patientens liv – inte bara att rädda tarmen, och den medicinska terapin får därför inte försena en adekvat kirurgisk åtgärd. Indikationerna för kirurgi är svårt skov som inte svarat på medicinsk behandling, komplikationer i form av toxisk kolondilatation, hotande eller manifest tarmperforation samt akut svår kolorektal blödning [4]. Vid försämring eller utebliven förbättring inom 4 till 5 dagar efter inledandet av rescue-behandling bör kolektomi också rekommenderas.
Den rekommenderade operationen är kolektomi och ileostomi med bevarad rektum [4]. Efter ett halvt år utförs den rekonstruktion som har beslutats i samråd med patienten, vilket innebär antingen proktektomi med bäckenreservoar eller ileorektalanastomos. Alternativt behålls en permanent ileostomi.
Underhållsbehandling
Recidivrisken vid ulcerös kolit är hög oberoende av svårighetsgrad. Inom 1 år får omkring 70 procent av patienterna ett återfall om inte förebyggande underhållsbehandling ges. Syftet med denna är att patienten ska bibehålla klinisk och endoskopisk remission och inte ha behandling med kortikosteroider. Underhållsbehandling med 5-aminosalicylsyra eller sulfasalazin reducerar recidivrisken till hälften, och patienten bör rekommenderas livslång sådan terapi (evidensstyrka 1, rekommendationsgrad A) [43]. Immunsuppressiv behandling med azatioprin eller 6-merkaptopurin rekommenderas vid steroidberoende ulcerös kolit, vid frekventa recidiv trots underhållsbehandling med 5-aminosalicylsyra eller vid intolerans mot dessa medel [4, 44, 45].
Prognos
Med adekvat behandling är mortaliteten vid svårt skov av ulcerös kolit i dag <1 procent, medan kolektomifrekvensen sedan länge har varit oförändrad, omkring 30 procent [3]. I en långtidsuppföljning av patienter med ett svårt skov, vilka haft recidivprofylaktisk behandling med enbart sulfasalazin eller 5-aminosalicylsyra, var operationsfrekvensen 64 procent efter 10 år, vilket belyser vikten av effektiv underhållsbehandling [46].
Framsteg i den medicinska behandlingen har minskat behovet av akut kolektomi. Fortsatta studier krävs dock för att fastställa den bästa rescue-behandlingen vid svårt skov av steroidrefraktär ulcerös kolit och den optimala efterföljande underhållsbehandlingen.Potentiella bindningar eller jävsförhållanden: Curt Tysk har fått föreläsararvode från Astra-Zeneca och Schering-Plough, Ragnar Befrits och Stefan Lindgren har fått föreläsararvode från Schering-Plough, Erik Hertervig har fått föreläsararvode från Abbott och Schering-Plough.