Sammanfattat
Hälsoekonomi handlar om hur man kan få ut största möjliga hälsa för tillgängliga resurser. Slutprodukten av en ekonomisk utvärdering är den inkrementella kostnadseffektkvoten, som är kostnaden för att erhålla en effektenhet av en behandling jämfört med en annan.
Den årliga kostnaden för osteoporos i Sverige har beräknats till 4,6 miljarder kronor, inkluderat alla samhällsrelevanta kostnader som kan relateras till första året efter en fraktur.
Andelen kvinnor med osteoporos är betydligt högre än andelen kvinnor som skulle kunna få behandling, vilket indikerar ett tydligt gap mellan faktisk förskrivning och behandlingsbehov.
Genom att kombinera kostnadseffektanalys och en bredare riskprofilbedömning skulle identifiering av patienter med hög frakturrisk som är lämpliga för behandling förenklas och förbättras både i ett kliniskt och ett hälsoekonomiskt perspektiv.
Hälsoekonomi handlar om hur man kan få ut största möjliga hälsa för tillgängliga resurser. Hälsoekonomiska utvärderingar har blivit ett allt viktigare verktyg i beslutsfattandet vad gäller subventionering av nya läkemedel i Sverige. För att ge vägledning om vilka behandlingar som bör väljas i en viss patientgrupp måste kostnader och hälsoeffekter ställas mot varandra. Ofta är nyare behandlingar mer effektiva än äldre – men till ett högre pris. Frågan är om det högre priset kan motiveras av förbättrade hälsoeffekter och minskade sjukdomskostnader.
Slutprodukten av en ekonomisk utvärdering är den inkrementella kostnadseffektkvoten, som är kostnaden för att erhålla en effektenhet av en behandling jämfört med en annan. Den vanligaste effektenheten är det kvalitetsjusterade levnadsåret (QALY), som inkluderar både mortalitets- och morbiditetsaspekter av en behandling.
Frakturer och förlust av livskvalitet
Osteoporos orsakar mer än 70000 frakturer årligen i Sverige. Frakturerna leder inte bara till försämrad hälsa för patienten utan också till höga samhällskostnader. Den årliga kostnaden för osteoporos i Sverige har beräknats till 4,6 miljarder kronor [1], inkluderat alla samhällsrelevanta kostnader som kan relateras till en fraktur, dvs kostnader för hälso- och sjukvård, anhörigvård och produktionsförluster. Dessa estimat är dock underskattningar av den reella kostnaden, då de endast inkluderar kostnaderna relaterade till höft-, kot- och handledsfrakturer det första året efter fraktur.
En annan aspekt som borde tas med i ett samhällsperspektiv är värdet av den livskvalitetsförlust som frakturer orsaker: Osteoporosrelaterade frakturer beräknas ge en förlust på 9050 kvalitetsjusterade levnadsår (QALY) per år [1]. Det finns inget specifikt värde på ett QALY i Sverige, men i olika studier har värdet beräknats till ca 220 000–650 000 kr [2, 3]. Baserat på dessa skattningar skulle det totala värdet av förlorade frakturrelaterade QALY vara 2–5,9 miljarder kronor per år.
Behandlingarnas kostnadseffektivitet
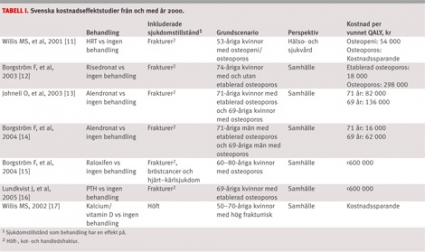
I Sverige har ett antal kostnadseffektstudier av osteoporosbehandlingar utförts de senaste åren [1]. I Tabell I sammanfattas alla publicerade studier från och med år 2000. I de sju studierna utvärderades bisfosfonater i tre och hormonell substitutionsterapi (HRT), raloxifen, paratyreoideahormon (PTH) och kalcium/vitamin D i en vardera. Kostnaden per vunnet QALY i grundscenarierna i de sju studierna varierar mellan kostnadssparande (dvs ena behandlingsalternativet ger bättre effekt och lägre kostnader) och ca 600000 kronor.
Det är dock svårt att dra slutsatser om vilket läkemedel som är det mest kostnadseffektiva, då samtliga studier jämför en läkemedelsbehandling med ingen behandling och patientgrupperna varierar. Den främsta anledningen till detta är att det inte finns några kliniska studier som har undersökt den relativa effekten på frakturrisk av de olika läkemedlen. Studien som undersöker HRT baseras på effektdata som fanns innan resultat från Women´s Health Initiative blev tillgängliga, vilket gör denna analys något inaktuell.
En jämförelse mellan de olika läkemedelsklasserna tyder dock på en genomgående lägre kostnadseffektkvot för bisfosfonater än för övriga läkemedel – HRT och kalcium/vitamin D undantagna. Skälet till att bisfosfonater har bättre kostnadseffektivitet är att de har uppvisat en signifikant riskminskning för höftfrakturer i kliniska studier. Dessa resultat avspeglas också i rådande behandlingsriktlinjer [4], där bisfosfonater är förstahandsval och övriga läkemedel är andrahandsval.
Behandlingsmönster i Sverige
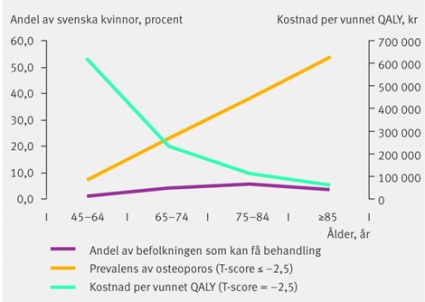
Baserat på läkemedelsförsäljning och definierade dygnsdoser (DDD) kan man beräkna andelen av befolkningen som skulle kunna behandlas med osteoporosläkemedel. I Figur 1 visas den åldersdifferentierade andelen av kvinnor i Sverige som potentiellt skulle kunna behandlas med bisfosfonater, raloxifen och PTH – baserat på 2004 års läkemedelsförsäljning. Som högst skulle 5,6 procent av den kvinnliga befolkningen i åldern 75–84 år få behandling med något av nämnda läkemedel.
Man kan relatera dessa siffror till andelen kvinnor i Sverige som kan beräknas ha osteoporos (dvs T-score ≤–2,5) och som skulle kunna vara kandidater för osteoporosbehandling. Som framgår av figuren är andelen kvinnor med osteoporos betydligt högre än andelen kvinnor som skulle kunna få behandling, enligt rådande läkemedelsförsäljning, vilket indikerar ett tydligt gap mellan faktisk förskrivning och patienter med behandlingsbehov.
En annan fråga är om det skulle vara kostnadseffektivt att behandla fler kvinnor med osteoporos. Figur 1 visar att behandling med en bisfosfonat skulle kunna vara kostnadseffektiv för alla kvinnor som har osteoporos och är 50 år eller äldre. För att kunna behandla alla med diagnosen osteoporos behöver dessa personer dock identifieras, tex med ett bentäthetsscreeningprogram, vilket skulle innebära en kostnad som skulle påverka kostnadseffektiviteten. Ett annat alternativ är att inrikta sig på patienter med riskfaktorer, exempelvis dem med tidigare fragilitetsfraktur.
Nya verktyg för beräkning av riskfaktorer
Idag ges oftast behandling till patienter som anses ha hög frakturrisk, baserat på låg bentäthet och tidigare frakturer. Det finns dock andra riskfaktorer som skulle kunna användas för en mer komplett bedömning av en patients frakturrisk. Med hjälp av en bredare riskprofilbedömning kan en starkare indikation för osteoporosbehandling säkerställas.
I ett pågående arbete inom WHO [5, 6] utvecklas en individuell frakturriskalgoritm med vilken man kommer att kunna beräkna patienters absoluta 10-årsrisk för fraktur, baserat på deras totala frakturriskprofil. Parallellt med detta arbete utvecklas även ett hälsoekonomiskt verktyg med vilket man kan beräkna vid vilken absolut 10-års risk för fraktur det kan vara kostnadseffektivt att initiera osteoporosbehandling, även kallat interventionströskelvärde [1, 7-10].
Genom att kombinera dessa två verktyg skulle identifiering av patienter med hög frakturrisk och som är lämpliga för behandling förenklas och förbättras både i kliniskt och hälsoekonomiskt perspektiv. Om dessa två instrument kunde utnyttjas i större skala inom vården skulle det påvisade behandlingsgapet kunna minskas utan alltför höga kostnader för att hitta de patienter med hög frakturrisk som borde få osteoporosbehandling.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.