Sammanfattat
Flertalet patienter på ett äldreboende har nedsatt njurfunktion. Detta åskådliggörs dåligt om man utgår endast från S-kreatinin, som i de flesta fall är normalt eller endast lätt förhöjt.
Resultaten från denna studie talar för att S-cystatin C bör användas som rutinmetod för att spegla njurfunktionen hos äldre personer.
En ökad medvetenhet om nedsatt njurfunktion skulle ge underlag för bättre läkemedelsordinationer (dosjustera/byta läkemedel som huvudsakligen utsöndras renalt) och därigenom minskad risk för läkemedelsrelaterade biverkningar hos våra äldre patienter.
Nedsatt njurfunktion påverkar farmakokinetiken främst hos de läkemedel som utsöndras oförändrade via njurarna. Om dessa ges i normal dos erhålls en högre plasmakoncentration, och risken för biverkningar och överdoseringar ökar. Generellt är läkemedel som utsöndras oförändrade till mer än 70 procent via njurarna aktuella för dosjustering vid nedsatt njurfunktion. Till denna grupp hör många vattenlösliga läkemedel, till exempel penicilliner, cefalosporiner, aminoglykosider och digoxin.
Dosreduktion av läkemedel kan ske genom att förlänga intervallet mellan doserna, genom att minska varje enskild dos eller både–och. I vissa fall kan även en dosökning krävas vid nedsatt njurfunktion, till exempel vid behandling med furosemid.
Börjar sjunka vid 20 års ålder
Hög ålder är den vanligaste orsaken till nedsatt njurfunktion. Den glomerulära filtrationshastigheten (GFR), som är det bästa måttet på njurfunktion [3], börjar sjunka hos människan vid 20 års ålder. Vid 75 års ålder har GFR reducerats med ca 50 procent. Den metod som används i primärvården för att mäta och åskådliggöra nedsatt njurfunktion är S-kreatinin och att eventuellt härifrån uppskatta GFR med hjälp av Cockcroft–Gaults ekvation.
S-kreatinin har felkällor särskilt hos äldre. Med en minskad muskelmassa, normalt åldrande och malnutrition följer en sänkt kreatininbildning. Värdena på S-kreatinin kan därför hålla sig inom det normala ganska länge hos äldre, trots att GFR kan vara kraftigt sänkt [3].
Det finns andra metoder som är bättre än Cockcroft–Gaults ekvation på att uppskatta GFR och som utöver S-kreatinin, ålder och kön även tar hänsyn till etnicitet, urea- och albuminkoncentrationer och kroppsyta [4].
I syfte att förbättra och förenkla diagnostiken av nedsatt njurfunktion har en ny mätmetod introducerats under de senaste åren, S-cystatin C [3, 5].
Cystatin C är ett lågmolekylärt protein som produceras med en jämn hastighet i alla kärnförande celler i kroppen . Serumcystatin C påverkas inte av födointag, kön, vikt eller muskelmassa, vilket är positivt när det gäller mätningar på barn och äldre [6]. Serumhalten påverkas inte heller av andra sjukdomar än nedsatt njurfunktion, men mycket stora doser av glukokortikoider och påverkad tyreoideafunktion kan påverka produktionen av cystatin C [5] och därigenom serumhalten. I en normalt fungerande njure elimineras cystatin C via glomerulär filtration, reabsorberas och bryts sedan ner i det närmaste fullständigt i proximala tubuli. Koncentrationen av cystatin C i serum stiger vid nedsatt glomerulär filtrationshastighet.
Har högre sensitivitet
Ett flertal studier av diagnostisk tillförlitlighet visar att S-cystatin C har högre sensitivitet och specificitet än plasmakreatinin att upptäcka reducerad njurfunktion mätt med clearancemetodik [7]. Detta innebär att metoden är mer lämplig att använda vid screening.
Ett flertal studier har visat mycket god korrelation mellan GFR och S-cystatin C [3]. I en svensk studie var korrelationen mellan S-cystatin C och iohexol god (P0,0001) vilket också talar för att S-cystatin C skulle kunna vara en bra markör för GFR [8].
Syfte att analysera läkemedelsbehandlingen
Syftet med denna studie var att kartlägga och åskådliggöra njurfunktionen (GFR) hos boende på ett äldreboende i Jönköpings kommun och analysera om olämplig läkemedelsbehandling förekom som följd av att patienter med nedsatt njurfunktion inte identifierats med den vanliga analysmetoden (S-kreatinin).
Metod
Studien genomfördes under våren 2005 på ett särskilt boende för äldre (SÄBO) i Jönköpings kommun. Boendet har 60 platser, varav 10 är kortvårdsplatser för patienter som till exempel varit inlagda på sjukhus och inte kan flyttas direkt hem.
Blodprov kunde tas av sjuksköterskan på boendet under april 2005 på 50 av de 51 patienter som ville delta. Proven skickades till laboratoriet på Länssjukhuset Ryhov i Jönköping för bestämning av serumkoncentrationerna av kreatinin respektive cystatin C. S-kreatinin mättes genom användning av Jaffés metod, och S-cystatin C fastställdes genom immunoturbidimetrisk metod (Dako Cytomation) med analysinstrumentet ADVIA 1650 från Bayer, USA. Patienternas ålder, kön och vikt noterades. Beräkningar av GFR gjordes på laboratoriet.
Kreatininclearance (GFR) beräknades med hjälp av Cockcroft–Gaults formel, GFR=1,23 x (140–ålder i år) x vikt i kg/ S-kreatinin ( x 0,85 för kvinnor), och för S-cystatin C användes formeln, GFRcystatin C ( ml/min/1,73 kvm)= 69,378 x cystatin C (mg/l)–1,6605. Denna formel har skapats via analys av cystatin C på 49 patientprov vid iohexolbelastning i Jönköping och stämmer i stort med formel som beräknats på större patientmaterial [9].
Fyrtioåtta patienters läkemedelslistor gicks igenom och bedömdes av en receptariestudent utifrån »Riktlinjer för dosering av läkemedel vid nedsatt njurfunktion« ur Läkemedelsboken 2001/2002 och Fass 2005.
De framkomna teoretiskt olämpliga läkemedelsordinationerna granskades därefter av en oberoende distriktsläkare och en njurläkare, som tog ställning till vad som var praktiskt olämpliga läkemedelsordinationer. Kontakt togs också med Läkemedelsverkets experter (N Feltelius och B Ljungberg) för klarläggande angående Trombyl och Fass-uppgift om kontraindikation vid GFR 30 ml/min.
Resultat
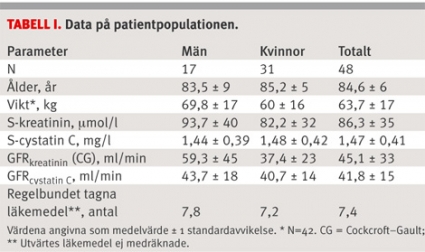
Av 59 boende ville 51 medverka i studien. Tre patienter föll bort, två på grund av inaktuell läkemedelslista och en på grund av svårigheter att ta prov. Av de återstående 48 personerna var 31 kvinnor och 17 män. Sex av de boende gick av praktiska skäl inte att väga, för dessa gick GFR inte att räkna ut från S-kreatinin. Deskriptiva data på inkluderade patienter återfinns i Tabell I.
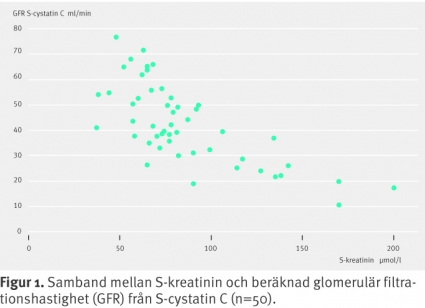
Njurfunktionen mätt med S-kreatinin överensstämde dåligt med GFR uträknat från S-cystatin C (Figur 1). En stor del av patienterna med GFR 40 ml/min hade ett normalt S-kreatinin.
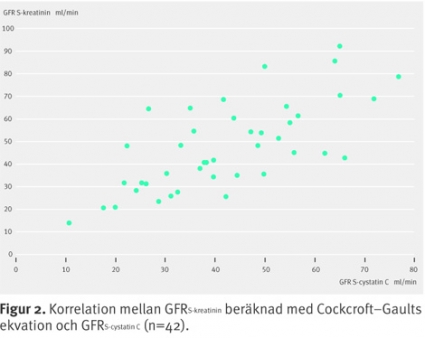
Om man räknar om S-kreatinin till GFR enligt Cockcroft–Gaults formel blev överensstämmelsen bättre. Korrelationen mellan GFR beräknat med hjälp av S-kreatinin och GFR från S-cystatin C var 0,71 (Figur 2).
Ett antal teoretiskt olämpliga läkemedelsordinationer konstaterades (Tabell II), totalt 29 olika läkemedelsordinationer till 19 patienter inom 8 läkemedelsgrupper. Av dessa hade 15 patienter läkemedel som borde undvikits och 4 hade läkemedel där dosen borde reducerats. Utöver detta fanns 14 läkemedelsordinationer inom 5 läkemedelsgrupper till ytterligare 6 patienter där nedsatt njurfunktion var ett observandum. Sammanlagt 26 patienter av 48 var alltså berörda av teoretiskt olämpliga läkemedelsordinationer.
De teoretiskt olämpliga läkemedelsordinationerna granskades av en njurläkare och en oberoende distriktsläkare. Man fann därvid att flertalet av dessa inte hade någon praktisk klinisk betydelse. Hos 8 patienter fanns olämpliga läkemedelsordinationer som bedömdes ha praktisk betydelse. Teoretiskt olämpliga men praktiskt användbara läkemedelsordinationer var exempelvis vanliga läkemedel som T Trombyl 75mg 1 och T Selexid 200mg x 2.
Diskussion
I denna studie framkommer att endast 8 av 48 boende hade GFR >60 ml/min (normal eller lätt nedsatt njurfunktion) beräknat via S-cystatin C, medan 35 av 48 hade normalt S-kreatinin (kvinnor 50–90, män 60–100 mikromol/l). Beräknat med Cockcroft–Gaults ekvation hade 70 procent av patienterna måttligt till gravt nedsatt njurfunktion jämfört med 84 procent beräknat med S-cystatin C.
Om man utgår från njurfunktionen enligt S-cystatin C hade hälften av patienterna minst en läkemedelsordination som var teoretiskt olämplig, medan olämpliga läkemedelsordinationer av praktisk betydelse fanns hos 17 procent (8 personer).
Boende på SÄBO hade i Jönköpings län år 2001 i genomsnitt ca 10 stående läkemedelsordinationer [11], varav flera borde justeras vid nedsatt njurfunktion. Utan kunskap om att patienten har nedsatt njurfunktion riskerar fel läkemedel ordineras eller felaktig, oftast för hög, dos ges.
I denna studien ingick endast ett SÄBO, med ett begränsat antal patienter, men åldersfördelning och könsfördelning överensstämmer med fördelningrna i andra studier på SÄBO [11]. Läkemedelsanvändningen kan inte generaliseras eftersom ordinationerna gjorts av en läkare, men läkemedelsgenomgångar hade genomförts regelbundet, vilket resulterat i att antalet stående läkemedel per boende (Tabell 1) är klart lägre än på andra SÄBO [11]. Sannolikt är därför de läkemedelsproblem som beror på nedsatt njurfunktion snarast mindre än på andra SÄBO.
Flertalet patienter på ett äldreboende har nedsatt njurfunktion. Detta åskådliggörs dåligt om man utgår endast från S-kreatinin, som i de flesta fall är normalt eller endast lätt förhöjt. Om Cockcroft–Gaults ekvation använts rutinmässigt (inklusive vägning och mätning av patienterna) för omräkning till GFR hade flertalet patienter med nedsatt njurfunktion identifierats.
Analys av S-cystatin C anses speciellt värdefull på äldre personer eftersom S-kreatinin då är mindre tillförlitligt, men S-cystatin C har hittills fått begränsad spridning. Att S-kreatinin ger ett dåligt mått på njurfunktionen jämfört med S-cystatin C framgår också av andra studier [12, 13].
Ett byte har diskuterats
Ett byte från S-kreatinin till S-cystatin C har diskuterats. Motståndet har främst handlat om kostnader, eftersom S-cystatin C kostar 2–3 gånger mer än S-kreatinin (12 respektive 37 kronor år 2005 i Jönköpings län). Båda metoderna har felkällor. S-kreatinin påverkas främst av förändrad muskelmassa, normalt åldrande och malnutrition.
Felkällorna vid bestämningen av njurfunktion hos äldre med S-cystatin C är analysberoende. Vid normala värden för S-cystatin C (0,90 och 1,3 mg/l) är spridningen (±2 SD) 0,10–0,14, vilket motsvarar en felmarginal i GFR på ±7–8 ml/min. Vid nedsatt njurfunktion är felmarginalen betydligt mindre. Sammantaget skulle felkällorna vid bedömning av njurfunktionen minska betydligt om S-cystatin C användes på de grupper där S-kreatinin har klara brister, till exempel äldre.
Bör användas som rutinmetod
Resultaten från denna studie talar för att S-cystatin C, omräknat till GFR, bör användas som rutinmetod för att spegla njurfunktionen hos äldre personer, även om detta medför något högre analyskostnader. Ökad medvetenhet om nedsatt njurfunktion skulle ge underlag för bättre läkemedelsordinationer och därigenom minskad risk för läkemedelsrelaterade biverkningar hos våra äldre patienter.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.