Sammanfattat
Tekniken att utföra koronarangiografi och perkutan koronarintervention (PCI) har successivt förfinats. Från att framför allt ha använts vid angina pectoris utnyttjas PCI i dag för behandling av akut kranskärlssjukdom.
Den största prognostiska nyttan är vid behandling av patienter med hjärtinfarkt med ST-förhöjning.
Risken för nya förträngningar på grund av ärrbildning på platsen för ingreppet, s k restenos, har med hjälp av läkemedelsavgivande stentar minskats markant.
Framtida utvecklingsmöjligheter inom området är nya antitrombotiska läkemedel som minskar risken för stenttrombos och läkemedel eller metoder som minskar risken för myokardskada i samband med PCI.
Koronarangiografi (kontrastundersökning av hjärtats kranskärl) kan i dag genomföras med liten risk för allvarliga komplikationer. Undersökningen ska alltid bedömas i relation till patientens kliniska symtom och fynd. Tekniken för ballongvidgning introducerades 1977 av Andreas Gruntzig och två år senare i Sverige på Karolinska sjukhuset av Alfred Szamosi.
I dag är ballongvidgning med inläggning av stent (metallnät), numera benämnd perkutan koronarintervention (PCI), i hjärtats kranskärl standardbehandling för patienter med kärlkramp och hjärtinfarkt. Tack vare teknikutvecklingen inom både kateter- och bildområdet samt ökade erfarenheter hos PCI-operatörerna har frekvensen av lyckade ingrepp ökat avsevärt. I takt med introduktion av nya blodförtunnande läkemedel och läkemedelsavgivande stentar (DES, drug-eluting stent) har även de vanligaste begränsningarna med PCI-behandling, nämligen stenttrombos (trombbildning i en stent) och restenos (återkomst av förträngning på grund av ärrbildning på platsen för ingreppet), minskat.
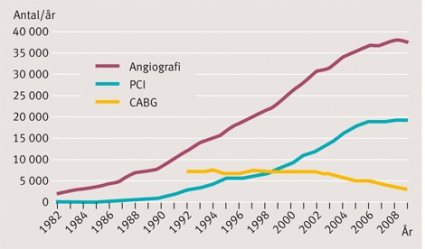
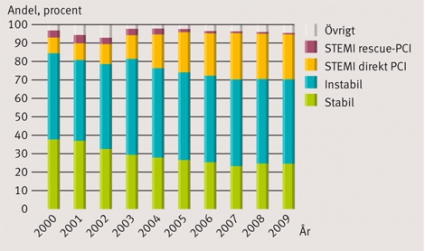
Det svenska koronarangiografi- och angioplastikregistret, SCAAR, med 100-procentig täckning avseende utförda undersökningar och behandlingar, ger unika möjligheter att följa trender och behandlingseffekter (Figur 1). I SCAAR noteras att den största andelen koronarangiografier och PCI utförs på patienter med akut kranskärlssjukdom (Figur 2).
Fortsatta utvecklingsmöjligheter för PCI-behandling är framför allt vid akut hjärtinfarkt, där forskning pågår för att hitta metoder för att minska myokardskadan som uppstår i samband med kärlets öppnande i form av reperfusionsskada och risk för embolisering.
Koronarangiografi – grunden för fortsatt behandling
Undersökning av hjärtats kranskärl med hjälp av kateter och kontrastmedel under röntgengenomlysning ger värdefull information om kranskärlssjukdomens utbredning och grad och utgör grunden för den fortsatta farmakologiska och interventionella behandlingen [1]. Risken för komplikationer är liten, ca 2–4 procent, och framför allt relaterad till insticksstället. Den vanligaste lokala komplikationen vid koronarangiografi utförd via a femoralis är att hematom uppstår. Om hålet i artären inte sluter sig kan ett pseudoaneurysm uppstå, vilket kan kräva behandling, vilket i sin tur förlänger vårdtiden. Koronarangiografi via a radialis orsakar sällan blödningskomplikationer men kan i undantagsfall leda till att artären ockluderar. Genom ett Allens test måste man därför förvissa sig om att god kollateralförsörjning föreligger. Allvarligare komplikationer är framför allt risken för stroke, då katetern kan peta loss aterosklerotiska plack från aorta ascendens eller aortabågen. Denna komplikation förekommer hos ca 0,1–0,5 procent, beroende på ålder och aterosklerossjukdomens utbredning. Risken för hjärtinfarkt och död ligger på ca 1/1 000 koronarangiografier [2].
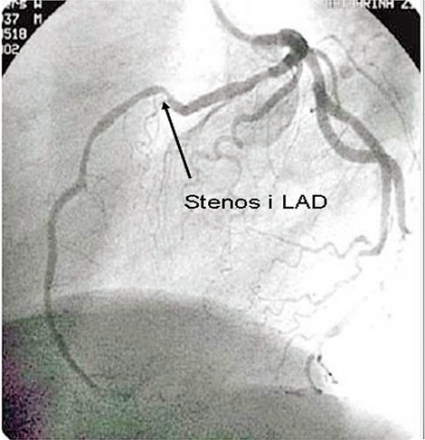
Det vanligaste sättet att bedöma förträngningar (stenoser) i kranskärlen är visuellt. Historiskt har man ansett stenoser som minskar kranskärlets diameter med 50 procent eller mer vara betydelsefulla (signifikanta) för uppkomst av ischemi [1].
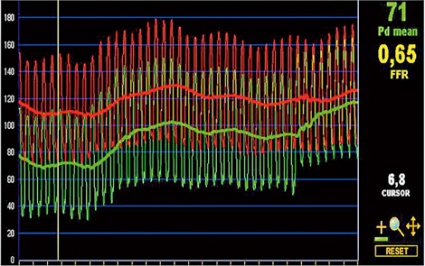
För att bedöma stenosens fysiologiska flödesbegränsningen kan intrakoronar tryckmätning göras med hjälp av en tryckgivare som sitter i änden av en tunn metalledare, som under samtidig adenosinadministration mäter blodtrycket distalt om stenosen. Det relativa tryckfallet, jämfört med trycket proximalt i kärlet, som benämns fractional flow reserve (FFR), ger information om stenosens roll för patientens symtom och prognos [1] (Figur 3).
Vid akut koronarsyndrom föreligger i de flesta fall indikation för koronarangiografi men vid stabil angina pectoris endast vid invalidiserande symtom trots adekvat medicinsk behandling. Vidare finns indikation för koronarangiografi hos patienter med hög risk för utbredd kranskärlssjukdom med uttalat patologiskt arbetsprov eller annat provokationstest samt återfall i anginasymtom efter genomförd PCI eller koronarkirurgi. Indikation för koronarangiografi föreligger inte vid låg risk för kranskärlssjukdom tillsammans med normalt arbetsprov och inga eller oklara symtom. Indikationer och kontraindikationer för koronarangiografi framgår av Fakta 1.
Förbättrad icke-invasiv diagnostik med datortomografisk angiografi kan minska behovet av koronarangiografi i framtiden. De relativt låga stråldoserna med den senaste generationens DT-angiografi tillsammans med ett högt negativt prediktivt värde för kranskärlssjukdom kommer sannolikt att öka metodens användning. Metoden har i dag klara begränsningar vid uttalad kranskärlssjukdom med förkalkningar och vid takykardier, särskilt förmaksflimmer [3].
PCI-behandling och läkemedelsavgivande stentar
Hos >90 procent av patienterna sker PCI-behandlingen genom ballongvidgning med inläggning av en stent i kranskärlet. Stentar introducerades i slutet av 1980-talet [4] och har inneburit minskad risk för akuta ocklusioner i det behandlade kärlet samt även minskat den kliniska restenosrisken jämfört med endast ballongvidgning.
Sedan början av 2000-talet har läkemedelsavgivande stentar (DES) minskat risken för kliniska restenoser ytterligare ner till ca 9 procent [5, 6]. Efter ett par års behandling med dessa stentar framkom i flera vetenskapliga rapporter (bl a från SCAAR) att behandling med DES var förenad med ökad mortalitet, sannolikt på grund av sena stenttromboser till följd av inkomplett endotelialisering. I senare SCAAR-rapporter med längre uppföljningstid har man inte kunnat påvisa ett samband mellan behandling med sådana stentar och ökat dödlighet [7].
Stabil kranskärlssjukdom och behandlingsmetoder
Den livligt diskuterade COURAGE-studien har visat att patienter med lindrig till måttlig angina pectoris och ej påvisbar ischemi med provokationstest med fördel kan behandlas med läkemedel och livsstilsmodifiering. Däremot bör patienter med angina pectoris med måttliga till uttalade besvär och icke-invasiva fynd av ischemi genomgå koronarangiografi och om möjligt revaskulariseras [8].
De senaste riktlinjerna från European Society of Cardiology rekommenderar att beslut om behandling med PCI eller koronarkirurgi i de flesta fall ska fattas multidiciplinärt, tillsammans med såväl hjärtkirurg som PCI-operatör [9]. Dokumentationen för båda metodernas förmåga att revaskularisera myokardiet är massiv med nära 20 000 litteraturreferenser. Ofta representerar dock inte studierna verkligheten. Vid analys av 15 randomiserade studier framkom att endast 5 procent av dem som genomgått angiografi kunde inkluderas, och enbart 30 procent av dem som räknats som flerkärlssjuka hade faktisk trekärlssjukdom [10]. Jämförelser av behandlingsmetoderna försvagas till nackdel för koronarkirurgi då cross-over till kirurgisk behandling ofta sker men analys av resultaten utförs enligt intention-to-treat-principen.
I en registerstudie från New York omfattande nära 60 000 patienter med minst tvåkärlssjukdom som följdes under tre år avled 16 procent av dem som behandlats med PCI jämfört med 11 procent av dem som opererats [11]. Det var inte en randomiserad studie, men efter justering för patientfaktorer beräknades att en initial PCI-strategi vid trekärlssjukdom innebar 36 procent högre risk att avlida inom tre år än kirurgi. I PCI-gruppen hade 27 procent behandlats med ny PCI och 8 procent med koronarkirurgi inom tre år. I den kirurgiska gruppen hade 5 procent behandlats med PCI och <1 procent genomgått en andra operation.
I randomiserade studier har ingen påtaglig överlevnadsvinst kunnat påvisas efter koronarkirurgi, men flertalet studier har inkluderat patienter med en- och tvåkärlssjukdom, en patientgrupp med god prognos. Metaanalyser av studier som jämfört PCI och koronarkirurgi har visat jämförbar tioårsöverlevnad [12, 13]. Det ska noteras att patienter med behandlad diabetes i BARI-studien hade signifikant bättre överlevnad tio år efter koronarkirurgi (58 procent) än efter PCI (46 procent) [13]. Sämre långtidsöverlevnad för diabetiker efter PCI har även dokumenterats i andra rapporter [15].
Den aktuellaste av de randomiserade studierna är SYNTAX, där 1 800 patienter med huvudstamsstenos eller trekärlssjukdom randomiserades till koronarkirurgi eller PCI med DES. Studien inkluderade patienter med komplex koronarsjukdom, och ett speciellt poängsystem utvecklades för att kunna skatta graden av kranskärlssjukdom [16]. Efter tre år var risken för död, hjärtinfarkt, stroke eller ny revaskularisering högre efter PCI (28 procent) än efter kirurgi (20 procent) (P < 0,001). Överlevnaden i grupperna skilde sig inte. Behovet av ny revaskularisering var 20 procent efter PCI jämfört med 11 procent efter kirurgi. Kirurgi resulterade i effektivare symtomlindring och färre symtomrecidiv som krävde ny intervention. Det fanns under första året, men inte därefter, en signifikant ökad risk för stroke efter koronarkirurgi. Det bör noteras att PCI-patienterna behandlades med klopidogrel under minst sex månader. Det har diskuterats om den högre risken för stroke året efter koronarkirurgi är resultatet av mindre effektiv trombocythämmande behandling än efter PCI.
Risken för hjärtinfarkt inom tre år efter ingreppet var högre i PCI-gruppen (7 procent) än i kirurgigruppen (4 procent). Det kan indikera att den mer perifera angreppspunkten på kranskärlet vid kirurgi i större utsträckning än efter PCI skyddar vid framtida koronarocklusioner. En intressant iakttagelse var att mortaliteten vid okomplicerad huvudstamsstenos var lika efter PCI och koronarkirurgi [17]. Vid låga SYNTAX-poäng sågs ingen skillnad i totalt utfall mellan grupperna, men vid poäng över 32 sågs en klar fördel för koronarkirurgi med 20 procents risk för död, hjärtinfarkt, stroke eller ny revaskularisering jämfört med 34 procent efter PCI.
Sammanfattningsvis visar randomiserade studier att PCI med fördel kan användas vid en- eller tvåkärlssjuka, men att koronarkirurgi är bättre vid uttalad kranskärlssjukdom, särskilt hos patienter med diabetes och vid höga SYNTAX-poäng. Arteriell revaskularisering med a thoracica interna har lång hållbarhet, och kirurgi kan ibland övervägas även vid en- eller tvåkärlssjuka, medan PCI kan vara säkrare vid uttalad kranskärlssjukdom och samtidiga komplicerande sjukdomar.Akut koronarsyndrom – huvudsaklig behandlingsindikation
Patienter med akut koronarsyndrom utgör i dag majoriteten av alla som genomgår PCI och koronarkirurgi (Figur 2). I regel utförs dessa behandlingar i anslutning till vårdtillfället. Det är framför allt FRISC II-studien som motiverat tidig invasiv utredning och revaskularisering [18]. Nyligen har det visats att PCI på kärl med instabila plack gör största nytta om den utförs tidigt i förhållande till symtomdebuten. Koronarkirurgi utförs helst efter några dagar om patienten kan stabiliserats medicinskt [9].
Primär PCI kallas PCI av det infarktrelaterade kärlet vid hjärtinfarkt med ST-förhöjning (STEMI). Två studier (DANAMI och PRAGUE 2) har visat att primär PCI, jämfört med trombolys, resulterar i en reduktion av risken för hjärtinfarkt, stroke eller död vid en månads uppföljning [19, 20]. Vid långtidsuppföljning (åtta år) av patienter i DANAMI-studien var den absoluta risken för det kombinerade effektmåttet ny hjärtinfarkt eller död lägre (35 procent jämfört med 41 procent) i PCI-gruppen än i trombolysgruppen [21].
En förutsättning för dessa resultat är en väl fungerande vårdkedja före, under och efter PCI tillsammans med god antitrombotisk behandling. Patienter som behandlats med trombolys med kvarstående ST-höjningar rekommenderas invasiv kranskärlsutredning och PCI. Även vid lyckad trombolysbehandling rekommenderas invasiv kranskärlsutredning och PCI inom 24 timmar från infarktdebuten [9].Framtidens PCI- och läkemedelsbehandling
Området antitrombotisk behandling har utvecklats starkt. Effektiva farmaka har eliminerat problem med non-responders. TRITON-TIMI 38-studien inkluderade drygt 13 000 patienter [22]. Syftet var att jämföra prasugrel med klopidogrel avseende effekterna kardiovaskulär död, hjärtinfarkt eller stroke under en uppföljning på minst tolv månader efter PCI. Resultaten visade att den relativa risken minskade med 19 procent vid prasugrelbehandling jämfört med dagens standardbehandling (klopidogrel). Prasugrel visade 52 procents reducerad risk för stenttrombos jämfört med klopidogrel både hos patienter som fått en metallstent och hos patienter som fått DES.
En fördefinierad subgruppsanalys på drygt 3 000 STEMI-patienter analyserade långtidseffekterna av prasugrel respektive klopidogrel. Studien visade att prasugrel förbättrade överlevnaden och minskade risken för ny hjärtinfarkt i denna patientgrupp. En månad efter ingreppet hade patienter som fått prasugrel 32 procent lägre risk att dö eller drabbas av ny hjärtinfarkt. Efter drygt ett år var skillnaden 21 procent. Resultaten för den totala populationen i TRITON-TIMI 38 visade på en viss förhöjd risk för allvarliga blödningar hos vissa patientgrupper som behandlats med prasugrel, framför allt de med tidigare TIA/stroke, ålder över 75 år eller vikt under 60 kg. Substudien på STEMI-patienter visade dock inte på någon signifikant skillnad mellan de två grupperna i fråga om förekomsten av allvarlig blödning.
PLATO-studien, som publicerades i slutet av år 2009, visade att den nya trombocythämmaren tikagrelor gav bättre effekt, utan nämnvärt ökad risk för blödning hos patienter med akut kranskärlssjukdom, än det beprövade klopidogrel [23]. I en senare analys av patientmaterialet har forskarna bakom studien tittat närmare på de ca 13 000 patienter, motsvarande 72 procent av det totala patientantalet, som planerades för tidig invasiv behandling med antingen PCI eller koronar bypass-kirurgi (CABG). Resultaten är samstämmiga med utfallet i studien som helhet. Hos de patienter som randomiserats till behandling med tikagrelor hade 9 procent drabbats av kardiovaskulär död, hjärtinfarkt eller stroke efter ett års uppföljning. Motsvarande siffra i gruppen som fick klopidogrel var 11 procent.Metoder för att minska reperfusionsskadan
Ett annat utvecklingsområde är läkemedel eller metoder som kan minska myokardskadan i samband med primär PCI vid STEMI. Behandling med PCI öppnar det avstängda kärlet för att åtgärda den syrebrist som uppstått i hjärtmuskeln. Problemet är att detta i sig kan leda till ytterligare skada av hjärtmuskeln via endera reperfusionskada eller distal embolisering. Reperfusionsskadan förklaras av att muskelcellerna går in i ett vilostadium då infarkten inträffar, och när blodet släpps på igen klarar inte cellerna av att ta emot allt syre, varför det bildas fria syreradikaler som skadar cellerna.
På senare år har man testat huruvida s k ischemisk konditionering kan användas för att minska reperfusionsskadan. Med ischemisk konditionering menas att man stänger av blodflödet tillfälligt i en del av kroppen för att genom hittills okända faktorer skydda samma kroppsdel eller en annan kroppsdel vid en längre tids stopp i blodflödet.
Danska forskare vid Århus universitetshospital i Skejby har visat att hjärtinfarktpatienter som får blodflödet tillfälligt avstängt i armen före ballongvidgningen delvis kan skyddas från skada i hjärtmuskeln [24]. I studien lottade man hälften av 333 patienter med STEMI till att få en blodtrycksmanschett uppblåst på överarmen suprasystoliskt fyra gånger redan i ambulansen på väg till sjukhuset för behandling med PCI. Patienterna undersöktes med myokardskintigrafi i samband med ballongvidgningen och 30 dagar därefter. På så sätt gick det att uppskatta hjärtmuskelskadan relaterad till riskarean för hjärtinfarkten, en markör för långtidsöverlevnad. Hos patienterna som genomgått ischemisk konditionering hade i median 75 procent av hjärtmuskelområdet klarat sig jämfört med 55 procent i kontrollgruppen. Forskarna konstaterar att skyddseffekten tycks vara bättre ju större område som hotas av infarkten. De anser att metoden, som de också tror kan ha betydelse i samband med trombolysbehandling vid stroke, bör utvärderas i en större studie.Trombektomi via specialkateter
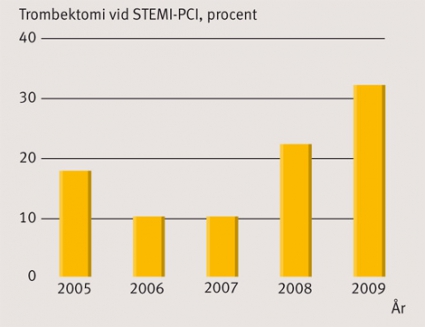
Behandling med trombektomi, som görs med hjälp av en specialkateter som suger ut den blodpropp som täpper till kranskärlet, har under senare år spridits snabbt i många länder. Teorin bakom trombektomins eventuella positiva effekt är att man kan minska trombosbördan som kan ge upphov till distal embolisering och som därmed kan förvärra myokardskadan. I Sverige behandlas i dag omkring hälften av patienterna med akut hjärtinfarkt med trombektomi före ballongvidgningen av kranskärlet (Figur 4). Fortfarande saknas dock säkra bevis för att trombektomi förbättrar prognosen. En studie vid ett holländskt sjukhus på drygt 1 000 patienter har visserligen visat dramatiskt ökad överlevnad efter trombektomi efter ett år [25].
En ny studie, TASTE (Thrombus aspiration in ST-elevation myocardial infarction in Scandinavia), kommer att undersöka om trombektomi vid STEMI sänker dödligheten efter 30 dagar. De flesta centra i Sverige och ett par större kliniker i Danmark och Island deltar i studien, som planeras inkludera totalt 5 000 patienter under två år. Patienterna kommer att randomiseras till gängse rutinbehandling eller till trombektomi före ballongvidgningen och stentinläggningen [26]. Unikt med denna studie är att den utförs med SCAAR som bas för både randomisering och uppföljning. Det innebär en möjlighet att genomföra randomiserade studier till förhållandevis låg kostnad. Man kan därtill testa olika behandlingskoncept utan att det finns ekonomiska incitament från läkemedels- eller materialtillverkare.Konklusion
Sammanfattningsvis är PCI-behandling i dag ett avancerat ingrepp, som framför allt utförs på patienter med akut koronarsyndrom, med god effekt på prognosen. Tekniken kan komma att förfinas ytterligare för att minska myokardskadans utbredning.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.