Sammanfattat
Den vanligaste inflammatoriska ledsjukdomen hos barn och tonåringar är juvenil idiopatisk artrit.
Juvenil idiopatisk artrit är en uteslutningsdiagnos.
Bara ca 1–3 procent av barn och tonåringar med juvenil idiopatisk artrit har positiv reumatoid faktor (RF) och/eller anticitrullinantikroppar (anti-CCP).
Barn med ledinflammation riskerar att utveckla asymtomatisk uveit, och risken är ökad om barnet är litet och har positiva antinukleära antikroppar (ANA).
Vården av barn med reumatiska sjukdomar har utvecklats mycket under de senaste årtiondena genom tillkomst av nya läkemedel, ökade kunskaper och bättre omvårdnad. I mitten av 1980-talet var det inte ovanligt att vi mötte barn med svåra skador av reumatisk ledsjukdom. Utbytta höftleder, stelopererade fotleder, felställda leder, tillväxthämning på grund av kortisonbehandling, synskada på grund av ögoninflammation och även rullstolsburna ungdomar var sådant vi såg och som vi sällan ser i dag.
Omhändertagandet har utvecklats mot nästan uteslutande poliklinisk vård. Tidigare var slutenvård vanligare, eftersom patienternas allmäntillstånd var sämre, behovet av fysikalisk terapi större på grund av ledskador med kontrakturer och fler patienter behövde opereras. Artroplastik, ett uttryck för permanent ledskada som ett resultat av »misslyckad« behandling, är mycket ovanlig i dag. Höftplastik, den vanligaste artroplastiken hos ungdomar med ledsjukdom, var (räknat på de senaste 20 åren) mest frekvent kring millennieskiftet.
Förekomsten varierar i olika delar av världen
Reumatisk ledsjukdom har tidigare benämnts juvenil kronisk artrit och juvenil reumatoid artrit. Beteckningarna har använts olika i olika delar av världen. Sedan 1997 finns en gemensam internationell benämning och definition – juvenil idiopatisk artrit (JIA) (Fakta 1).
Förekomsten av juvenil idiopatisk artrit varierar i olika delar av världen. I Norden är incidensen 11–14/100 000 barn och år upp till 16 års ålder, och den är vanligare ju längre norrut man kommer [1]. Vi uppskattar att ca 1 200–1 700 barn och tonåringar upp till 18 år har sjukdomen i Sverige i dag [2].
Klassifikation av samlingsbegreppet
Majoriteten av barn med juvenil idiopatisk artrit har inte samma kliniska bild som vuxna med reumatoid artrit. Juvenil idiopatisk artrit är ett samlingsbegrepp för barnens kroniska ledinflammatoriska sjukdomar, och de s k ILAR-kriterierna (International League of Associations for Rheumatology) indelar sjukdomen i åtta kategorier (Tabell I). Man brukar tala om debutform av sjukdomen så som den presenterar sig de första 6 månaderna och tiden därutöver som förloppsformen [3]. Den vanligaste kategorin är »kvarstående fåledsartrit«, vilket betyder ett engagemang av högst fyra leder under hela sjukdomsförloppet, även efter de första 6 månaderna.
Att man valt samlingsbegreppet juvenil idiopatisk artrit och inte gjort en uppdelning efter de olika sjukdomsformerna beror på att barnen kan ha en sjukdomsbild vid debuten, och först långt senare utvecklar sig sjukdomen till exempelvis en psoriasisartrit eller ankyloserande spondylit. Det är med andra ord svårt att under barnaåren förutsäga sjukdomsbilden under ungdomsåren och i vuxen ålder.
Psoriasis är ovanligt hos barn men förstagradsärftlighet för psoriasis, nagelförändringar och daktylit hos barnet är sådant som vi använder i klassifikationen av psoriasisartrit hos barn.
Sakroilit tar ofta tid att utveckla, men ärftlighet för HLA-B27-associerad sjukdom, HLA-B27 hos patienten, pojke över 6 år vid debut, akut främre uveit och/eller entesiter används för klassifikation av s k entesitrelaterad juvenil idiopatisk artrit, en motsvarighet till ankyloserande spondylit hos vuxna.
Med användning av kriterier för diagnostiken följer också att vissa barn inte kan placeras in i en viss grupp eller hamnar i två kategorier.
Ledsvullnad och morgonstelhet vanligaste debutsymtom
Sjukdomsbilden är varierande. De allra vanligaste debutsymtomen är ledsvullnad och morgonstelhet. Värmeökning över ett svullet ledområde är också vanligt. Låggradig feber förekommer ibland hos barn med engagemang av många leder vid debut och höggradig feber hos dem som utvecklat en särskild kategori av juvenil idiopatisk artrit, den s k systemiska formen.
Smärta är sällan det som dominerar den kliniska bilden hos de yngre barnen, sannolikt eftersom de har svårt att uttrycka var de har ont, men deras beteende och rörelsemönster tyder på smärta. Hos de äldre barnen är smärta en viktig del av symtombilden. Juvenil idiopatisk artrit kan också debutera med uveit, psoriasis eller inflammatorisk tarmsjukdom, och ledmanifestationerna kan komma långt senare.
En liten grupp av patienter har den systemiska formen. De insjuknar med svängande feber, oftast högst kvällar och nätter, utslag som blossar med febertopparna, svullna lymfkörtlar och svullen lever och/eller mjälte samt serosit (oftast perikardit). Alla patienter med den systemiska formen får inte alla symtom/kliniska fynd, och det är inte ovanligt att ledinflammationerna kommer i ett senare skede, efter månader eller år (Figur 1).
Utredningen styrs efter klinisk bild
Sjukdomen är en uteslutningsdiagnos varför utredningen styrs efter klinisk bild. Vanliga basprov är CRP och/eller SR, blodstatus med differentialräkning, ALAT och urinsticka. Ett normalt CRP- och/eller SR-värde utesluter inte juvenil idiopatisk artrit. Förhöjda nivåer av trombocyter är ett vanligt fynd. Positiva antinukleära antikroppar (ANA) står för ökad risk att utveckla uveit hos de yngre barnen och kan (framför allt om ANA är hög eller faller ut i en specifik autoantikropp) indikera att artriterna är en del av en inflammatorisk systemsjukdom hos de äldre barnen.
Reumatoid faktor (RF) och/eller antikroppar mot cykliskt citrullinerade peptider (anti-CCP) visar positiva värden hos ca 1–3 procent av barnen, nästan uteslutande hos dem som insjuknar med engagemang i många leder och är i tonåren.
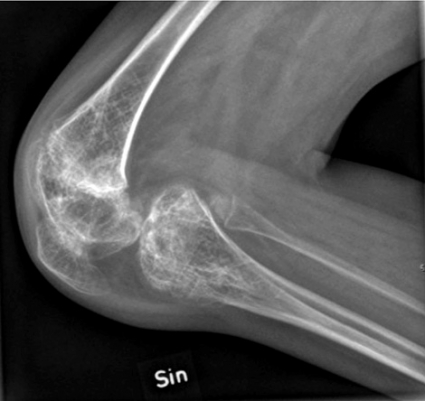
Om sjukdomen börjar i en enda led (monoartrit), röntgas leden för att utesluta t ex infektion och ortopedisk sjukdom. Det är också viktigt att utesluta borreliaartrit. Vid symtom på den systemiska formen är blododling, ultraljudsundersökning av hjärta och buk samt röntgen av lungor delar av utredningen. Benmärgsundersökning är viktig att överväga.
Uveit hos 15–20 procent
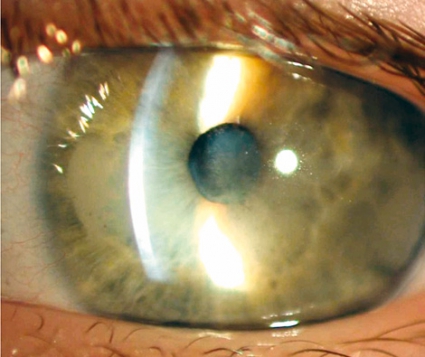
Ca 15–20 procent av alla barn med juvenil idiopatisk artrit utvecklar främre uveit (Figur 2, Fakta 2). Denna är oftast utan symtom och kan på sikt vara den största riskfaktorn för framtida skador av sjukdomen, som grav synnedsättning eller till och med blindhet. Risken för uveit är störst för små flickor med fåledsartrit (högst 4 leder engagerade) och med positiv ANA [4, 5]. På grund av risken för uveit behöver barn med juvenil idiopatisk artrit undersökas av ögonläkare med 3–6 månaders mellanrum under många år.
Medicinsk behandling
Den medicinska behandlingen av barn med juvenil idiopatisk artrit har blivit intensivare. Kunskap om den inflammatoriska processen talar för att tidigt insatt behandling är viktig. Stora undersökningar på vuxna och enstaka kontrollerade läkemedelsstudier på barn har utförts.
Grunden för den farmakologiska behandlingen av de reumatiska ledsjukdomarna är därför tidigt insatt aktiv behandling med målsättning att förhindra leddestruktion och funktionsinskränkning.
NSAID är baspreparat. Av de preparat som vi använder i dag är NSAID basterapi mot ledsmärta och ledstelhet och används bl a i väntan på utredning och mer kraftfull behandling. De flesta NSAID-preparat är inte registrerade för användning till barn. NSAID är en symtomatisk behandling utan visad ledskyddande effekt. När en patient har fått diagnosen juvenil idiopatisk artrit och har inflammerade leder inleds behandlingen med injektion av kortison i de påverkade lederna. Långverkande kortikosteroider lokalt minskar dramatiskt inflammation i ledkapseln med mindre smärta och ökad rörlighet som följd.
I dag vet vi också att kortisoninjektioner i leder inte skadar brosket, så som man tidigare ansett. Ledinjektioner är en viktig del i den primära behandlingen och i behandlingen av sjukdomsskov.
LARM-preparat har gett bättre behandlingsresultat. I mitten av 1980-talet började metotrexat användas till patienter med barnreumatism. Det innebar en stor förbättring av behandlingsresultaten [6]. Det senaste decenniet har indikationerna vidgats, och metotrexat används även parenteralt i form av subkutana injektioner. Frånsett för metotrexat är effekten av LARM (långverkande antireumatiska mediciner) dåligt vetenskapligt dokumenterad hos barn, och något vetenskapligt underlag för en remissionsinducerande effekt finns inte.
Metotrexat är förstahandsmedel när kortisoninjektion i leden/lederna inte har gett tillräckligt resultat eller när vi redan från början bedömer att kortisoninjektioner sannolikt inte kommer att räcka för att stoppa sjukdomen. Medlet har en gynnsam säkerhetsprofil med liten risk för allvarliga biverkningar i det dosintervall som används vid reumatiska sjukdomar. Tyvärr är det inte helt ovanligt med illamående efter en tids behandling [7]. Om metotrexat har dålig effekt i tablettform, är det indicerat att byta till subkutan behandling.
Förutom metotrexat är sulfasalazin det LARM-preparat som används för behandling av barn. Sulfasalazin har inte någon vetenskapligt bevisad effekt vid juvenil idiopatisk artrit i de få studier som genomförts. Läkemedlet ges i första hand till HLA-B27-positiva barn med artrit.
Utvecklingen inom läkemedelsbehandling vad gäller både substanser och hur dessa används har varit dramatisk de senaste 15 åren. Vi vet att det är viktigt att starta tidigt med behandling, men vi saknar prediktorer för vilka barn som behöver den mest intensiva behandlingen [8, 9] och vilka som klarar sig med enklare terapi.
Biologiska läkemedel kan ge dramatisk förbättring. Biologiska läkemedel riktade mot proinflammatoriska cytokiner har för barn liksom vuxna med reumatisk sjukdom i många fall inneburit en dramatisk förbättring av artritsjukdomen. Cytokinhämmare till barn och tonåringar är aktuellt först när metotrexat är prövat subkutant eller när biverkningarna av metotrexat är intolerabla. I första hand används en TNF-antagonist.
Behandlingen är kostsam – över 100 000 kr per år med vuxendos. Samhällsekonomiskt kan kostnaden dock försvaras om läkemedlen används på strikt indikation och om man räknar med att patienternas produktiva år blir fler genom att hon/han kan fullfölja skola och yrkesutbildning och delta i arbetslivet.
Den risk för allvarliga infektioner som befarades från början har visat sig vara mindre än man trodde men är ändå viktig att beakta. Epidemiologiska studier på vuxna och barn har inte kunnat påvisa någon ökad risk för malignitet som kan kopplas till behandling med TNF-alfa-hämmare [10].
Tillväxtrubbning är en komplikation
En av komplikationerna till juvenil idiopatisk artrit är tillväxtrubbning lokalt av skelettet, och vid långvarig inflammation finns risk för generellt hämmad längdtillväxt. Det finns forskning som visar normaliserad längdtillväxt hos barn med tillväxthämning under behandling med TNF-alfa-hämmaren etanercept [11].
Prognos – växer inte bort
En vanlig vanföreställning har varit att barnreumatism växer bort i tonåren. Epidemiologiska studier visar dock att sjukdomen är mer allvarlig än så. I ett nyligen publicerat arbete över nordiska barn med juvenil idiopatisk artrit var cirka hälften av patienterna inte i remission 8 år efter sjukdomsdebuten, ca 30 procent behandlades med ett LARM-preparat och 12 procent med ett biologiskt läkemedel [4].
Även om det inte är lika vanligt i dag med leddestruktioner som resttillstånd efter inflammation, är det inte ovanligt att vi fortsätter att behandla de tonåringar som vi uppfattar som välbehandlade i sin artritsjukdom för att de har kvarstående smärta. Finns det kvar en viss inflammation? Kan andra smärtlindrande åtgärder vara viktiga att arbeta med? Oftast behövs flera olika insatser.
Ett önskvärt mål är att redan vid diagnostillfället kunna identifiera de patienter som kräver mer intensiv medicinsk behandling och på motsvarande sätt förhindra att patienter som har god prognos inte utsätts för tyngre behandling än nödvändigt. Den mest intensiva farmakoterapin kan innebära en risk för allvarliga biverkningar i både det korta och det långa perspektivet. Detta ställer ökade krav på övervakning av effekter och bieffekter vid behandling med biologiska läkemedel.
Risk för långvarigt smärtsyndrom
Utredning och behandling av smärta är ett viktigt och vanligt inslag i vården. Den antiinflammatoriska behandlingen ger inte alltid tillräcklig smärtlindring. Fysikalisk behandling som värme/kyla, TNS (transkutan elektrisk nervstimulering) och akupunktur kan vara värd att pröva. Det finns studier som tyder på att smärta kan förstärka inflammation genom smärtmediatorer som är proinflammatoriska.
Vi vet att barn med reumatisk sjukdom inte härdas i sin smärta utan tvärtom. Långvarig smärta riskerar att påverka smärtreceptorer och nervbanor negativt med sänkt smärttröskel som följd. Ibland hamnar våra patienter i ett långvarigt smärtsyndrom, där det är en stor utmaning att förstå hur mycket som handlar om behovet av en bättre farmakologisk behandling av ledsjukdomen och vad som kräver andra insatser i smärtlindrande syfte. Vi vet också genom kvalitativa studier att smärtan ger dessa barn en känsla av utanförskap.
Det är viktigt att arbeta med barnets strategier för att hantera smärtan så att de blir så konstruktiva som möjligt. Avspänning och god sömn tillsammans med fysisk träning är viktiga faktorer. Kognitiv beteendeterapi (KBT) och ACT (acceptance and commitment therapy) är metoder att överväga. ACT är en vetenskapligt förankrad psykoterapeutisk metod och en ny form av KBT.
För att vården av barn med reumatiska sjukdomar ska fungera optimalt krävs insatser från många yrkeskategorier. Förutom barnläkare eller barnreumatolog och barnsjuksköterska behövs sjukgymnast, arbetsterapeut, kurator och psykolog. Att arbeta tillsammans i ett team med barnet i centrum är ovärderligt. Utredning och behandling av reumatiska sjukdomar i barndomen spänner över många kunskapsområden och för att ämnesområdet ska utvecklas optimalt behöver vi samarbeta mellan professionerna. Med nationella och internationella nätverk breddas kunskaperna, och vi är med i en snabb utveckling (Fakta 3).
*
Potentiella bindningar eller jävsförhållanden: Stefan Hagelberg, Anders Fasth och Lillemor Berntson har deltagit i flera expertgruppsmöten arrangerade av Abbott. Anders Fasth och Lillemor Berntson deltog under 2011 i ett expertgruppsmöte med Roche under vilket Anders Fasth också föreläste. Anders Fasth har erhållit föreläsningsarvode från Bristol-Myers Squibb och deltagit i kliniska prövningar sponsrade av Abbott, Merck Sharp & Dohme och Pfizer.